Clear Sky Science · nl
Stratificatie op voorschrift‑dosering verbetert deep learning‑gebaseerde VMAT‑dosisvoorspelling bij lokaal gevorderde NSCLC
Waarom slimmer gerichte radiatie belangrijk is
Wanneer artsen gevorderde longkanker behandelen met bestraling, balanceren ze nauwkeurig: genoeg energie leveren om de tumor onder controle te krijgen en tegelijk kwetsbare omliggende organen sparen. Het opstellen van zulke plannen is traag, complex en hangt sterk af van de ervaring van de planner. Deze studie onderzoekt hoe kunstmatige intelligentie het stralingspatroon in de borstkas kan voorspellen en toont vooral aan dat het trainen van de AI met zorgvuldig gegroepeerde dosisniveaus de voorspellingen nauwkeuriger en klinisch bruikbaarder maakt.
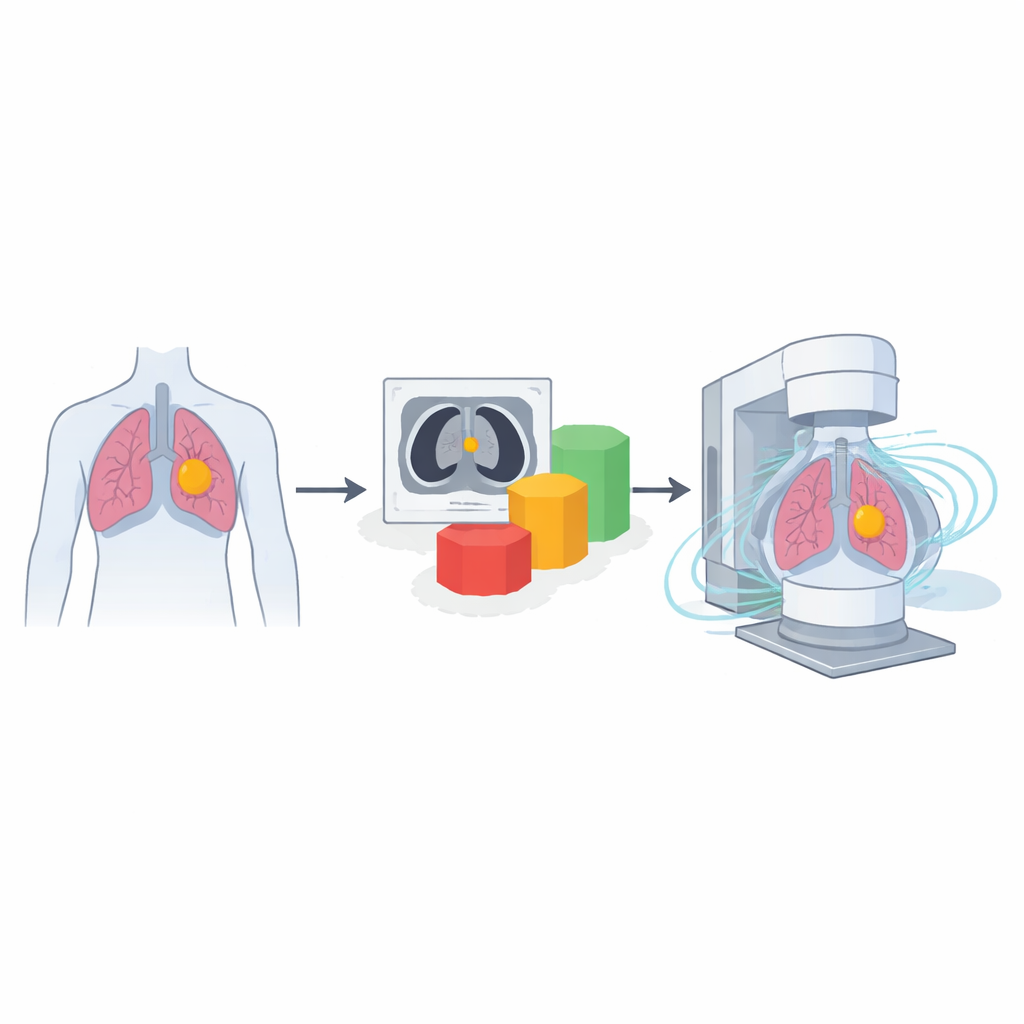
Hoe longkanker met gerichte bundels wordt behandeld
De meeste mensen met lokaal gevorderde niet‑kleincellige longkanker komen niet in aanmerking voor operatieve verwijdering van de tumor. In plaats daarvan krijgen zij vaak chemotherapie in combinatie met sterk gevormde bestralingsbundels die in bogen rond de borstkas bewegen, een techniek die bekendstaat als VMAT. Het doel is de tumor te voorzien van een hoge, uniforme dosis terwijl de blootstelling van longen, hart, slokdarm en ruggenmerg beperkt blijft. Het bereiken van dit evenwicht vereist doorgaans meerdere ronden van proef‑en‑foutaanpassingen, wat tijd kost en behandelbeslissingen kan vertragen. Als artsen snel kunnen inschatten welk dosispatroon realistisch haalbaar is voor een individuele patiënt, kunnen ze eerder de beste behandelingsstrategie kiezen.
Een algoritme leren dosispatronen te herkennen
De onderzoekers grepen naar deep learning, een vorm van AI die patronen rechtstreeks uit beelden leert. Ze verzamelden CT‑scans en voltooide behandelplannen van 72 longkankerpatiënten die met VMAT werden behandeld. Voor elke patiënt rekenden ze opnieuw uit hoe hetzelfde bundel‑opzet drie verschillende totale doses zou afleveren: 50, 54 en 60 gray (Gy), de gebruikelijke eenheid voor bestraling. Elk geval werd omgezet in een driedimensionale grid met markeringen voor de tumor, belangrijke organen en de onderliggende CT‑afbeelding. Deze negen kanalen aan informatie werden ingevoerd in een 3D U‑Net, een veelgebruikt neuraal netwerkontwerp dat kan leren hoe dosis door het lichaam vloeit op basis van anatomie.
Waarom groeperen op voorschrift‑dosis ertoe doet
Een centrale vraag was hoe om te gaan met het feit dat patiënten verschillende totale voorschrift‑doses krijgen. Het team bouwde vier verder identieke AI‑modellen. Drie waren "single‑prescription" modellen, elk alleen getraind op plannen met één dosisniveau (50, 54 of 60 Gy). Het vierde model mengde 50 en 60 Gy‑gevallen zonder het netwerk te vertellen welke voorschrift het zag. Bij testen op nieuwe patiënten kwamen de voorschrift‑specifieke modellen beter overeen met de werkelijke dosis in de tumor, waarbij zowel dekking als hotspots dicht bij de klinische plannen bleven, doorgaans binnen enkele Gy. Daarentegen maakte het gemengde model merkbaar grotere fouten in de hoogste dosisregio's van de tumor en rond het ruggenmerg, waar de dosis onder strikte veiligheidslimieten moet blijven.
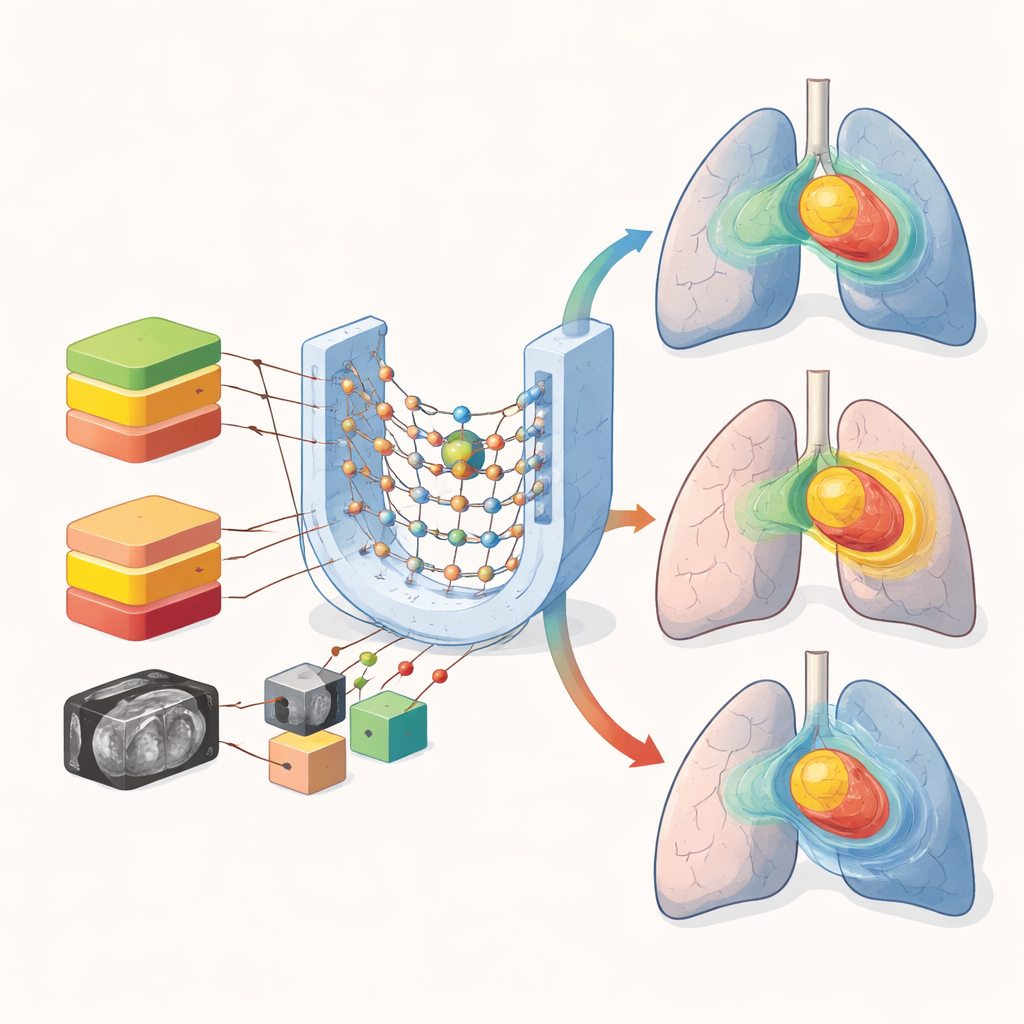
Belangrijke organen beschermen en tegelijkertijd planning versnellen
Opmerkelijk genoeg presteerden het gemengde en de gestratificeerde modellen voor veel organen zoals longen, hart en slokdarm vergelijkbaar. Gemiddelde dosisfouten in deze grotere structuren bleven bescheiden over alle benaderingen. De belangrijkste zwakte van het mengen van voorschriften trad op in kleine, gevoelige structuren zoals het ruggenmerg, waar een steile dosisafval essentieel is. Visuele controles van de voorspelde dosiskaarten lieten zien dat alle modellen de algemene vorm van het hoogdosisgebied in de tumor vastlegden, maar dat het mengen van voorschriften leidde tot meer vervaging in scherpe gradiënten en lage‑dosisgebieden van de longen. Deze verschillen, hoewel numeriek subtiel, kunnen van belang zijn wanneer artsen beslissen of een hogere voorschrift‑dosis veilig is.
Wat dit betekent voor patiënten en klinieken
Voor patiënten vervangt dit werk de zorgvuldige dosisberekeningen van klinische systemen niet, maar het kan helpen om tijd en moeite te richten op plannen die werkelijk haalbaar en veilig zijn. Door te laten zien dat het groeperen van trainingsdata op voorschrift‑dosis AI‑voorspellingen aanzienlijk verscherpt — vooral voor tumorbedekking en bescherming van het ruggenmerg — benadrukt de studie een praktische ontwerpkeuze die computerondersteuning betrouwbaarder kan maken. Met verdere tests in grotere en diversere patiëntengroepen zouden zulke modellen alledaagse hulpmiddelen kunnen worden die artsen een snelle, anatomie‑gebaseerde preview geven van waarschijnlijke stralingsafwegingen, en zo meer consistente en betere behandelingsplanning ondersteunen.
Bronvermelding: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Trefwoorden: radiotherapie bij longkanker, deep learning dosisvoorspelling, VMAT‑planning, optimalisatie van behandelplannen, organen in risico