Clear Sky Science · nl
De dubbele rol van extracellulaire vesikels bij stolling en immuunmodulatie bij glioblastoom
Waarom bloedstolsels belangrijk zijn bij hersenkanker
Mensen met de diagnose glioblastoom, de meest agressieve vorm van hersenkanker, lopen vaak een onverwacht risico: gevaarlijke bloedstolsels in de benen of de hersenen. Deze stolsels kunnen de overleving verkorten en de toch al complexe behandelingen bemoeilijken. Deze studie stelt een eenvoudige maar cruciale vraag: wat is het aan glioblastoomcellen dat het omliggende bloed zo vatbaar maakt voor stolling, en hoe herleven de kleine deeltjes die ze in het bloed afgeven ook het immuunsysteem van het lichaam?
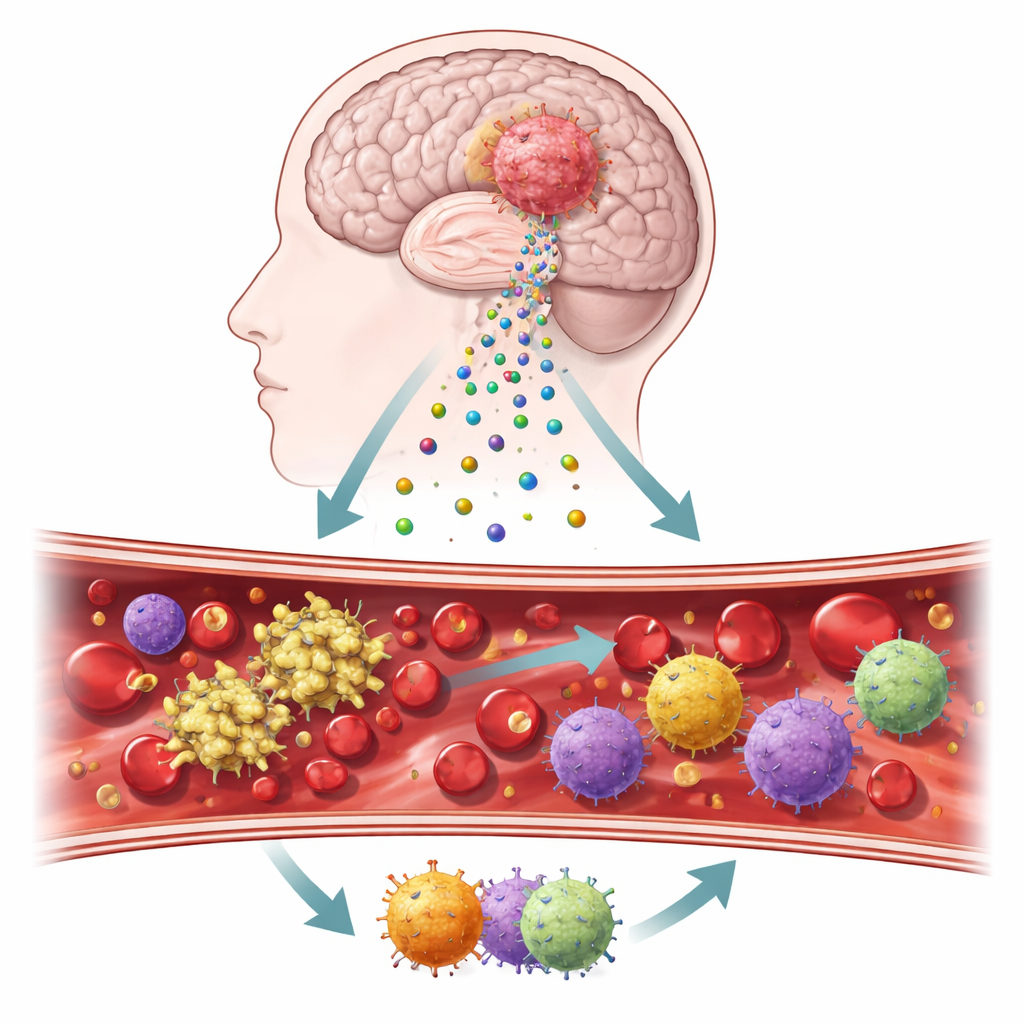
Kleine boodschappers die een hersentumor verlaten
De onderzoekers concentreerden zich op microscopische blaasjes, extracellulaire vesikels genaamd, die van tumorcellen afknoppen en door bloed en hersenweefsel zweven. Deze vesikels dragen op hun oppervlak twee sleutelproteïnen, tissue factor en podoplanine, die bekendstaan om het aanzwengelen van stolling en het beïnvloeden van ontsteking. Met tumormonsters, tijdens operaties afgenomen bloed en kweekcellen uit patiënten tumoren bouwde het team een stapsgewijze werkwijze om te volgen hoe deze moleculen zich gedragen in echte patiënten en in gecontroleerde laboratoriumtesten. Ze vergeleken ook tumormateriaal met normaal hersenweefsel om te bepalen hoe sterk deze stollingsgerelateerde signalen aanstaan.
Een rustige bloedbaan maar een geprepareerde tumorzône
Standaard ziekenhuisonderzoeken suggereerden dat het bloed van veel patiënten voor de operatie verrassend normaal leek: gebruikelijke stollingstijden en stollingsstevigheidswaarden lagen grotendeels binnen referentiewaarden. Toch ontstond bij onderzoek van de tumoren zelf een ander beeld. Glioblastoomweefsel vertoonde consequent hoge niveaus van tissue factor en podoplanine en zeer lage niveaus van een natuurlijke remmer, de tissue factor pathway inhibitor. Uit patiënten afgeleide tumorcellijnen behielden dit patroon grotendeels in kweek, wat bevestigt dat het ‘stolingsvriendelijke’ profiel een intrinsieke eigenschap van de kankercellen is. Wanneer deze cellen, of de vesikels die ze afgeven, in het laboratorium met plasma werden gemengd, vormden zich sneller stolsels, vooral via het zogenaamde extrinsieke pad dat afhankelijk is van tissue factor.
Verschillende tumorcellen, verschillende stollingsstrategieën
Niet alle glioblastomen gedroegen zich hetzelfde. Sommige uit patiënten afkomstige cellijnen hadden zeer veel tissue factor, andere meer podoplanine en weer andere weinig van beide. Cellen rijk aan tissue factor waren het meest effectief in het verkorten van de stollingstijd, terwijl podoplanine-rijke cellen een bescheidener bijdrage leverden via effecten op bloedplaatjes. Toen één dergelijke cellijn in subgroepen werd gesorteerd die alleen tissue factor, alleen podoplanine, beide of geen van beide uitdrukten, bleven de cellen niet lang in die toestand. Over drie weken kropen ze terug richting gemengde profielen, wat wijst op een hoge mate van plasticiteit. Deze dynamische verschuiving ging gepaard met veranderingen in oxidatieve stress binnen de cellen, wat suggereert dat chemische stress in de tumor cellen richting een meer pro-stollende staat kan duwen.
Vesikels als vormgevers van hersen- en bloedimmuniteit
Het team onderzocht vervolgens hoe door tumoren afgeleide vesikels de eigen immuuncellen van de hersenen, microglia genoemd, en circulerende witte bloedcellen en neutrofielen beïnvloeden. Vesikels van sterk pro-stollende tumorlijnen werden gemakkelijk door microglia opgenomen en vertraagden hun migratie, terwijl ze ze richting een meer ontstekingsachtige, ‘M1-achtige’ toestand duwden en tekenen van cellulaire veroudering veroorzaakten. In de bloedbaan activeerden vesikels rijk aan tissue factor leukocyten, verhoogden de productie van reactieve zuurstofsoorten en stimuleerden de afgifte van plakkerige webachtige structuren door neutrofielen, bekend als extracellulaire vallen. Vesikels met podoplanine waren minder krachtig in het aanjagen van deze explosieve immuunreacties maar stimuleerden sterk een senescentie-achtig programma waarbij immuuncellen stoppen met delen en hun gedrag veranderen. Zelfs vesikels zonder beide sleutelproteïnen konden nog enige senescentie uitlokken, wat impliceert dat andere inhoud ook van belang is.
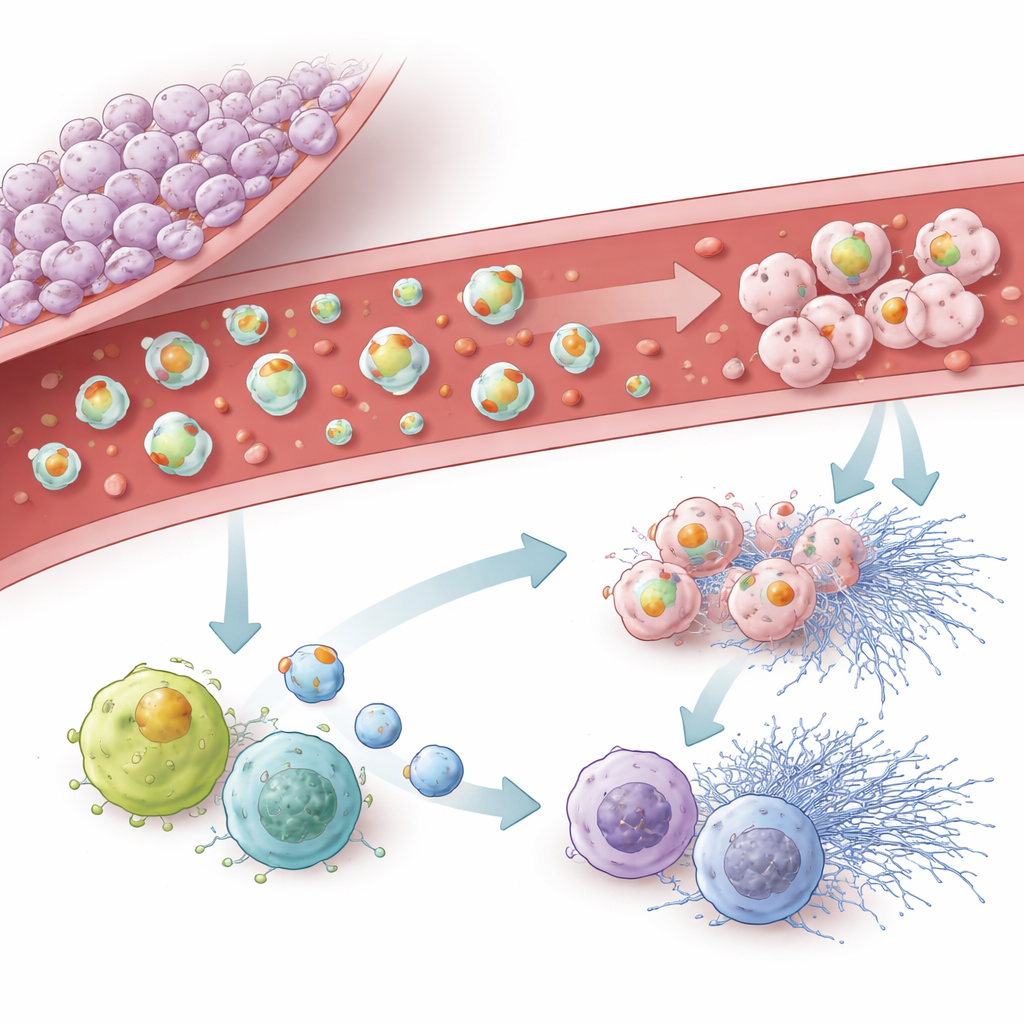
Wat dit betekent voor patiënten en toekomstige zorg
Samengevoegd tonen de bevindingen aan dat glioblastoom het bloed niet overal simpelweg dikker maakt. In plaats daarvan creëren de tumor en de vesikels die het afgeeft een gelokaliseerde, zeer complexe zone waar stolling en ontsteking elkaar versterken. Tissue factor blijkt de belangrijkste motor van stolselvorming en inflammatoire activatie, terwijl podoplanine een eigen invloed heeft op bloedplaatjes, immuunsenescentie en microglia-gedrag. Omdat deze vesikels circuleren en de toestand van de tumor weerspiegelen, zouden ze in de toekomst als bloedgebaseerde markers kunnen dienen om patiënten met een bijzonder hoog risico op stolsels te identificeren. Ze kunnen ook wijzen op meer gerichte preventiestrategieën die het pro-stollingsmachinerie van de tumor aanpakken zonder het bloed breed te verdunnen.
Bronvermelding: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Trefwoorden: glioblastoom, bloedstolsels, extracellulaire vesikels, tumormicro-omgeving, immuunrespons