Clear Sky Science · nl
Beoordeling van het dodecinescafoïde van Mycobacterium tuberculosis als multimerisatieplatform voor de immunogeniciteit van HPV L2-antigenen
Waarom dit onderzoek belangrijk is voor toekomstige vaccins
Humane papillomavirussen (HPV) veroorzaken bijna alle baarmoederhalskankers en een toenemend aandeel van andere kankers, maar huidige vaccins zijn complex om te produceren en dekken niet volledig alle gevaarlijke virustypen. Deze studie verkent een nieuwe manier om een eenvoudiger, breder beschermend HPV-vaccin te bouwen dat goedkoper, stabieler en wereldwijd gemakkelijker inzetbaar zou kunnen zijn, vooral in lage- en middeninkomenslanden. Door te herordenen hoe belangrijke virale proteïnefragmenten aan het immuunsysteem worden gepresenteerd, streven de onderzoekers ernaar het lichaam aan te zetten tot de productie van krachtige antilichamen tegen veel HPV-typen tegelijk.
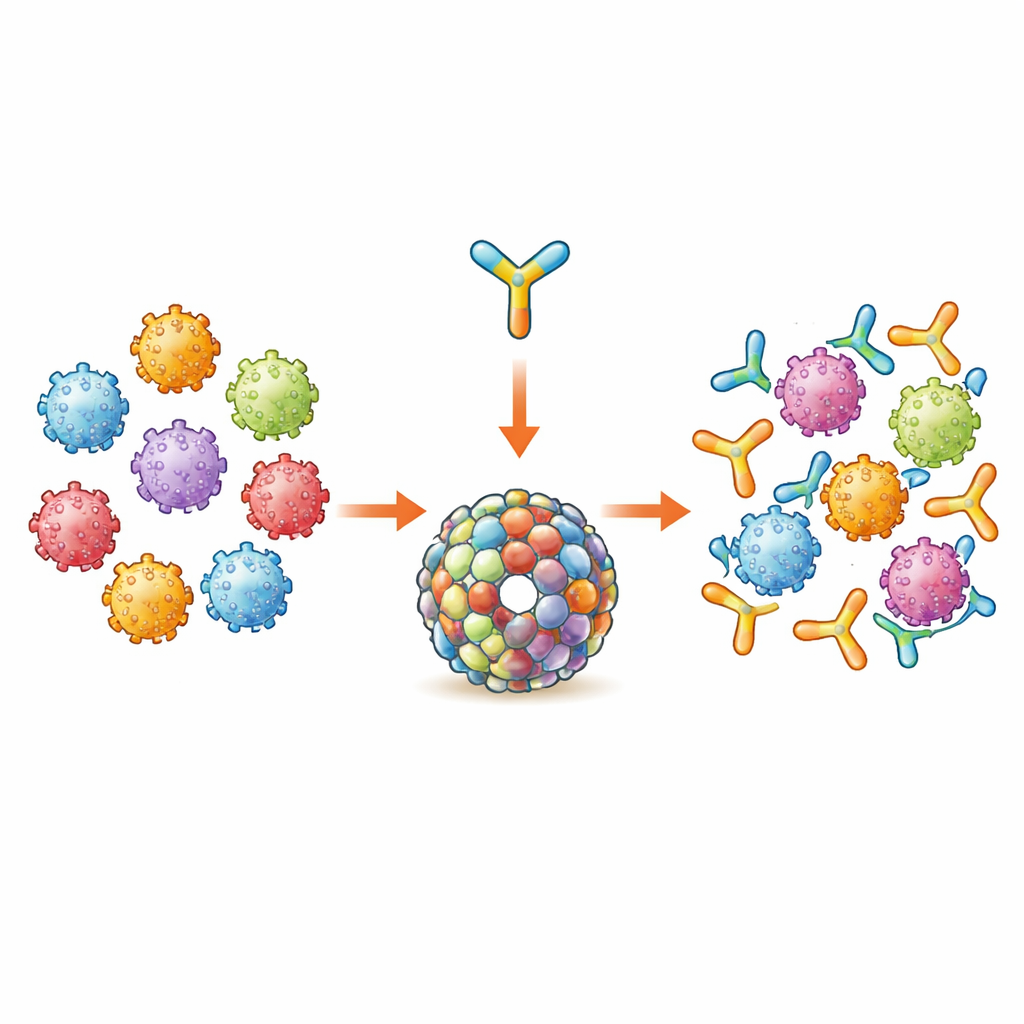
Een nieuw bouwblok voor HPV-bescherming
De huidige HPV-injecties vertrouwen op een viraal schaleiwit genaamd L1, dat assembleert tot virusachtige deeltjes die sterk antistoffen stimuleren maar voornamelijk tegen de weinig HPV-typen in elk vaccin. Het team concentreerde zich in plaats daarvan op een tweede viraal eiwit, L2, dat korte regio’s bevat die overeenkomen tussen veel HPV-typen en daardoor een bredere bescherming kunnen oproepen. Ze gebruikten een eerder ontworpen antigeen genaamd Trx-8mer, waarbij kleine geconserveerde L2-stukjes uit acht HPV-typen aan elkaar zijn gekoppeld en gepresenteerd op een stabiel drager-eiwit. Eerder onderzoek toonde al aan dat het samenbrengen van zeven van deze Trx-8mer-eenheden in een ringvormig complex (een vaccin genaamd PANHPVAX) sterke, kruisbeschermende antistoftiters produceert en nu in een vroeg stadium van humane testen zit.
Een bacterieel eiwit omvormen tot vaccinplatform
In deze studie probeerden de onderzoekers voorbij zeven kopieën te gaan en nog meer L2-antigenen in elk deeltje te proppen, volgens de theorie dat sterk repetitieve patronen bijzonder goed B-cellen activeren, de antistofproducerende cellen van het immuunsysteem. Ze kozen een klein, hittebestendig eiwit uit de tuberkelbacil, dodecin genoemd, dat van nature assembleert tot holle bolletjes van twaalf identieke subeenheden. Door Trx-8mer genetisch te fuseren met dodecin, creëerden ze meerdere nieuwe vaccinkandidaten die zichzelf zouden moeten samenstellen tot multimerische nanodeeltjes met veel kopieën van L2. Deze deeltjes konden in bacteriën worden geproduceerd, dankzij hun robuustheid bij hoge temperatuur worden gezuiverd, en met verschillende biofysische methoden worden geverifieerd als de beoogde nanoschaalstructuren.
Wanneer directe fusie niet voldoende is
Verrassend genoeg bleek het simpelweg direct bevestigen van de L2-lading aan het dodecin-scafoïde niet beter te presteren dan het bestaande heptamerische referentievaccin PANHPVAX in muizen. Hoewel de multimerische deeltjes zoals gepland vormden en neutraliserende antilichamen opwekten tegen zowel vaccins als niet-vaccins HPV-typen, waren de titers over het algemeen lager dan die gezien met PANHPVAX. Het toevoegen van een ingebouwd helper-T-cel-epitoop, dat soms antistoftiters verhoogt, verbeterde de prestaties ook niet. Structurele modellering en functionele data suggereerden dat de omvangrijke, direct gefuseerde Trx-8mer-eenheden elkaar mogelijk dicht opeen drukken en belangrijke L2-regio’s verbergen voor B-celreceptoren, waardoor de immuunrespons werd afgezwakt ondanks dat er theoretisch meer antigeenkopieën aanwezig waren.
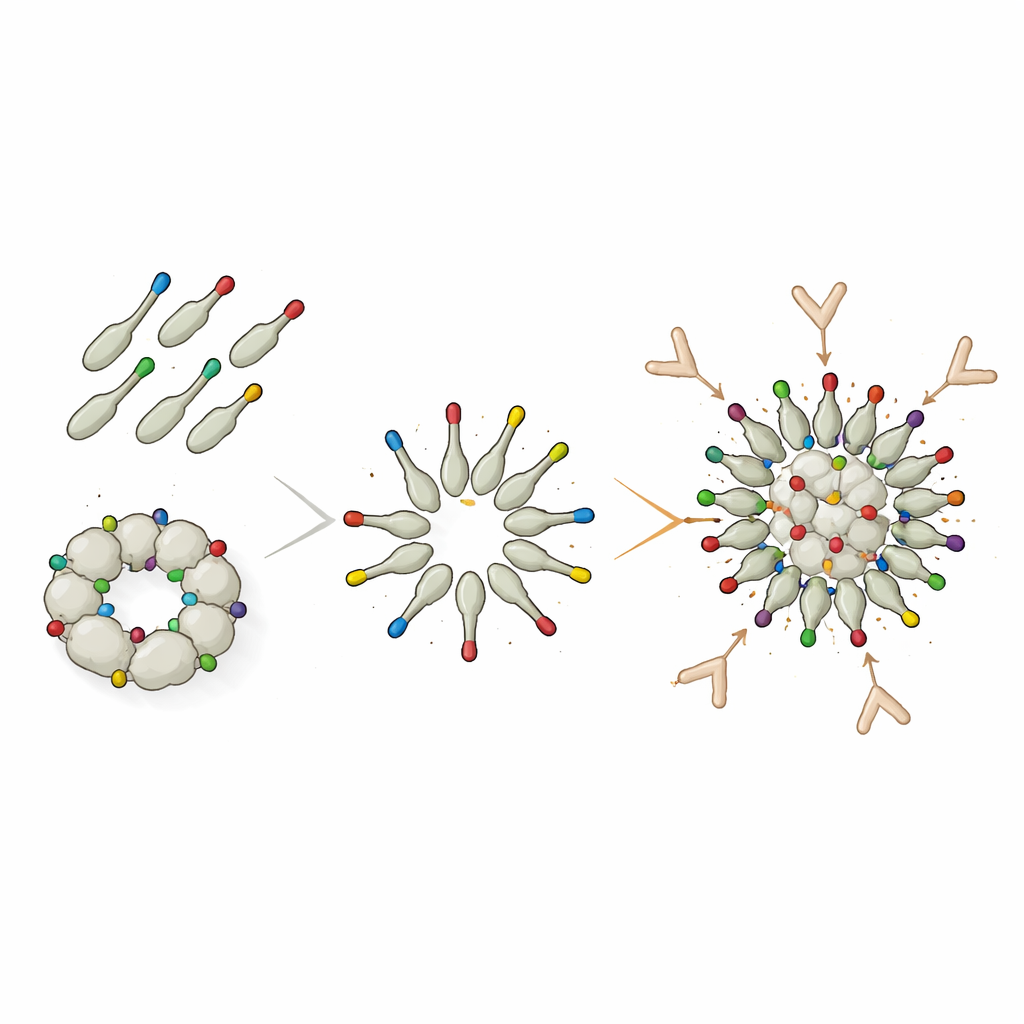
Click-on decoratie verhoogt reacties sterk
Om deze structurele beperkingen te omzeilen schakelde het team over op een modulair “eiwit-lijm”-systeem genaamd DogTag/DogCatcher. In dit ontwerp werd dodecin eerst geproduceerd met alleen een klein DogTag-peptide aan het oppervlak, zodat het vrij kon assembleren tot schone nanodeeltjes. Separaat werd het Trx-8mer-antigeen gefuseerd met de corresponderende DogCatcher-partner. Wanneer ze werden gemengd, sluiten Tag en Catcher zich via een spontane covalente binding aan elkaar, waarmee de Trx-8mer-eenheden met L2 op de vooraf gevormde dodecin-deeltjes werden geklikt. Hoewel slechts ongeveer de helft van de Trx-8mer-aan het eind aan nanodeeltjes vastzat en de rest vrij in oplossing bleef, produceerden muizen die met dit gedecoreerde construct werden gevaccineerd veel hogere neutraliserende antistoftiters tegen meerdere hoogrisico-HPV-typen dan bij de direct-gefuseerde deeltjes. Voor sommige typen, zoals HPV16, presteerden de gedecoreerde deeltjes zelfs beter dan PANHPVAX.
Gevolgen voor betaalbare, brede HPV-vaccins
Al met al toont de studie aan dat de ruimtelijke ordening van antigenen belangrijker kan zijn dan het aantal kopieën op papier. Het vooraf assembleren van een stevig nanodeeltjesscafoïde en het daarna vastklikken van antigenen gaf de L2-fragmenten gunstige tussenruimtes en oriëntaties, wat leidde tot sterkere en bredere antistofreacties in muizen. Omdat de dodecin-gebaseerde deeltjes klein, zeer thermisch stabiel en in bacteriën produceerbaar zijn, vormen ze veelbelovende kandidaten voor volgende generaties HPV-vaccins die goedkoper te vervaardigen zijn en minder afhankelijk van koudeketens. Met verdere verfijning en testen zou dit modulaire platform vaccins kunnen ondersteunen die tegen veel HPV-typen beschermen in één toegankelijke injectie, en mogelijk zelfs aangepast kunnen worden om preventieve en therapeutische componenten in hetzelfde deeltje te combineren.
Bronvermelding: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Trefwoorden: HPV-vaccin, nanodeeltje-immunogeen, L2-antigeen, dodecin-scafoïde, eiwitconjugatie