Clear Sky Science · nl
Tenoxicam-beladen bioglas/chitosaancomposieten voor botweefselengineering: in vitro karakterisering, gestage geneesmiddelafgifte en antimicrobiële activiteit
Gebroken botten genezen met slimere materialen
Wanneer een bot ernstig beschadigd is, volstaan metalen platen en schroeven vaak niet. Artsen moeten pijn en zwelling dempen, op de loer liggende ziekteverwekkers bestrijden en nieuw botgroei stimuleren. Deze studie onderzoekt één enkel, slim materiaal dat al die taken tegelijk probeert uit te voeren: een miniatuur, botachtige scaffold die geleidelijk een ontstekingsremmend middel afgeeft terwijl het stevig aan het skelet hecht en schadelijke bacteriën ontmoedigt.
Een nieuw soort botpleister
De onderzoekers richtten zich op een hardnekkig probleem in de orthopedie: grote botdefecten die pijnlijk, ontstoken en vatbaar voor infectie zijn. Standaard pijnstillers en antibiotica verspreiden zich door het hele lichaam en bereiken mogelijk nooit voldoende concentraties precies daar waar ze het hardst nodig zijn — het beschadigde gebied. Het team wilde een lokale “botpleister” ontwikkelen die direct in de beschadigde plek kan worden geplaatst, groeiend weefsel ondersteunt en wekenlang geneesmiddel gelijkmatig afgeeft, terwijl het lichaamsvriendelijk blijft.
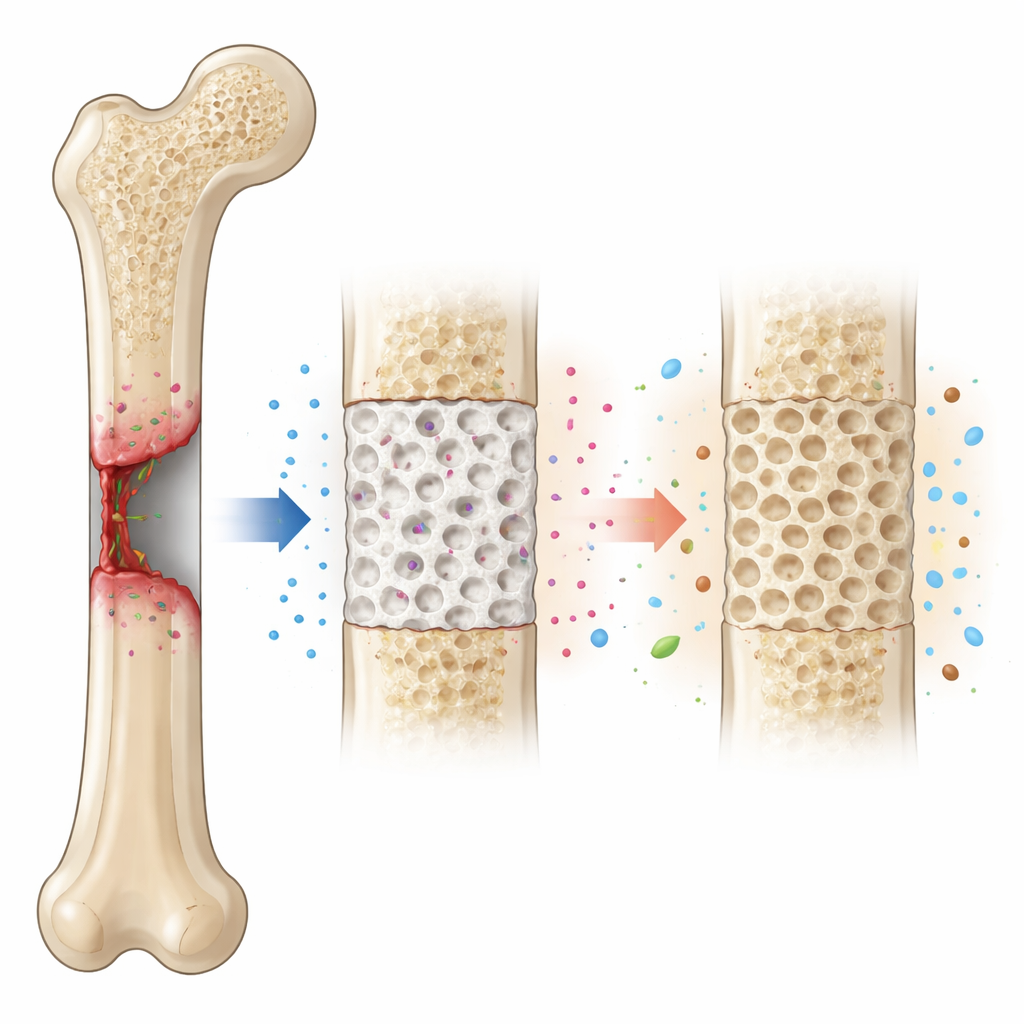
Glas, natuurlijke suiker en pijnverlichting mengen
Het materiaal dat ze ontwikkelden combineert drie sleutelcomponenten. Ten eerste bioglas, een speciaal type glas dat al bekendstaat om zijn sterke hechting aan bot door het vormen van een dunne minerale laag vergelijkbaar met natuurlijke botkristallen. Ten tweede chitosan, een afbreekbare stof afgeleid van schaaldieren die flexibele, poreuze structuren kan vormen en milde antimicrobiële eigenschappen heeft. Ten derde Tenoxicam, een veelgebruikt middel om pijn en ontsteking te verminderen. Met behulp van een chemische route die het sol-gelproces wordt genoemd, mengde het team verschillende hoeveelheden Tenoxicam (1, 2 en 3 gewichtprocent) in een mengsel van bioglas en chitosan, en perste de resulterende poeders vervolgens tot kleine schijfjes.
Testen hoe de botpleister zich in het lichaam gedraagt
Om na te bootsen wat er in een mens gebeurt, werden de schijfjes meer dan een maand lang geweekt in een vloeistof die menselijk bloedplasma nauwkeurig imiteert. Geavanceerde instrumenten werden gebruikt om te zien hoe hun oppervlakken veranderden. Spectroscopie- en röntgenmetingen lieten zien dat alle monsters snel een laag hydroxyapatiet ontwikkelden, hetzelfde mineraal dat een groot deel van natuurlijk bot vormt. Deze nieuwe laag werd in de loop van de tijd meer geordend en overvloediger, vooral in het monster met de hoogste medicijnlading. Elektronenmicroscoopbeelden toonden een sterk poreus oppervlak gevuld met onderling verbonden poriën. Zulke porositeit is cruciaal: het laat lichaamsvloeistoffen, voedingsstoffen en botvormende cellen doordringen en verankeren, waardoor het implantaat goed kan integreren met levend weefsel.
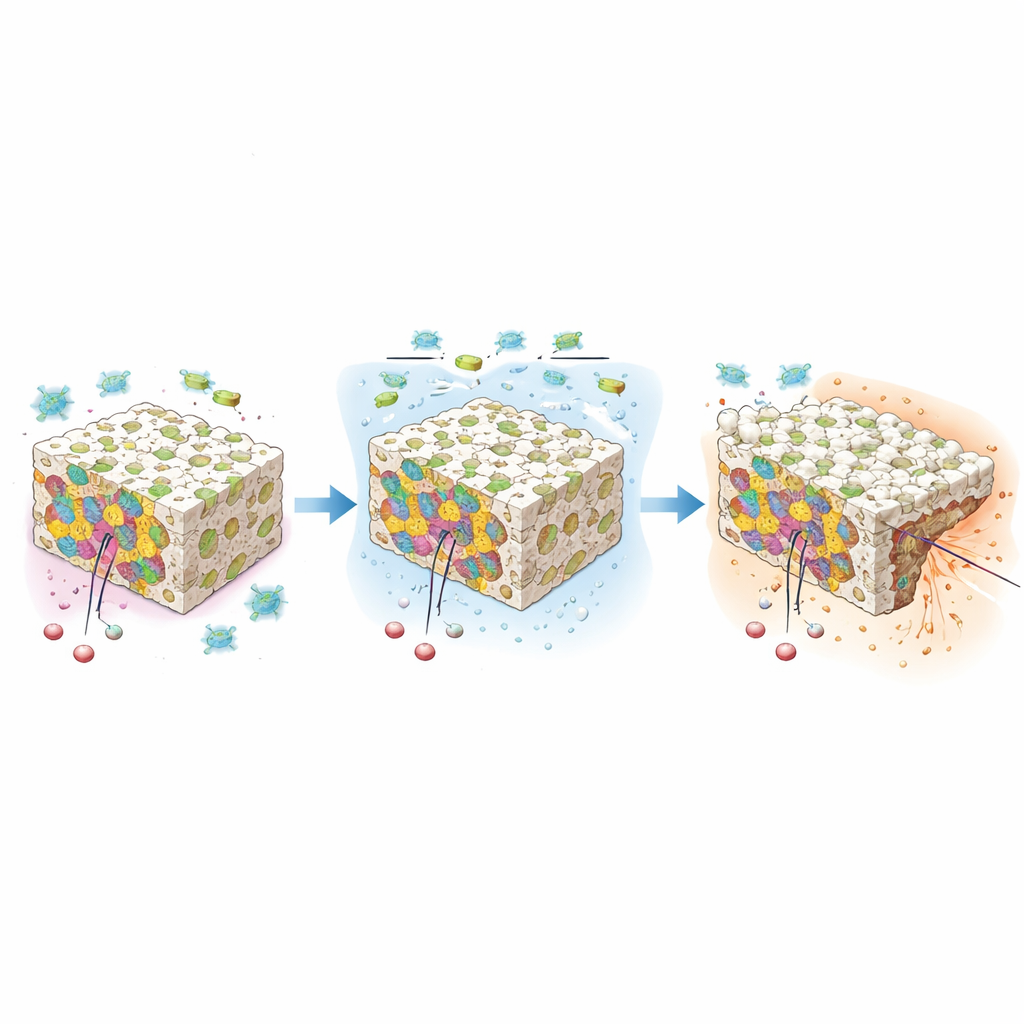
Langzame, constante medicijnafvoer en ingebouwde verdediging tegen bacteriën
De wetenschappers volgden ook hoe Tenoxicam zich over 33 dagen uit de schijfjes verspreidde. Alle drie de varianten gaven het geneesmiddel vrij in drie fasen: een snellere vroege piek, een middenperiode met gestage afgifte en een langzamere staartfase. In het algemeen volgde de afgifte grotendeels zogenoemd nulde-ordegedrag, wat betekent dat het medicijn vrijwel constant vrijkwam — ideaal om stabiele pijn- en ontstekingscontrole te behouden zonder grote pieken of dalen. Het meest beladen monster gaf de grootste totale hoeveelheid vrij terwijl het toch gecontroleerd bleef. Tegelijkertijd perste het team de materialen tot kleine pelletjes en plaatste die op bacteriekweekplaatjes. De composieten produceerden duidelijke "kill zones" tegen zowel Gram-positieve als Gram-negatieve stammen, waaronder Staphylococcus aureus en Escherichia coli. Het monster met de meeste Tenoxicam liet het sterkste algemene antibacteriële effect zien.
Wat dit kan betekenen voor toekomstige botreparatie
Samengevat suggereren de resultaten dat deze Tenoxicam-beladen bioglas–chitosaancomposieten drie taken tegelijk kunnen vervullen: ze hechten aan bot door het groeien van een natuurlijke minerale laag, ze bieden een langdurige lokale bron van pijn- en ontstekingsremming, en ze helpen gevaarlijke bacteriën rond de verwonding onderdrukken. Hoewel het werk in laboratoriumtesten en niet in patiënten is uitgevoerd, wijst het op toekomstige botimplantaten die niet slechts passieve ruimtehouders zijn, maar actieve partners in genezing — nieuw bot ondersteunen terwijl ze stilletjes medicijnen precies daar afleveren waar ze het meest nodig zijn.
Bronvermelding: El-khooly, M.S., Elkelish, A., Abdel-Aal, A.A. et al. Tenoxicam-loaded bioglass/chitosan composites for bone tissue engineering: in vitro characterization, sustained drug release, and antimicrobial activity. Sci Rep 16, 8258 (2026). https://doi.org/10.1038/s41598-026-42389-z
Trefwoorden: botweefselengineering, geneesmiddelafgevende scaffold, bioglas chitosaancomposiet, tenoxicam-afgifte, antibacterieel biomateriaal