Clear Sky Science · nl
Multicentrische clinicopathologische studie van het spectrum van odontogene myxoomlaesies met kwantitatieve pathologie
Waarom dit belangrijk is voor patiënten en tandartsen
Diep in het kaakbot kunnen zeldzame tumoren maanden of jaren ongemerkt groeien voordat ze worden ontdekt. Deze gezwellen, odontogene myxomen en myxofibromen genoemd, zijn geen kanker, maar ze kunnen uitbreiden, het bot verzwakken en de operatie bemoeilijken. Decennialang hebben pathologen ze grotendeels met het blote oog beoordeeld, wat heeft geleid tot verschillen in hoe ziekenhuizen hetzelfde type laesie beschrijven en classificeren. Deze studie brengt krachtige beeldanalysetools naar het microscooppreparaat en laat zien hoe kunstmatige intelligentie (AI) artsen kan helpen deze tumoren helderder en consistenter te zien.
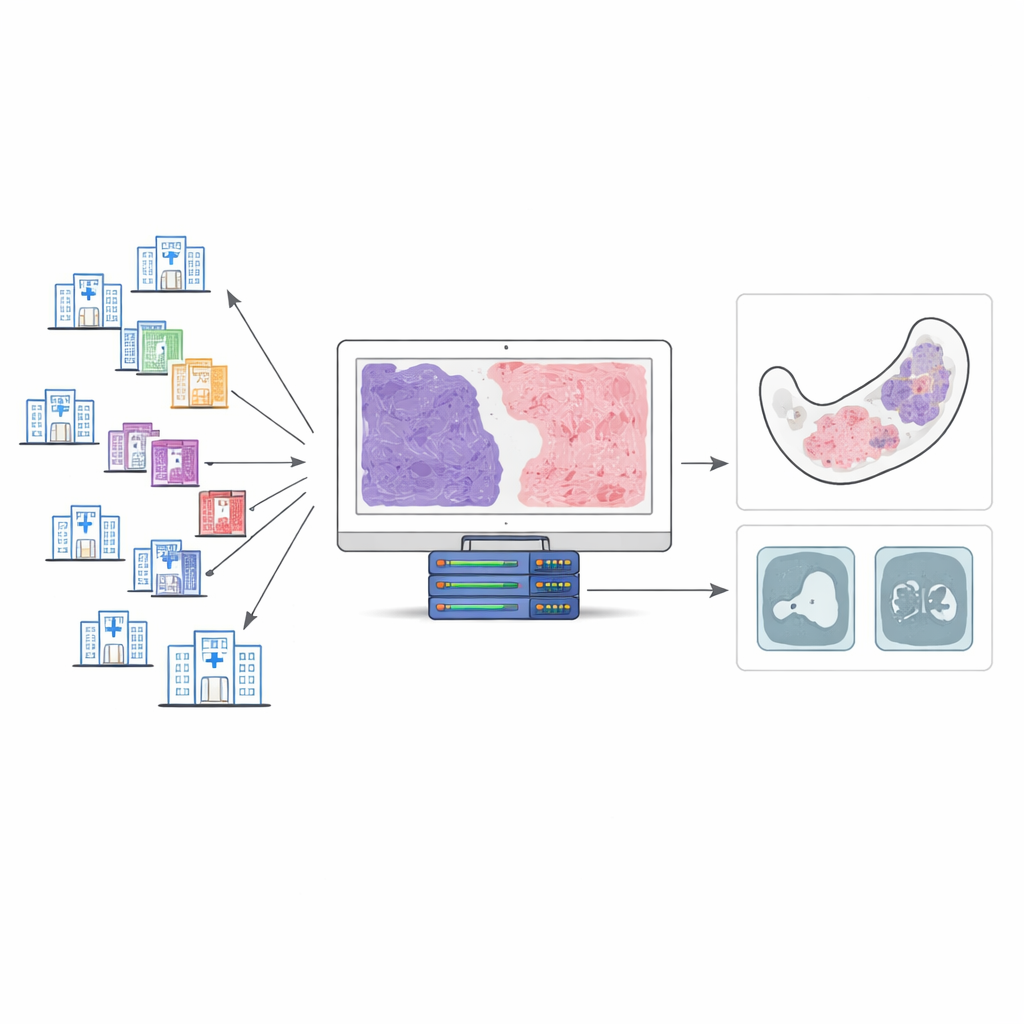
Zeldzame kaaktumoren die bedrieglijk op elkaar lijken
Odontogeen myxoom en odontogeen myxofibroom ontstaan uit weefsels die betrokken zijn bij de tandvorming. Beide zijn zachte, gelei‑achtige tumoren die in het kaakbot liggen. Onder de microscoop bevatten ze een mengeling van losse, myxoïde gebieden en dichtere vezelige banden. Traditioneel proberen pathologen ze te onderscheiden door in te schatten hoeveel van de tumor vezelig is versus myxoïde. Maar deze tumoren zijn zeldzaam en er bestaan geen algemeen aanvaarde regels voor hoeveel vezelig weefsel nodig is om de diagnose van het ene naar het andere label te verschuiven. Daardoor kunnen verschillende ziekenhuizen aan zeer vergelijkbare laesies verschillende namen geven, zelfs wanneer patiënten vergelijkbare klachten en scanbevindingen hebben.
Microscooppreparaten omzetten in cijfers
Het onderzoeksteam verzamelde 143 weefselmonsters van patiënten die in twintig jaar tijd in 34 ziekenhuizen werden behandeld, en concentreerde zich uiteindelijk op 100 gevallen die aan strikte kwaliteitscriteria voldeden. Alle monsters werden gekleurd met een speciale kleurstof (Masson’s trichroom) die vezelig weefsel anders kleurt dan het omringende tumorweefsel. Twee ervaren orale pathologen beoordeelden elk geval zorgvuldig en schatten het percentage vezelig weefsel in stappen van 10%. Deze expertschattingen dienden als referentie om een AI-systeem te trainen hetzelfde taakje automatisch en volledig kwantitatief uit te voeren.
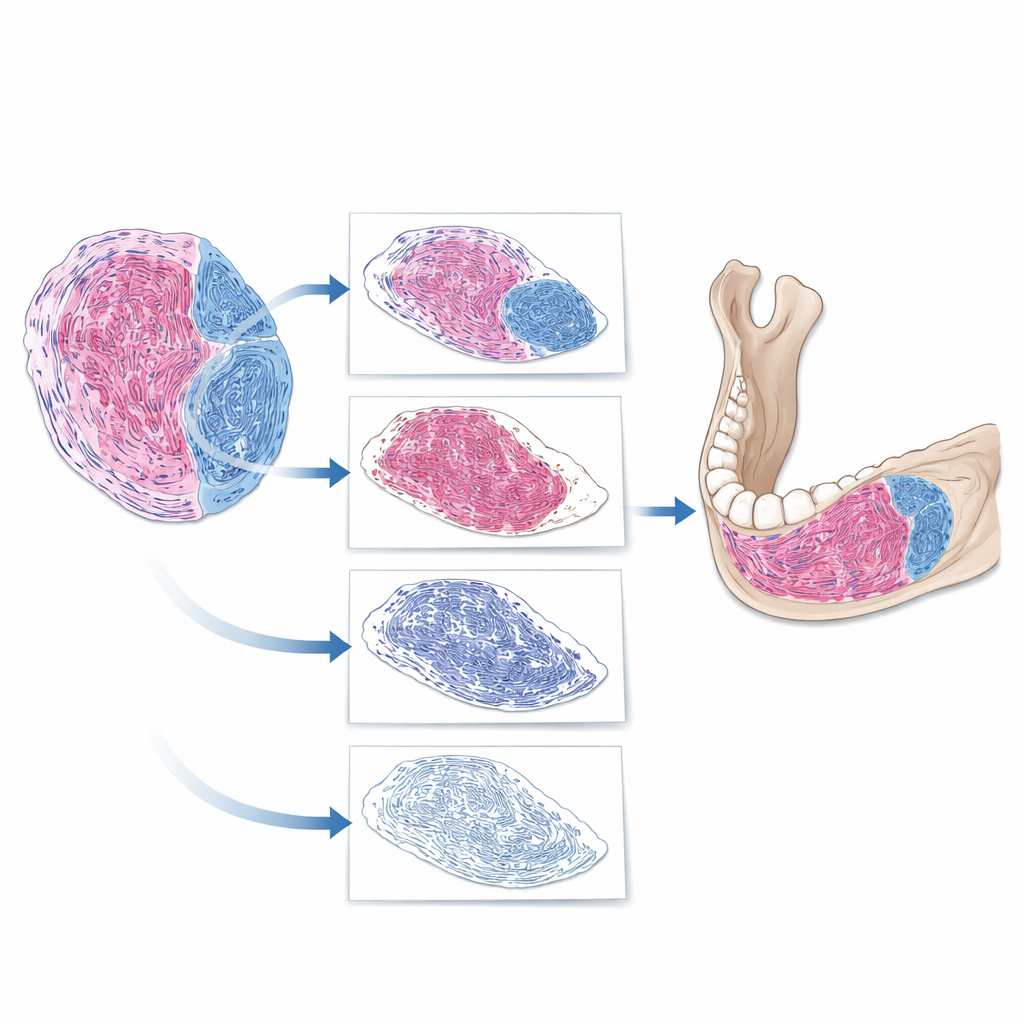
Hoe de AI een tumorpreparaat "leest"
Het team bouwde een stapsgewijze digitale pijplijn om hele‑slide beelden te analyseren. Eerst scheidde de software echt weefsel van lege achtergrond op het preparaat. Vervolgens isoleerde het de tumor van nabijgelegen structuren zoals bot en tanden. Ten slotte verwijderde het binnen de tumor celkernen en concentreerde het zich op het resterende materiaal, waarbij het regio’s identificeerde die de vezelige kleurstof hadden opgenomen. Hieruit berekende de AI een verhouding vezelig weefsel: het oppervlak van vezelig weefsel gedeeld door het totale tumoroppervlak. Toen de onderzoekers de door AI gegenereerde waarden vergeleken met hun eigen expertschattingen, was de overeenstemming sterk, met in de meeste individuele gevallen slechts ongeveer 10 procentpunt spreiding. Dit suggereert dat de AI betrouwbaar het oordeel van experts kan spiegelen, terwijl het datals precieze meting in plaats van ruwe indrukken uitdrukt.
Wat de vezelige samenstelling onthult over het uiterlijk van de tumor
Met deze metingen onderzochten de onderzoekers hoe vezelgehalte samenhing met klinische en radiologische kenmerken. Ze vonden dat de hoeveelheid vezelig weefsel sterk varieerde tussen instellingen, wat de verschillen weerspiegelt in hoe pathologen de tumoren oorspronkelijk hadden benoemd. Bij het bekijken van beeldvormingskenmerken viel één patroon op: tumoren die op scans als één holte verschenen (uniloculaire laesies) hadden doorgaans een hoger aandeel vezelig weefsel dan tumoren met meerdere kleine compartimenten (multiloculaire laesies). Dit past bij het idee dat meer vezelig, dicht weefsel eerder een meer solide, enkellaags massa kan vormen, terwijl losser, meer vloeistofrijk weefsel kan uiteenvallen in meerdere ruimtes.
Wat dit betekent voor toekomstige diagnostiek en zorg
De studie beoogt niet ziekten een nieuwe naam te geven of pathologen door machines te vervangen. In plaats daarvan toont ze aan dat op AI gebaseerde kwantitatieve pathologie een gedeelde meetlat kan bieden voor zeldzame kaaktumoren tussen vele ziekenhuizen. Door de subtiele texturen van tumorweefsel om te zetten in reproduceerbare cijfers, maakt deze benadering zichtbaar hoeveel alledaagse diagnoses afhangen van subjectief oordeel en biedt ze een manier om die variabiliteit te verminderen. Voor patiënten kan meer consistente interpretatie van deze laesies zorgen voor helderder behandelbesluitvorming en betere vergelijking van uitkomsten tussen centra. Naarmate vergelijkbare methoden worden uitgebreid naar andere zeldzame tumoren, kan AI‑geassisteerde microscopie stilletjes herdefiniëren hoe pathologen ziekte zien—hun beoordelingen meer vergelijkbaar en uiteindelijk nuttiger makend, ongeacht waar een patiënt wordt behandeld.
Bronvermelding: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Trefwoorden: odontogeen myxoom, kaaktumoren, digitale pathologie, kunstmatige intelligentie, verhouding vezelig weefsel