Clear Sky Science · nl
Genetische analyse van belangrijke spelers in de PI3K-signaalcascade van colorectaal carcinoom
Waarom uw genen er toe doen voor colongezondheid
Colorectale kanker is een van de meest voorkomende en dodelijke kankers wereldwijd, en het aantal gevallen neemt toe in veel landen die een snelle levensstijlverandering doormaken. Toch loopt niet iedereen met vergelijkbare dieet- of leefgewoonten hetzelfde risico. Deze studie stelt een eenvoudige maar krachtige vraag: helpen erfelijke verschillen in belangrijke groeiregulerende genen verklaren wie colorectale kanker ontwikkelt, hoe agressief die is en hoe goed standaardmedicijnen werken — met name in een grote groep patiënten uit Pakistan, een populatie die tot nu toe onderbelicht is?
Een drukke regelroute binnen onze cellen
Cellen in het darmkanaal ontvangen voortdurend signalen die aangeven wanneer ze moeten groeien, delen of zelfvernietigen. Een van de drukst gebruikte communicatiepaden is de PI3K–AKT–mTOR-route — een cascade van moleculaire schakelaars die celgroei, overleving, vaatvorming en weerstand tegen celdood bevordert. Wanneer deze route overactief is, kunnen cellen ongecontroleerd gaan vermenigvuldigen en tumoren vormen. De genen PIK3CA, AKT1 en mTOR bevinden zich op cruciale controlepunten langs dit pad. Subtiele erfelijke veranderingen in deze genen, zogenaamde single nucleotide polymorfismen (SNP’s), en sterkere veranderingen bekend als “hotspot”-mutaties kunnen het evenwicht naar kanker kantelen of beïnvloeden hoe tumoren reageren op behandeling.
DNA-scans bij patiënten en gezonde vrijwilligers
Om dit te onderzoeken voerden de onderzoekers een case–control-studie uit met 495 personen met colorectale kanker en 495 kankervrije vrijwilligers, afgestemd op leeftijd en geslacht. Bloedmonsters leverden DNA op, dat werd onderzocht op zeven SNP’s verspreid over PIK3CA, AKT1 en mTOR, samen met twee veelbekende hotspot-mutaties, E542K (in PIK3CA) en E17K (in AKT1). Met gerichte PCR-methoden en DNA-sequencing vergeleek het team hoe vaak elk genetisch variant voorkwam bij patiënten versus controles en koppelde deze patronen aan klinische kenmerken zoals leeftijd, familiegeschiedenis, darmziekte, tumorklasse en de medicatieregimes die patiënten kregen. 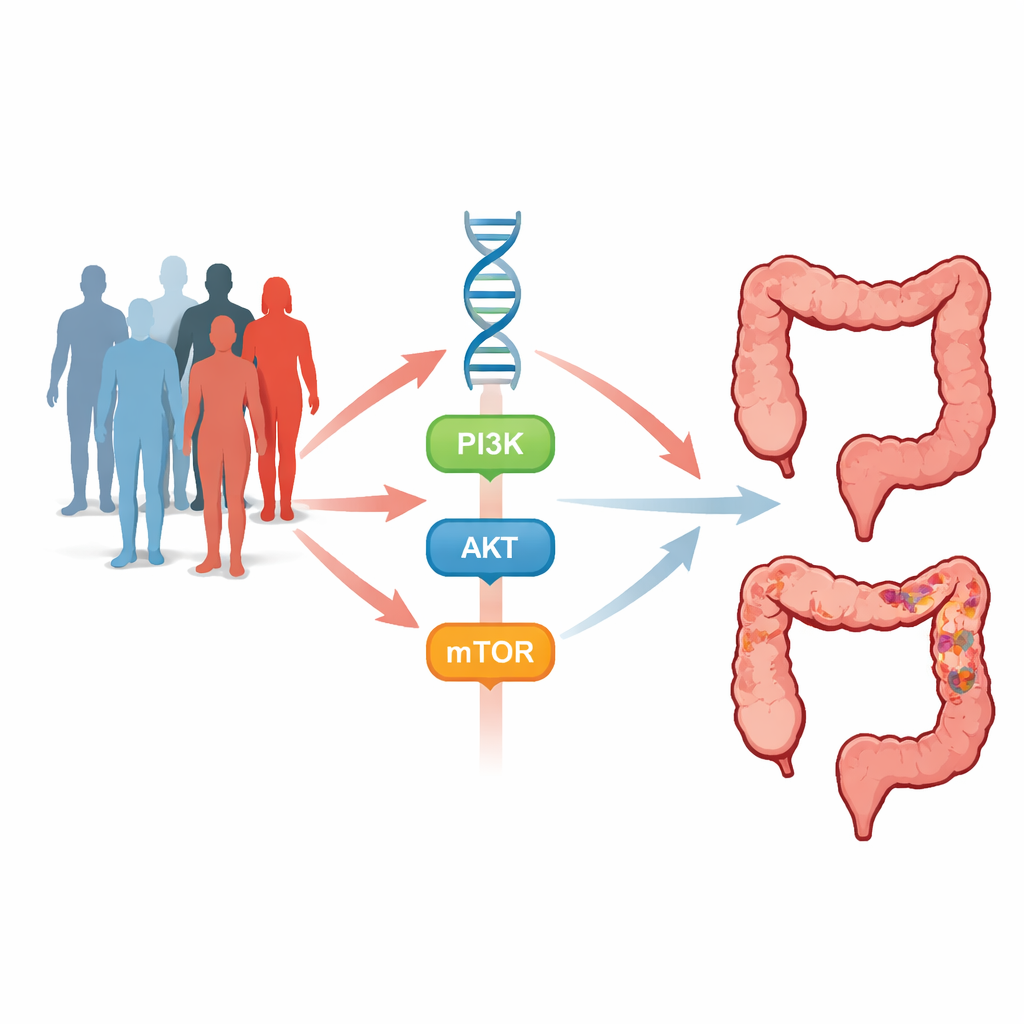
Riskante varianten en krachtige mutaties
De analyse toonde aan dat de meeste geteste varianten veel vaker voorkwamen bij mensen met colorectale kanker dan bij gezonde controles, wat sterk suggereert dat ze bijdragen aan het ziektesrisico. Verschillende AKT1- en mTOR-varianten vertoonden in het bijzonder opvallend hogere frequenties bij patiënten, terwijl bepaalde “normale” versies van deze genen vaker bij controles werden gevonden, wat duidt op een mogelijke beschermende rol. De hotspot-mutaties vertelden een nog duidelijker verhaal: de E542K-verandering in PIK3CA kwam voor bij ongeveer 15% van de patiënten, en de E17K-verandering in AKT1 bij ongeveer 29%, beide veel vaker dan bij de controles. Computergebaseerde modellering wees uit dat deze mutaties de algemene eiwitvorm niet dramatisch vervormen, maar eerder de route in een meer 'aan'-toestand lijken te vergrendelen, waardoor continue groeisignalen ontstaan die tumorgroei bevorderen.
Van genen naar behandeling en overleving
Genetica opereert niet los van andere factoren, dus de onderzoekers onderzochten hoe deze varianten interacteren met reële risicofactoren en therapieën. Veel van de SNP’s werden in verband gebracht met roken, inflammatoire darmziekte, familiegeschiedenis, kankertype en -stadium, en of patiënten chemotherapie of bestraling hadden gekregen. Bij follow-up van patiënten over tijd vonden ze dat bepaalde genversies gekoppeld waren aan betere of slechtere totale overleving. Zo leefden mensen met de normale versies van meerdere AKT1- en mTOR-varianten over het algemeen langer dan degenen met de hoog-risico versies. De studie vergeleek ook de overleving tussen patiënten die gangbare combinaties van geneesmiddelen ontvingen. Capecitabine, een veelgebruikt chemotherapietablet, werd geassocieerd met de beste overlevingsschattingen, en verschillende varianten in het pathway leken te beïnvloeden hoe goed verschillende regimes werkten, wat suggereert dat erfelijke genetica kan helpen bij meer gepersonaliseerde behandelkeuzes. 
Hoe veranderingen samen meekomen
Buiten individuele varianten onderzochten de auteurs hoe groepen veranderingen de neiging hebben samen te worden geërfd — een patroon dat bekend staat als linkage disequilibrium. Ze ontdekten een blok van aangrenzende varianten dat PIK3CA en AKT1 overspant en dat vaker samen voorkwam bij patiënten dan bij controles. Dit suggereert dat combinaties van kleine DNA-verschillen langs het PI3K-pad gezamenlijk iemands basale risico en tumorgedrag kunnen beïnvloeden, in plaats van dat één enkele verandering alles verklaart.
Wat dit betekent voor patiënten en precisiegeneeskunde
Voor een niet‑specialistische lezer is de conclusie dat dit werk de gedachte versterkt dat 'one size fits all' een slecht model is voor de zorg bij colorectale kanker. In deze Pakistaanse cohorte correleerden specifieke erfelijke varianten en hotspot-mutaties in groeiregulerende genen duidelijk met kankerrisico, tumorkenmerken en overleving, en ze leken zelfs te moduleren hoe patiënten reageerden op standaardchemotherapie. Hoewel deze bevindingen bevestigd moeten worden in grotere en meer diverse groepen, wijzen ze op een toekomst waarin een eenvoudige bloedtest voor PI3K–AKT–mTOR-varianten kan helpen degenen met een hoger risico te identificeren, aangeven welke patiënten mogelijk baat hebben bij bepaalde geneesmiddelen, en anderen besparen van ineffectieve of onnodig toxische behandelingen.
Bronvermelding: Pervaiz, H., Masood, N., Malik, P.A. et al. Genetic analysis of key players in PI3K signaling cascade of colorectal carcinoma. Sci Rep 16, 11317 (2026). https://doi.org/10.1038/s41598-026-42006-z
Trefwoorden: genetica van colorectaal kanker, PI3K AKT mTOR-pathway, single nucleotide polymorfismen, precisie-oncologie, chemotherapie-respons