Clear Sky Science · nl
Visualisatie van kwaadaardige progressie: in situ CD109-gebaseerde ruimtelijke immunofluorescentie-assay geeft transformatie van papillair naar anaplastisch schildkliercarcinoom binnen het tumormicro-omgeving weer
Waarom deze studie over schildklierkanker belangrijk is
Anaplastisch schildkliercarcinoom is een van de dodelijkste menselijke kankers en kan een normaal gesproken goed behandelbare schildkliertumor veranderen in een snel fataal ziektebeeld. Artsen begrijpen echter nog niet volledig hoe een veelvoorkomend, langzaam groeiend papillair schildkliercarcinoom plotseling kan overgaan in deze agressieve vorm. Deze studie volgt die transformatie direct binnen de tumor van een patiënt, met een nieuwe beeldvormingstechniek waarmee te zien is hoe kankercellen en hun directe omgeving stap voor stap verschuiven. Het werk biedt een gedetailleerder beeld van hoe de lokale tumoromgeving cellen richting een dodelijker staat kan duwen en suggereert nieuwe mogelijkheden om deze overgang te vertragen of te voorkomen.
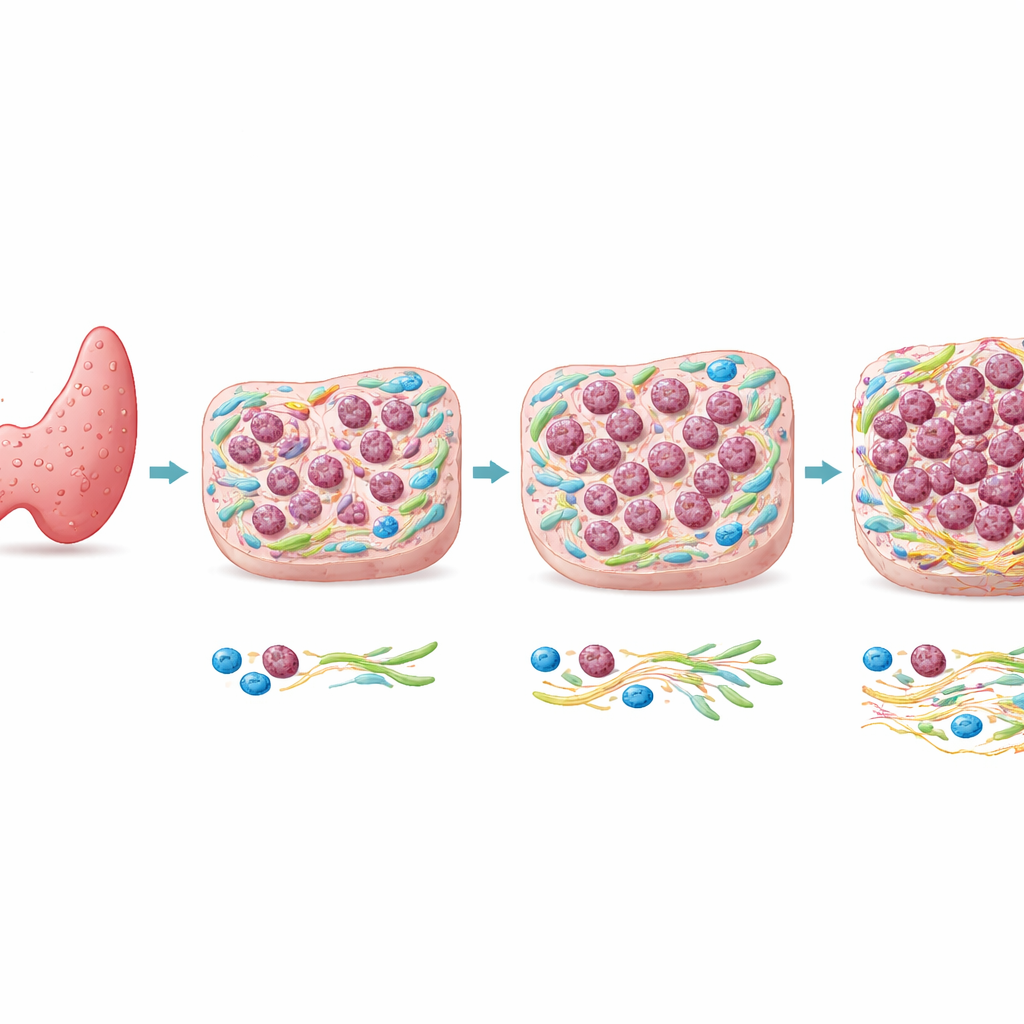
Van een veelvoorkomende tumor naar een zeldzame doder
De meeste schildklierkankers zijn papillair schildkliercarcinoom (PTC), die over het algemeen langzaam groeien en goede prognoses hebben. Anaplastisch schildkliercarcinoom (ATC) daarentegen is zeldzaam maar vaak dodelijk binnen enkele maanden. Genetische studies hebben aangetoond dat ATC en nabijgelegen PTC in dezelfde patiënt vaak veel van dezelfde DNA-mutaties delen, inclusief veranderingen in bekende kankergenen. Die gelijkenis suggereert dat genen alleen mogelijk niet verklaren waarom slechts sommige delen van een tumor anaplastisch worden. De auteurs richtten zich daarom op wat er gebeurt in het weefsellandschap rondom de cellen — de tumormicro-omgeving — om te zien of lokale omstandigheden deze gevaarlijke verschuiving bevorderen.
Een nieuwe manier om kanker in situ in kaart te brengen
Het team ontwikkelde een ruimtelijke immunofluorescentie (SPI)-assay, een vorm van multikleurmicroscopie die de helderheid van specifieke eiwitten meet in honderden kleine, afgebakende vakjes over een weefselsectie. Ze baseerden deze methode op CD109, een membraaneiwit dat zij identificeerden als een merker van kwaadaardig gedrag in schildklierweefsel, en CK8/18, een eiwit kenmerkend voor gewone papillair tumorcellen. Door de verhouding van CD109 tot CK8/18 in vele kleine regio’s te berekenen, maakten ze kleurenkaarten die duidelijke PTC-gebieden scheidden van duidelijke ATC-gebieden en, cruciaal, tussenzones onthulden waar beide merkers overlappen. In plaats van een scherpe grens bleek de overgang van papillair naar anaplastisch kanker een geleidelijke, vlekkerige continuüm te zijn.
Vijf zones langs een pad van verandering
Om dit continuüm beter te begrijpen, verdeelden de onderzoekers het weefsel in vijf regio’s, van puur PTC tot volledig ontwikkeld ATC. Vervolgens onderzochten ze tal van aanvullende eiwitten die informatie geven over celidentiteit, groei, beweging en het ondersteunende weefsel. Over deze regio’s heen namen klassieke epitheliale kenmerken zoals E-cadherine en CK8/18 gestaag af, terwijl merkers geassocieerd met celmotiliteit en vormverandering, zoals vimentine, toenamen. Eiwitten die snelle celdeling aangeven, stegen in de meer anaplastische zones. Tegelijkertijd werden de omliggende steunende cellen — kankergeassocieerde fibroblasten — en immuuncellen, in het bijzonder bepaalde macrofagen, talrijker en meer geactiveerd, en namen de door hen geproduceerde eiwitten toe.
Wanneer het tumorraamwerk vijandig wordt
Er deed zich een opvallende verandering voor in het skelet van de tumor, de extracellulaire matrix. In de anaplastische regio’s deponeerden fibroblasten-achtige cellen meer collageenvormen III en VI en een matrixeiwit genaamd TGFBI, en deze vezels waren dikker, verwarder en georiënteerd in meerdere richtingen in plaats van in nette, parallelle lijnen. Dit herschikte netwerk maakt het weefsel waarschijnlijk mechanisch stijver. In deze stijvere zones was een drukgevoelig signaalmolecuul, YAP, actiever in zowel kankercellen als steunende cellen. Dezelfde gebieden toonden meer tekenen van DNA-schade en een vorm van inflammatoire celdood, samen met vrijlating van S100-eiwitten die als alarmsignalen kunnen fungeren en de omgeving verder ontsteken. De auteurs stellen dat deze combinatie van compressie, celdood en chronische ontsteking de overleving en verspreiding bevordert van reeds gemuteerde kankercellen die stress kunnen doorstaan en een epitheliaal–mesenchyme-achtige transitie ondergaan.
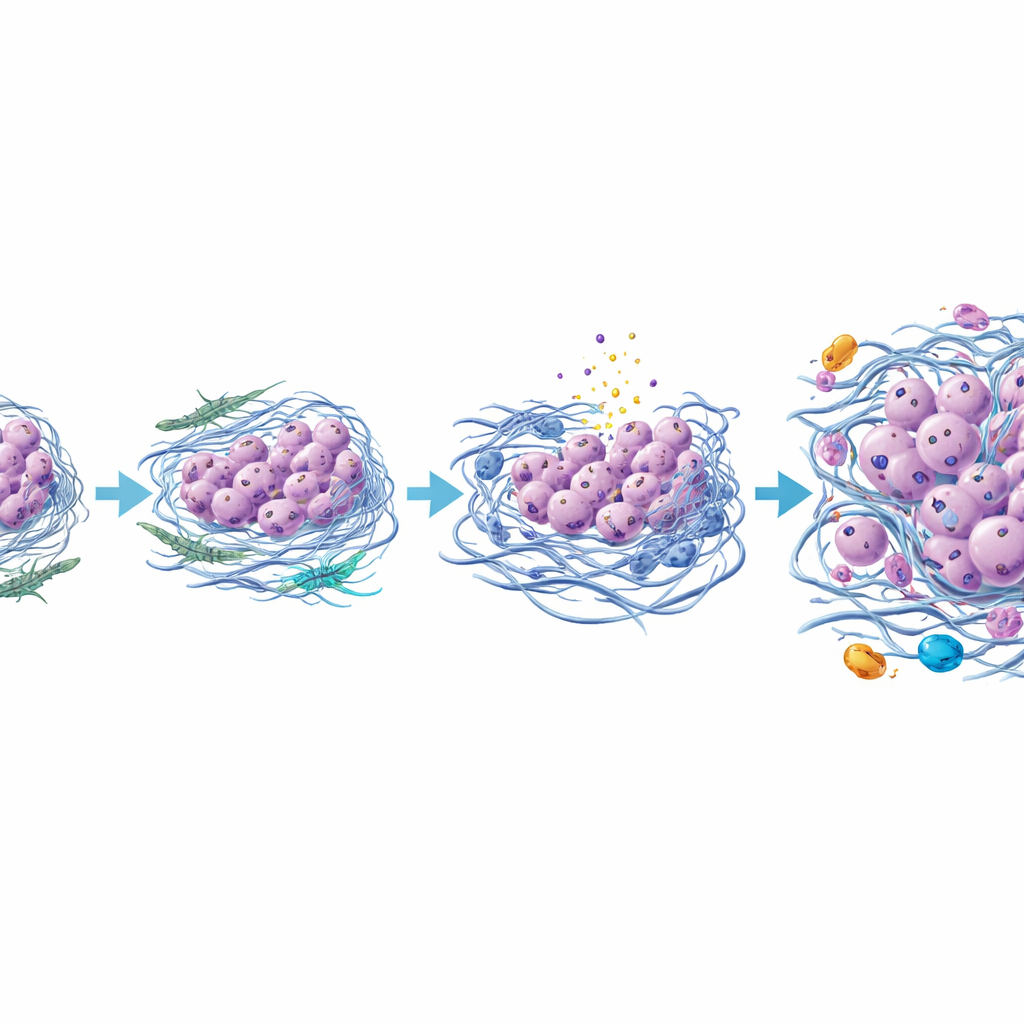
Een nieuw beeld van hoe een schildkliertumor dodelijk wordt
Samengebracht suggereren de bevindingen dat anaplastische schildklierkanker niet alleen ontstaat door extra genmutaties, maar door een hervormde directe omgeving rond de tumor. Terwijl papillair tumorcellen en nabijgelegen steuncellen interageren, evolueren sommige fibroblasten naar een agressiever type dat de omringende matrix verdikt en verhardt, kwetsbare cellen samendrukt tot de dood en ontstekingsbevorderende immuuncellen aantrekt. De overlevende, veerkrachtigere kankercellen verliezen geleidelijk hun oorspronkelijke schildklierkenmerken en nemen een meer mobiel, invasief profiel aan, en vormen uiteindelijk een anaplastische tumor. Hoewel dit werk is gebaseerd op één goed bestudeerd geval en bevestiging in meer patiënten nodig heeft, introduceert het een krachtige beeldvormingstool en een gedetailleerd model waarin het richten op de steunende cellen van de tumor, de matrix of ontstekingssignalen kan helpen om een van de meest gevreesde transformaties bij schildklierkanker te voorkomen of uit te stellen.
Bronvermelding: Cohen, T., Suzuki, K., Matsuda, K. et al. Visualizing malignant progression: in situ CD109-based spatial immunofluorescence assay delineates papillary to anaplastic thyroid carcinoma transformation within the tumor microenvironment. Sci Rep 16, 8682 (2026). https://doi.org/10.1038/s41598-026-41927-z
Trefwoorden: anaplastisch schildkliercarcinoom, papillair schildkliercarcinoom, tumormicro-omgeving, stijfheid van de extracellulaire matrix, ruimtelijke immunofluorescentie