Clear Sky Science · nl
Analyse van extracellulaire vesikels afkomstig van bronchiale epitheelcellen met conventionele, beeldvormende en nanoschaal flowcytometrie-technologieën
Waarom kleine belletjes in de longen ertoe doen
Onze longen zijn bekleed met cellen die voortdurend met het immuunsysteem communiceren, zeker wanneer we stof, vervuiling of ziekteverwekkers inademen. Een groot deel van deze “conversatie” verloopt via microscopische belletjes die extracellulaire vesikels worden genoemd — pakketjes van vetten en eiwitten die door cellen worden vrijgegeven. Deze vesikels kunnen longziekten verergeren of juist verzachten en kunnen in de toekomst dienen als vroege waarschuwingssignalen voor aandoeningen zoals astma, chronische obstructieve longziekte (COPD) en fibrose. Deze studie onderzoekt hoe je deze lastige deeltjes het beste kunt meten met verschillende typen geavanceerde laser-gebaseerde instrumenten, met het oog op praktische toepassing in onderzoek en toekomstige klinische tests.
Onzichtbare boodschappen van luchtwegcellen
Extracellulaire vesikels (EVs) zijn kleine, door een membraan omsloten pakketjes die vrijwel alle cellen uitscheiden in vloeistoffen zoals bloed, urine en de dunne laag vloeistof die onze luchtwegen bekleedt. EVs afkomstig van humane bronchiale epitheelcellen — de cellen die de ademhalingsbuizen bekleden — zijn al gekoppeld aan meerdere longprocessen: ze kunnen beïnvloeden hoe allergieën ontstaan, helpen bij het bestrijden van longinfecties, de structuur van de luchtwegen vormen bij COPD en zelfs littekenvorming in longweefsel beperken. Omdat ze stukjes eiwit, vet en genetisch materiaal van hun moedercel bevatten, kunnen EVs fungeren als vingerafdrukken van longgezondheid of -ziekte en mogelijk uiteindelijk zelf als therapie worden gebruikt. De uitdaging is dat ze extreem klein, sterk heterogeen en in lage concentraties aanwezig zijn, wat het lastig maakt ze nauwkeurig te detecteren en te tellen.
Voorbij trage en gefragmenteerde tests
Traditioneel vertrouwen wetenschappers op verschillende afzonderlijke methoden om EVs te bestuderen. Ultracentrifugatie of grootte-exclusiechromatografie worden gebruikt om ze te isoleren; nanopartikel-trackinganalyse meet hoe ze bewegen om grootte en aantal te schatten; en elektronenmicroscopen leveren gedetailleerde beelden. Hoewel krachtig, zijn deze benaderingen traag, arbeidsintensief en niet ideaal voor routinematig of klinisch gebruik. Cruciaal is dat ze weinig informatie geven over welke specifieke eiwitten elk vesikel draagt. Flowcytometrie — een technologie die veel wordt gebruikt om bloed- en immuuncellen te analyseren — biedt een gestroomlijnde alternatieve aanpak. Deeltjes worden één voor één langs lasers geleid, waarbij hun lichtverstrooiing (gerelateerd aan grootte) en fluorescentie (van kleurstoffen of antilichamen) worden gemeten. Recente instrumentontwerpen beloven flowcytometrie tot op het niveau van de kleinste vesikels te brengen, waardoor de mogelijkheid ontstaat dat één machine grootte, aantal en karakterisering van EVs in één run kan uitvoeren.
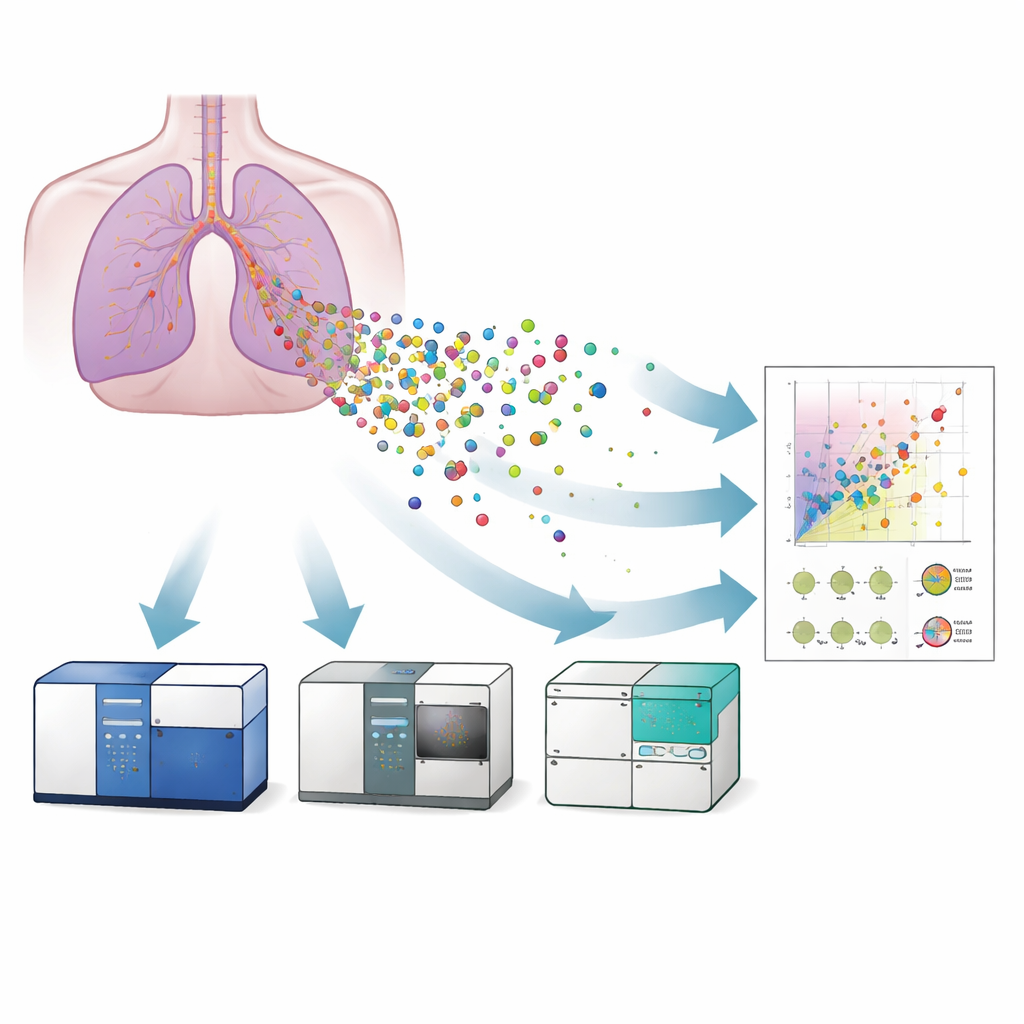
Drie machines, één doel
De onderzoekers vergeleken drie varianten van flowcytometrie voor het bestuderen van EVs die vrijkomen uit een in het laboratorium gekweekt model van menselijk bronchiaal epitheel: een conventionele flowcytometer, een beeldvormende flowcytometer en een nanoschaal flowcytometer. Eerst bevestigden ze de aanwezigheid en het typische uiterlijk van vesikels met elektronenmicroscopie en superresolutiemicroscopie, die ook lieten zien dat de vesikels oppervlakteeiwitten droegen die tetraspaninen worden genoemd (CD9, CD63, CD81) — standaardmarkers voor EVs. Vervolgens gebruikten ze zorgvuldig gekalibreerde referentiedeeltjes en liposoomstandaarden om de lichtsignalen van elk instrument om te zetten naar geschatte vesikelgroottes. De nanoschaal flowcytometer kon vesikels detecteren tot ongeveer 40 nanometer, het beeldvormende instrument tot ongeveer 55 nanometer, terwijl de conventionele machine moeite had onder ruwweg 120 nanometer. Dit betekende dat alleen de gevoeliger systemen de allerkleinste, en mogelijk medisch meest relevante, vesikels volledig konden vastleggen.
De vesikels labelen en tellen
Om zeker te zijn dat ze intacte, biologisch actieve vesikels maten en geen fracties of afvaldeeltjes, gebruikte het team een kleurstof genaamd calcein-AM. Deze kleurstof licht alleen op zodra hij een intact membraan is gepasseerd en door enzymen binnenin het vesikel wordt verwerkt. Ze stemden de kleurstofconcentratie zorgvuldig af zodat vesikels sterk werden gemarkeerd terwijl de achtergrondsignalen werden geminimaliseerd, en kozen een concentratie die duidelijke, lineaire reacties over verdunningen van monsters gaf. Calcein werd daarna gecombineerd met fluorescerende antilichamen die zich binden aan tetraspaninen op het vesikeloppervlak, waardoor de instrumenten vesikels met verschillende combinaties van deze markers konden scheiden. De groep mat ook hoe gevoelig elk apparaat was voor deze fluorescerende markers — hoeveel antilichaammoleculen aanwezig moesten zijn op een vesikel voordat het betrouwbaar kon worden gedetecteerd. Beeldvormende flowcytometrie bood over het algemeen lagere detectiedrempels dan de conventionele cytometer, waardoor het beter geschikt is voor deeltjes met slechts een klein aantal markereiwitten.
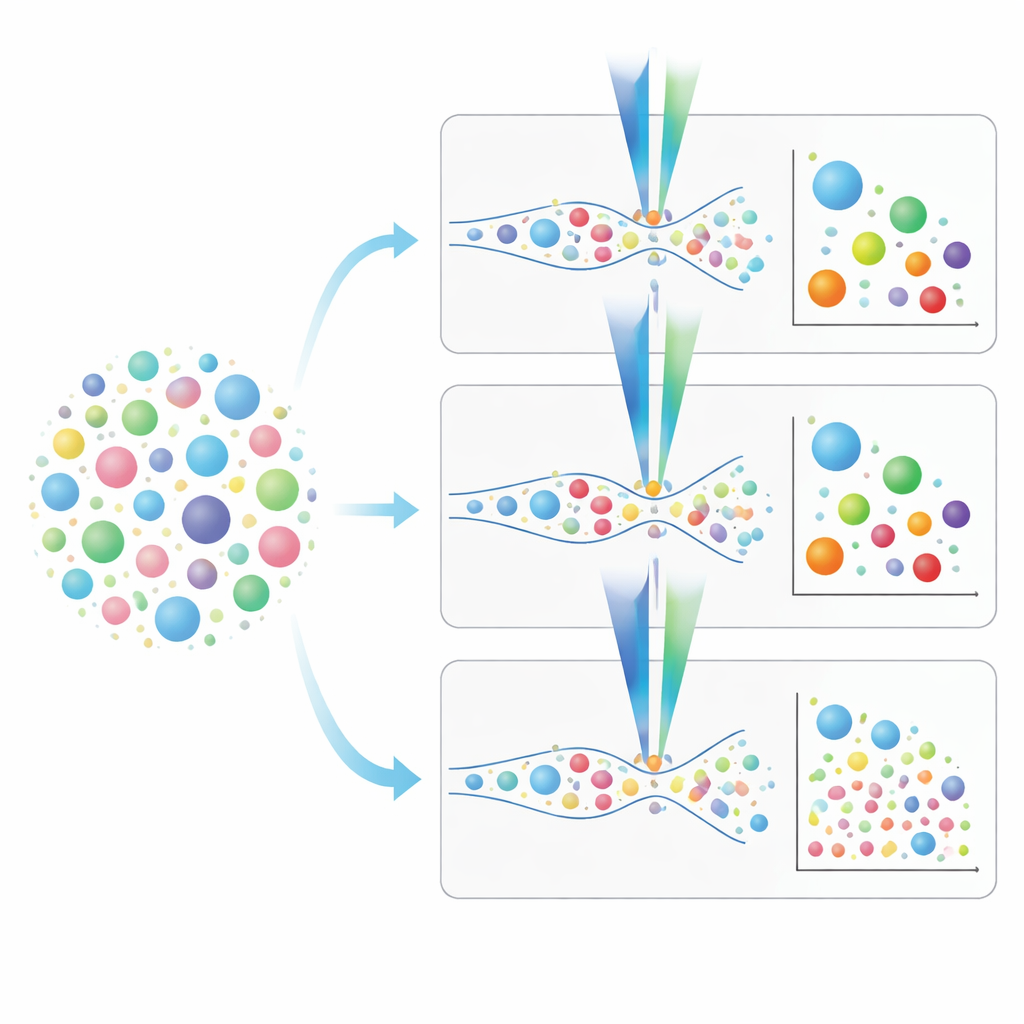
De juiste tool kiezen voor onderzoek naar longvesikels
Uit deze vergelijking blijkt een praktisch beeld. Conventionele flowcytometers zijn sneller en kunnen monsters analyseren zonder voorafgaande isolatie, maar missen veel van de kleinste vesikels die mogelijk cruciale ziektesignalen dragen. Beeldvormende en nanoschaal flowcytometers, hoewel langzamer en in het geval van het nano-instrument meer afhankelijk van voorafgaande monsteropzuivering, kunnen tot veel kleinere groottes kijken en ondersteunen rijkere “vingerafdrukken” van vesikeloppervlakte-eiwitten. De auteurs beschrijven stapsgewijze kleuring- en kalibratiestrategieën, benadrukken het belang van het kennen van de detectiegrens van elke fluorescerende marker en tonen hoe misleidende signalen van kleurstoffen die ook fragmenten of niet-vesikeldeeltjes labelen vermeden kunnen worden. In eenvoudige bewoordingen bieden ze een routekaart voor onderzoekers om te beslissen welk instrument en protocol het beste passen bij hun vragen over long-EVs, en helpen zij het veld dichter bij het gebruik van deze microscopische boodschappers als praktische hulpmiddelen voor het begrijpen, diagnosticeren en uiteindelijk behandelen van luchtwegaandoeningen.
Bronvermelding: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Trefwoorden: extracellulaire vesikels, longepitheel, flowcytometrie, aandoening van de luchtwegen, biomarkeranalyse