Clear Sky Science · nl
Kwantiatieve ex vivo beoordeling van doeldtemperatuur en ablatieduur voor protocoloptimalisatie van microgolfablaties met MRI‑thermometrie
Tumorbehandelingen in realtime volgen
Wanneer artsen levertumoren wegbranden met warmte, willen ze precies zien welke delen van het orgaan tijdens de ingreep worden vernietigd. Magnetische resonantie‑beeldvorming (MRI) biedt een manier om als het ware de temperatuur in het lichaam te “zien” terwijl de warmte zich verspreidt. Deze studie onderzoekt hoe heet, en hoe lang, artsen veilig leverweefsel kunnen verwarmen tijdens microgolfablatie zonder betrouwbare temperatuurkaarten van MRI te verliezen — een belangrijke stap naar preciezere, minder invasieve kankerbehandelingen.
Waarom warmtebehandelingen van de lever betere observatie vereisen
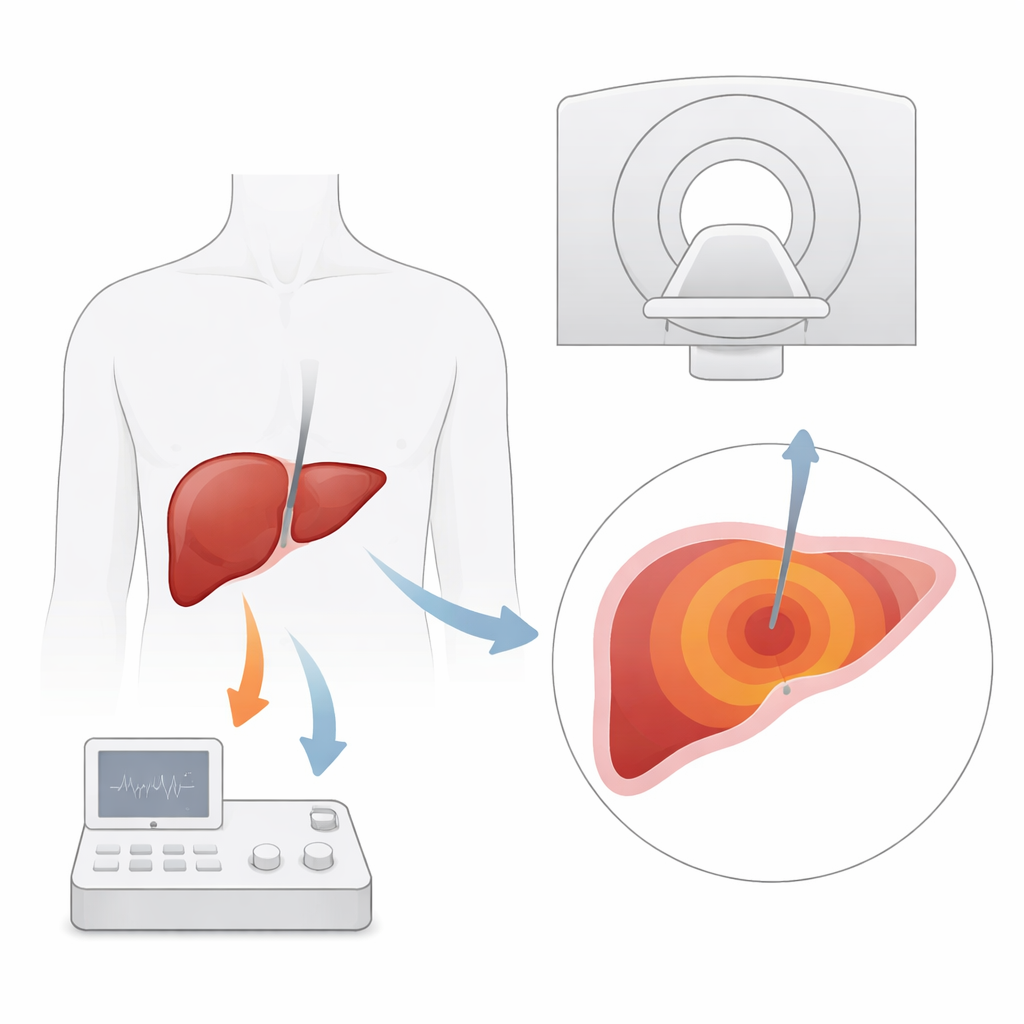
Microgolfablatie gebruikt een dunne naald om energie af te geven die tumorweefsel in de lever verhit en vernietigt. Het is vooral belangrijk voor patiënten met leverkanker of metastasen die geen operatie kunnen ondergaan. Traditionele beeldvorming, zoals echografie en CT, helpt bij het bepalen waar de naald geplaatst moet worden, maar toont kleine tumoren vaak niet duidelijk en is beperkt in het volgen van hoe ver de warmte tijdens de behandeling is verspreid. MRI valt op omdat het niet alleen zachte weefsels zeer gedetailleerd kan tonen, maar ook temperatuurveranderingen kan meten via een eigenschap van watermoleculen. In theorie stelt dit artsen in staat om een warmtekaart van de lever in realtime te volgen en te verzekeren dat de hele tumor, plus een veilige marge, wordt vernietigd.
Wanneer te veel warmte het zicht belemmert
In de praktijk kunnen MRI‑temperatuurkaarten onbetrouwbaar worden wanneer weefsel erg heet wordt. Bij hoge temperaturen kookt het water in het weefsel en ontstaan kleine gasbelletjes die het magneetveld verstoren. Die verstoringen verschijnen als foutieve temperatuurwaarden en vreemde vormen op de kaart, waardoor het moeilijk is te bepalen waar de werkelijke ablatiezone ophoudt. De onderzoekers vermoedden dat het hanteren van iets lagere doeldtemperaturen schonere, betrouwbaardere MRI‑kaarten zou opleveren, ook al zouden de behandelde gebieden dan kleiner zijn. Hun doel was combinaties van doeldtemperatuur en verwarmingsduur te vinden die beeldhelderheid en voldoende weefselvernietiging het beste in balans brengen.
Warmteinstellingen testen in donordierenlevers
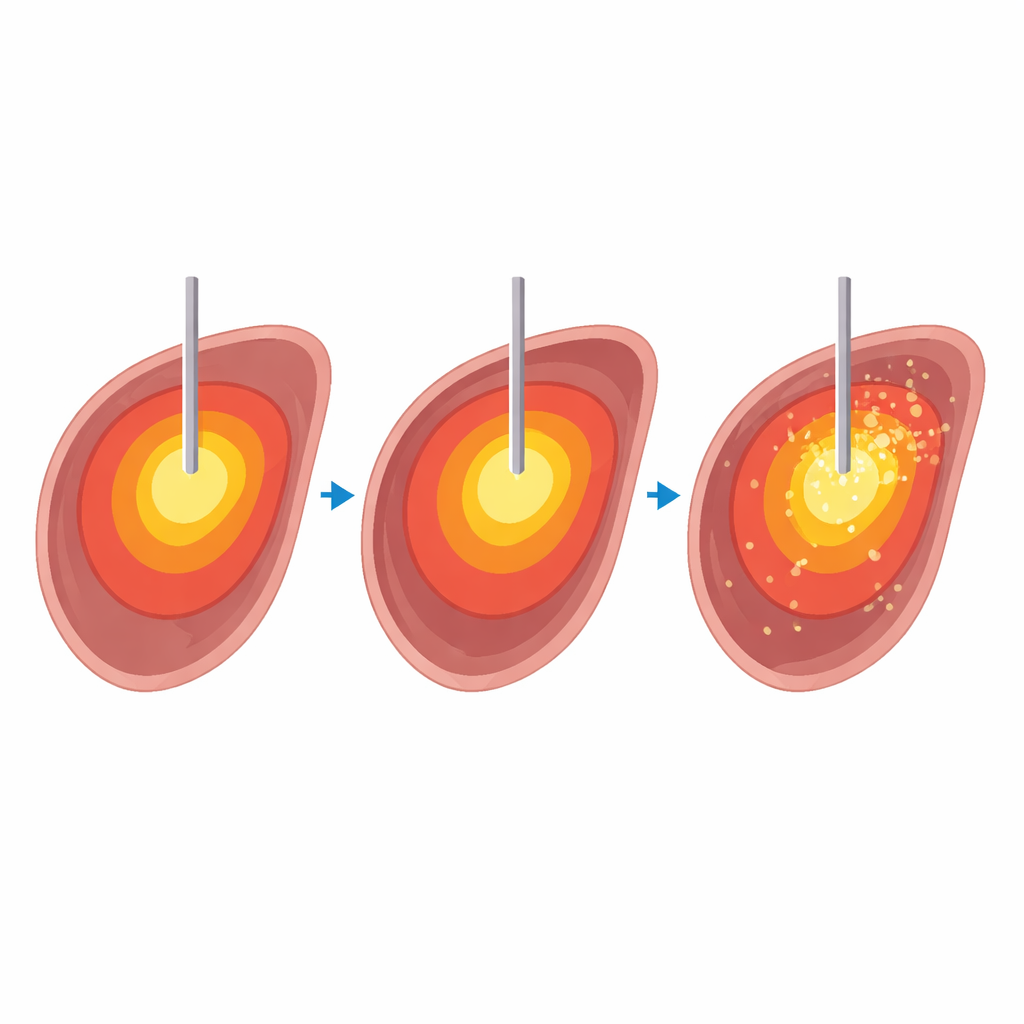
Om dit veilig en nauwkeurig te onderzoeken voerde het team 32 microgolfablaties uit in tien rundslevers die kort na slacht waren verwijderd. In een 1,5‑tesla MRI‑scanner verwarmden ze leverweefsel tot vier doeldtemperaturen — 60, 80, 100 en 120 graden Celsius — voor vier verschillende tijdsintervallen tussen 5 en 15 minuten. Tijdens elke ablatie produceerde een snelle MRI‑sequentie elke paar seconden driedimensionale temperatuur‑ en “thermische dosis”‑kaarten. Na verwarming werden de levers langs het naaldspoor in plakjes gesneden en werden de zichtbare dode weefselgebieden gemeten en vergeleken met de door MRI voorspelde gebieden. Twee radiologen beoordeelden de kwaliteit van de MRI‑kaarten op een vijfpuntschaal, waarbij zij rekening hielden met hoe rond en regelmatig de verwarmde zone leek en hoe sterk artefacten door gas en de naald stoorden.
Koelere verbrandingen, duidelijkere kaarten
De experimenten toonden een duidelijke afweging aan. Hogere temperaturen gaven grotere dode weefselzones, zoals te verwachten viel, maar de MRI‑temperatuurkaarten verslechterden sterk boven 100 graden. Bij deze hogere instellingen werden de ablaties vormen onregelmatiger en veroorzaakten gasgerelateerde verstoringen ogenschijnlijk dalende of zelfs negatieve temperatuurwaarden nabij de naald. Daarentegen waren de MRI‑kaarten bij 60 en 80 graden vloeiender, ronder en veel beter afgestemd op de werkelijke laesiegroottes die in de weefselplakjes werden gezien. Statistische analyses bevestigden sterke overeenstemming tussen MRI‑afgeleide gebieden en echte necrose bij lagere temperaturen, met verzwakkende of wegvallende correlaties bij hogere temperaturen. Het verlengen van de verwarmingsduur compenseerde gedeeltelijk voor lagere temperaturen qua totale schade, maar kon niet volledig de grootste laesies evenaren die bij 120 graden werden gezien.
Een tweefasige strategie voor veiligere, slimmere ablatie
Op basis van deze bevindingen stellen de auteurs een praktisch compromis voor toekomstige MRI‑geleidingbehandelingen voor. Een eerste verwarmingsfase rond 80 graden Celsius gedurende 15 minuten bood een goede balans: de beeldkwaliteit was hoog, de ablatiezone redelijk groot en weefselonderzoeken toonden effectieve celdood. Voor gevallen die nog grotere behandelzones vereisen, suggereren ze een tweefasige benadering: begin met een laagtemperatuurfase om een schone thermische kaart te krijgen en de dekking te verifiëren, verhoog daarna, zodra plaatsing en marges bevredigend lijken, de temperatuur in een tweede fase om het gedode gebied uit te breiden, met de aanvaarding dat de temperatuurskaart tijdens die laatste verhoging minder betrouwbaar zal zijn.
Wat dit betekent voor toekomstige patiëntenzorg
Voor niet‑specialisten is de kernboodschap dat “de warmte een beetje terugdraaien” een hittegebaseerde kankerbehandeling eigenlijk veiliger en preciezer kan maken — althans in gecontroleerde laboratoriumomstandigheden. Lagere doeldtemperaturen gaven veel duidelijkere MRI‑temperatuurkaarten, waardoor het makkelijker werd te zien waar weefsel daadwerkelijk was vernietigd. Het nadeel is dat koelere verbrandingen kleinere laesies opleveren, dus artsen mogelijk langere of meerfasige behandelingen nodig hebben om grote tumoren te bedekken. Omdat dit onderzoek werd uitgevoerd in niet‑levende dierlijke levers zonder bloedstroom of ademhalingsbeweging, is vervolgonderzoek bij patiënten noodzakelijk. Desondanks wijst de studie op behandelprotocollen waarin MRI niet alleen wordt gebruikt om de naald te richten, maar ook om de verbranding in realtime te bekijken en bij te sturen, wat mogelijk de uitkomsten voor mensen met levertumoren kan verbeteren.
Bronvermelding: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
Trefwoorden: microgolfablaties, MRI‑thermometrie, leverkanker, thermische ablatie, beeldgestuurde therapie