Clear Sky Science · nl
Hybride kennis- en data-gedreven modellering voor robuuste detectie en sortering van spikes in menselijke C-vezel microneurografie
Luisteren naar de zenuwen van pijn en jeuk
Onze alledaagse ervaringen van pijn en jeuk beginnen als kleine elektrische pulsen die zich razendsnel voortplanten langs dunne zenuwvezels in de huid. Wetenschappers kunnen in wakker vrijwilligers naar deze signalen luisteren met een techniek die microneurografie heet, waarbij een haarfijn elektrode in een zenuw wordt geplaatst. In deze opnames spreken echter veel vezels tegelijk en klinken hun elektrische ‘stemmen’ vrijwel identiek. Dit artikel introduceert een nieuwe computergebaseerde methode om die overlappende signalen beter te scheiden en te identificeren, met als langetermijndoel het ontcijferen van hoe menselijke zenuwen sensaties zoals pijn en jeuk coderen.
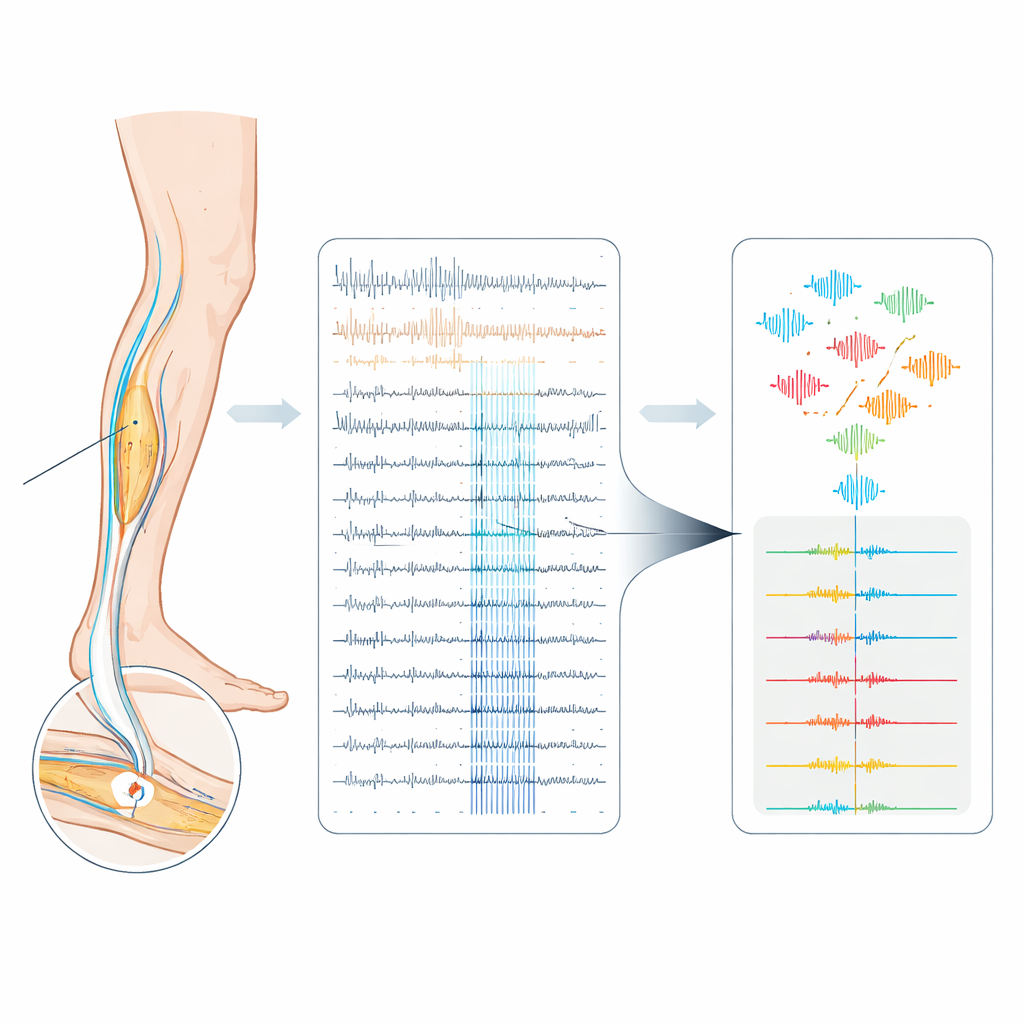
Waarom zenuwspikes zo moeilijk uit elkaar te houden zijn
Elke sensorische zenuwvezel communiceert met de hersenen via korte elektrische uitbarstingen die spikes worden genoemd. Niet alleen het aantal spikes, maar ook hun precieze timing en patroon kunnen bepalen hoe een stimulus aanvoelt. Helaas lijken de opgenomen spikes van verschillende vezels in perifere menselijke zenuwen vaak bijna hetzelfde en zijn ze weggestopt in ruis. Een enkele metalen elektrode neemt meestal meerdere vezels tegelijk op en de spike‑vormen verschuiven langzaam tijdens lange experimenten. Bestaande automatische methoden om spikes te scheiden zijn grotendeels ontworpen voor arrays met veel elektroden, waar ruimtelijke informatie helpt. Wanneer die methoden worden toegepast op eenelektrode‑opnames van menselijke C‑vezels—ongeïsoleerde vezels die cruciaal zijn voor pijn en jeuk—zijn ze vaak onbetrouwbaar.
De timing van de zenuw zelf als leidraad gebruiken
De auteurs bouwen voort op een slimme truc die al in de microneurografie wordt gebruikt, de zogenaamde “markeringmethode”. Tijdens een experiment krijgt de huid zachte elektrische pulsen met een lage, constante frequentie. Elke puls wekt betrouwbaar één spike op van elke geactiveerde C‑vezel na een vaste vertraging, zodat herhaalde responsen van dezelfde vezel een verticale “spoor” vormen wanneer de data proef na proef worden uitgezet. Als een vezel extra spikes heeft afgevuurd vlak voor de volgende puls, vertraagt zijn geleiding iets en arriveert de volgende respons later. Deze vertraging, bekend als activiteit‑afhankelijke vertraging, fungeert als een vingerafdruk van hoe actief die ene vezel is geweest. Het nieuwe werk breidt dit idee uit door het stimulatieprotocol zo te herontwerpen dat niet alleen de reguliere achtergrondpulsen, maar ook extra tussenliggende pulsen als timingankers worden gebruikt. Daardoor worden alle elektrisch opgewekte spikes in de opname nauwkeurig tijdgelinkt en gelabeld, wat een zeldzame ‘grondwaarheid’-dataset creëert in een rumoerige menselijke zenuw.
Een hybride route van ruwe ruis naar schone spiketreinen
Met deze grondwaarheid bouwt het team een semi‑geautomatiseerde analyseketen die deskundige kennis combineert met machine learning. In de kennisgestuurde fase berekenen ze eerst gemiddelde spiketemplates voor alle zichtbare sporen en kiezen ze de vezel met de grootste, schoonste spike als hoofddoel. Ze meten de gebruikelijke vertraging van die vezelresponsen en zoeken naar intervallen waarin de vertraging toeneemt, wat wijst op extra activiteit. Spikedetectie wordt vervolgens beperkt tot deze intervallen, wat de zoekruimte sterk verkleint en valse alarmen vermindert. In de datagedreven fase wordt elke gedetecteerde golfvorm omgezet in numerieke kenmerken—ofwel compacte beschrijvingen ofwel het ruwe 3‑milliseconde spanningssnippet zelf—en gevoed aan meerdere classificatoren, waaronder support vector machines en een populaire boosted tree‑methode genaamd XGBoost. De modellen worden getraind op de betrouwbaar gelabelde spikes uit het grondwaarheidsprotocol en afgestemd met kruisvalidering om de beste model‑kenmerkcombinatie voor elke opname te vinden.
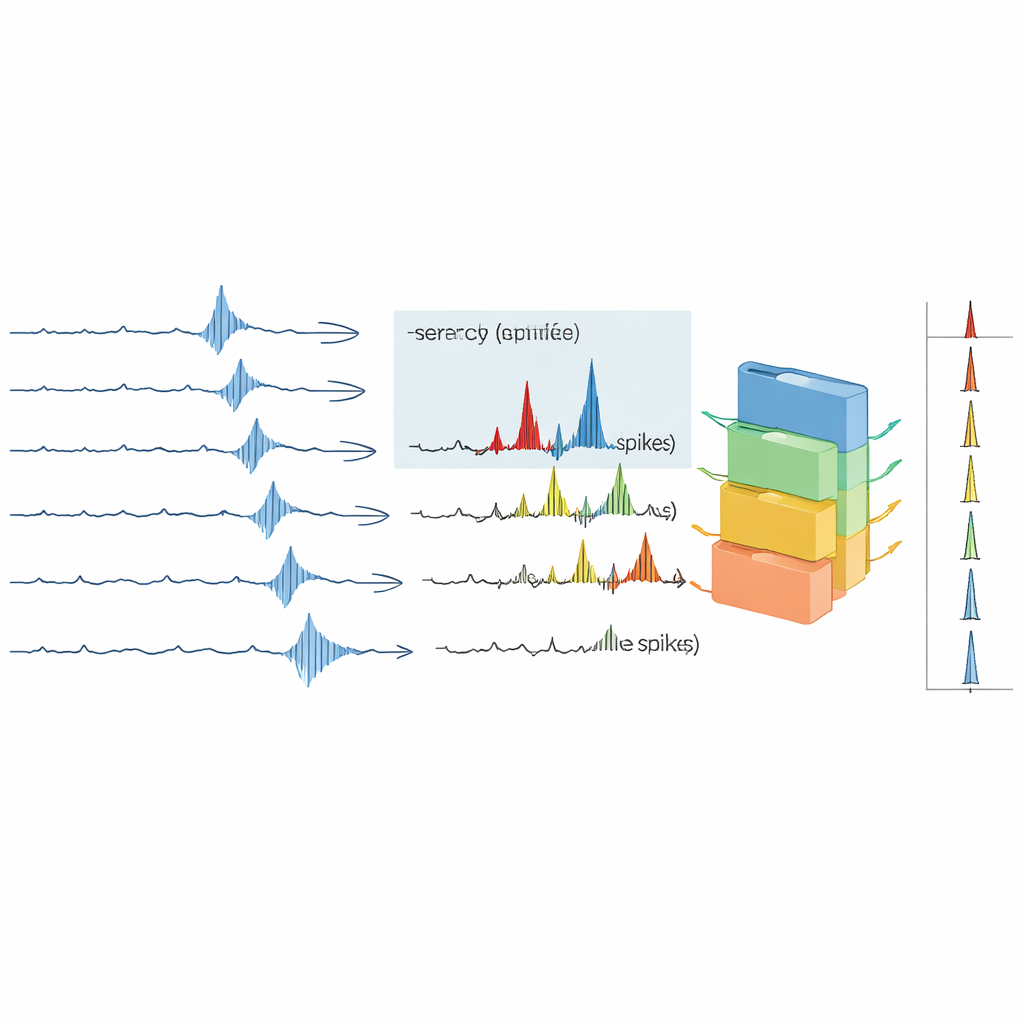
Hoe goed de nieuwe aanpak presteert
De auteurs testen hun pijplijn op zes uitdagende opnames van menselijke vrijwilligers, waarbij signaalkwaliteit en het aantal actieve vezels variëren. Ze vergelijken hun resultaten met Spike2, een veelgebruikt commercieel programma dat op template‑matching vertrouwt. Over de datasets heen wint geen enkel machine‑learningrecept elke keer, maar XGBoost met rauwe golfvormen geeft meestal de hoogste mediaanprestatie. Opnames met hogere signaal‑ruisverhoudingen en minder vezels sorteren het beste, terwijl één bijzonder rumoerige dataset met zeer vergelijkbare spike‑vormen in wezen onsorteerbaar blijft. In het algemeen bereikt de nieuwe pijplijn hogere F1‑scores en veel minder fout‑positieven dan Spike2, vooral wanneer de aandacht wordt beperkt tot tijdsintervallen waarin fysiologische latentieverschuivingen echte activiteit aangeven. In een realistisch voorbeeld waarbij een jeukopwekkend middel in de huid wordt geïnjecteerd, zijn de pijplijn en Spike2 het grotendeels eens over welke spikes van de doelvezel komen, maar de nieuwe methode vermijdt veel twijfelachtige extra spikes met onwaarschijnlijk hoge vuursnelheden.
Wat dit betekent voor het begrijpen van pijn en jeuk
Voor niet‑specialisten is de kernboodschap dat de studie een betrouwbaardere manier levert om naar individuele zenuwvezels bij mensen te luisteren, zelfs wanneer hun signalen klein, rumoerig en overlappend zijn. Door bekend fysiologisch gedrag—hoe spikes in de tijd uitlijnen en hoe hun vertragingen veranderen met recente activiteit—te combineren met moderne machine learning, kunnen de auteurs beter vaststellen welke spikes daadwerkelijk bij een bepaalde vezel horen en welke niet. Deze verbeterde sortering is een noodzakelijke stap voordat wetenschappers gedetailleerde spikepatronen veilig kunnen interpreteren als codes voor pijn, jeuk of andere sensaties. Hoewel sommige opnames te rommelig blijven om te analyseren, biedt de pijplijn duidelijke criteria om te beoordelen wanneer data bruikbaar zijn en legt ze een basis voor toekomstige studies die spontane pijnsignalen bij zenuwaandoeningen willen ontcijferen en behandelingen willen afstemmen op hoe individuele menselijke zenuwvezels vuren.
Bronvermelding: Troglio, A., Fiebig, A., Maxion, A. et al. Hybrid knowledge- and data-driven modelling for robust spike detection and sorting in human C-fiber microneurography. Sci Rep 16, 8975 (2026). https://doi.org/10.1038/s41598-026-41561-9
Trefwoorden: microneurografie, C-vezels, spike-sorting, pijn en jeuk, machine learning