Clear Sky Science · nl
Verklaarbare en veilige federated learning voor privacyverhogende huidkankerclassificatie met een lichtgewicht multi-schaal CNN
Waarom slimmer huidkankeronderzoek ertoe doet
Huidkanker is de meest voorkomende vorm van kanker wereldwijd en vroege opsporing kan levens redden. Toch berust een nauwkeurige diagnose nog steeds sterk op specialisten die vlekken en moedervlekken op de huid zorgvuldig beoordelen. Veel klinieken hebben zo’n expertise niet, en het delen van grote verzamelingen patiëntbeelden om betere computertools te trainen roept ernstige privacyzorgen op. Deze studie introduceert een nieuwe manier waarop ziekenhuizen kunnen samenwerken om een krachtig systeem voor huidkankerdetectie te trainen zonder ooit rauwe patiëntbeelden te delen, terwijl artsen ook heldere visuele verklaringen krijgen van wat het systeem ziet.
Samenwerken zonder geheimen prijs te geven
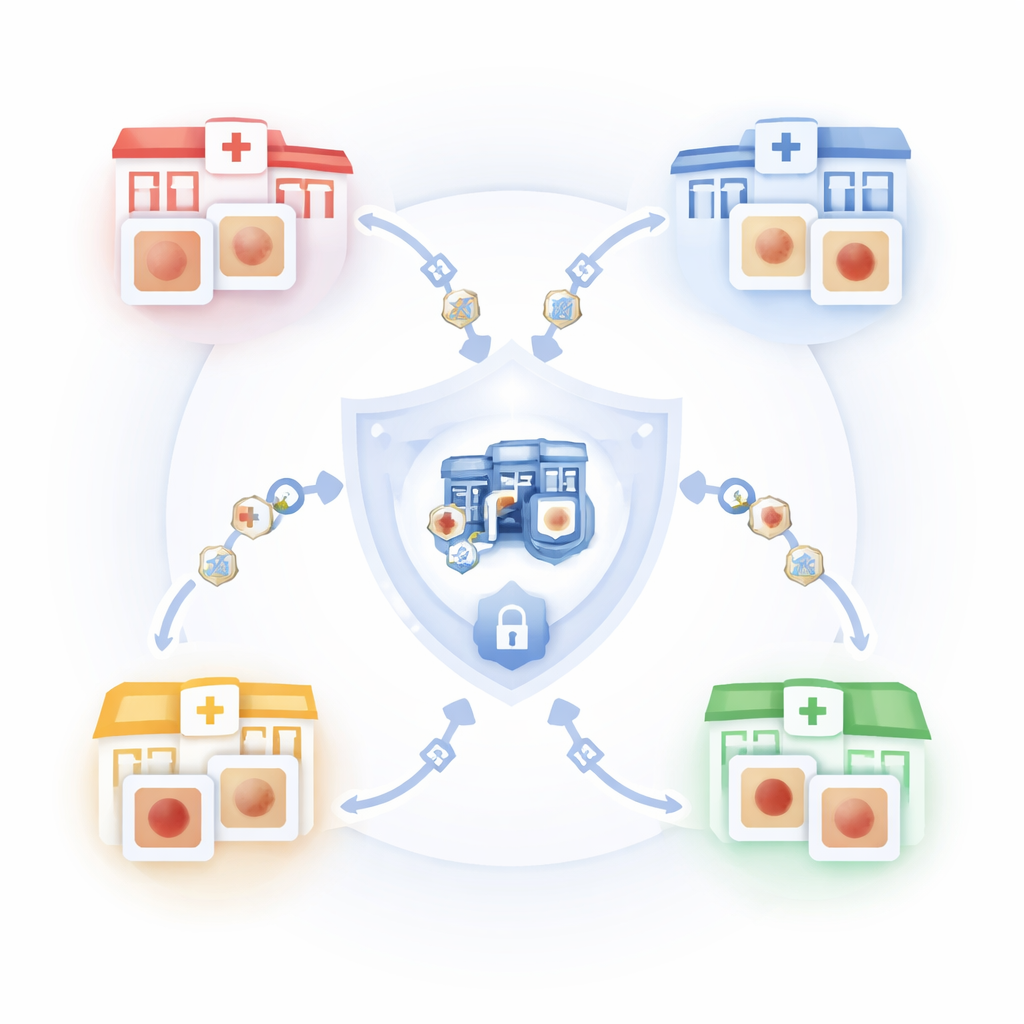
Het kernidee is een trainingsmethode genaamd federated learning. In plaats van huidbeelden naar een centrale server te sturen, bewaart elk ziekenhuis zijn foto’s lokaal en traint het een lokale kopie van hetzelfde computermodel. Alleen het aangeleerde “know‑how” (modelupdates) wordt naar een centrale server gestuurd, waar deze worden samengevoegd tot een beter globaal model en daarna teruggestuurd naar alle ziekenhuizen. In dit werk simuleren de auteurs meerdere ziekenhuizen die op deze manier samenwerken op een grote openbare dataset van huidlaesies, zodat het model profiteert van gevarieerde casussen terwijl de patiëntbeelden nooit de thuissituatie van de instelling verlaten.
Een slanke maar scherpziende beeldlezer
Om deze samenwerking praktisch te maken, ontwierp het team een nieuw lichtgewicht multi‑schaal convolutioneel neuraal netwerk (LWMS‑CNN). Veel populaire beeldmodellen zijn groot en traag om over ziekenhuisnetwerken te verzenden; dit model gebruikt daarentegen minder dan één miljoen trainbare parameters, een fractie van wat bekende architecturen vereisen. De structuur verwerkt elk huidbeeld op meerdere detailniveaus parallel, van fijne randen en texturen tot bredere patronen, en fuseert vervolgens deze aanwijzingen. Dit compacte ontwerp bleek zowel nauwkeurig als efficiënt en versloeg of evenaarde zwaardere modellen zoals ResNet en DenseNet op standaardmaten zoals nauwkeurigheid, precisie en F1‑score, terwijl het veel kleiner en sneller is—belangrijk voor gebruik op bescheiden ziekenhuisservers of zelfs edge‑apparaten.
Privacy vergrendelen met encryptie
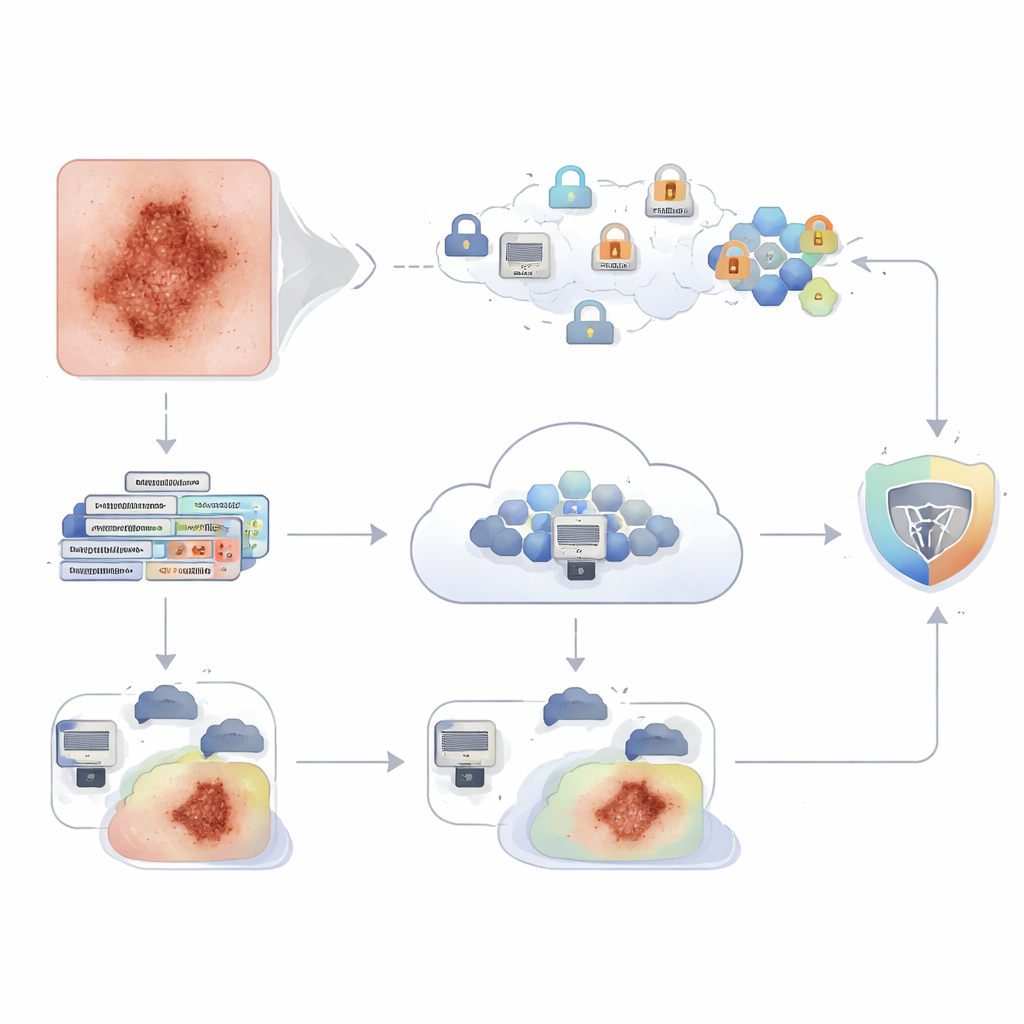
Hoewel federated learning voorkomt dat rauwe beelden worden verzonden, kunnen gedeelde modelupdates nog steeds informatie lekken bij geavanceerde aanvallen. Om deze kloof te dichten wikkelen de auteurs de hele uitwisseling in homomorfische encryptie, een cryptografische techniek waarmee de server modelupdates kan optellen en middelen kan berekenen terwijl ze versleuteld blijven. Ziekenhuizen versleutelen hun modelwijzigingen voordat ze deze verzenden; de server ziet alleen versleutelde waarden, maar kan nog steeds de gecombineerde update berekenen. Alleen een vertrouwde partij kan het geaggregeerde resultaat ontsleutelen. Tests toonden aan dat het toevoegen van deze bescherming de prestatie nauwelijks beïnvloedde: de nauwkeurigheid daalde met slechts ongeveer 0,3 procentpunt (van 98,62% naar 98,34%), een kleine prijs voor sterk verbeterde privacy en naleving van strikte medische gegevensregels.
De zwarte doos openen voor clinici
Hoge nauwkeurigheid alleen is niet genoeg in de geneeskunde; clinici moeten begrijpen waarom een algoritme een bepaalde beslissing nam. De studie voegt daarom verklaarbare‑AI‑hulpmiddelen toe bovenop het getrainde model. Eén hulpmiddel, SHAP, benadrukt welke delen van een beeld het meest bijdroegen aan een beslissing, waarbij elke pixelpatch als een “speler” in een stemspel wordt behandeld. Een ander, Grad‑CAM, legt een hittekaart over de laesie heen en laat zien waar het netwerk zijn aandacht op richtte toen het bijvoorbeeld een plekje als kwaadaardig of goedaardig bestempelde. Samen stellen deze weergaven dermatologen in staat te controleren of het model naar zinvolle structuren kijkt—zoals onregelmatige randen of kleurvariaties—en niet naar haren, lichtvlekken of achtergrondhuid, en om onzeker of foutief geclassificeerde gevallen te onderzoeken.
Van labtests naar klinieken in de praktijk
Het versleutelde LWMS‑CNN federated systeem werd getraind en geëvalueerd op de HAM10000‑dataset voor huidlaesies en vervolgens getest op twee aanvullende verzamelingen, ISIC 2019 en PAD‑UFES‑20, die verschillen in camera’s, laesietypen en patiëntpopulaties. Het behaalde hoge nauwkeurigheden in alle drie datasets, wat suggereert dat de aanpak goed generaliseert buiten een enkele databron. De auteurs onderzochten ook zwaardere, realistischere settings waarin verschillende “ziekenhuizen” verschillende mixen van gevallen zien, en vergeleken meerdere manieren om modelupdates te combineren; de standaardmethode FedAvg werkte het beste. Hoewel de experimenten werden uitgevoerd in een gesimuleerde multi‑clientopstelling in plaats van op fysiek gescheiden ziekenhuizen, tonen de resultaten aan dat een compact model, privacybehoudende training en duidelijke visuele verklaringen kunnen worden samengebracht in één kader. Voor patiënten wijst dit op toekomstige huidkankercontroles die nauwkeuriger, breder beschikbaar en respectvoller ten aanzien van privacy zijn, terwijl artsen toch nadrukkelijk betrokken blijven.
Bronvermelding: Sayeed, A.S.M., Birahim, S.A., Ullah, M.S. et al. Explainable and secure federated learning for privacy-enhancing skin cancer classification using a lightweight multi-scale CNN. Sci Rep 16, 11414 (2026). https://doi.org/10.1038/s41598-026-41360-2
Trefwoorden: huidkankerdetectie, federated learning, privacy van medische gegevens, verklaarbare AI, homomorfische encryptie