Clear Sky Science · nl
Voorspelling van levermetastasen bij colorectale kanker met een MRI-radiomodel
Waarom dit onderzoek ertoe doet
Colorectale kanker behoort tot de grootste doodsoorzaken wereldwijd, voornamelijk omdat de ziekte vaak naar de lever uitzaait voor of na de eerste operatie. Het vroegtijdig opsporen van deze uitzaaiingen kan het vooruitzicht van een patiënt drastisch veranderen, maar de huidige scans en bloedtesten zijn verre van perfect. Deze studie onderzoekt of computers kunnen “lezen tussen de pixels” van routinematige MRI-scans van de oorspronkelijke darmtumor om te voorspellen welke patiënten het meest waarschijnlijk levermetastasen zullen ontwikkelen, lang voordat die metastasen zichtbaar worden.
Meer zien dan het blote oog
Standaard medische beeldvorming wordt meestal geïnterpreteerd door het menselijk oog, dat heel goed is in het opsporen van duidelijke massa’s maar minder in staat is subtiele patronen waar te nemen. Radiomics is een nieuwe benadering die elke scan als een bron van meetbare data behandelt. Door grijstinten, vormen en texturen om te zetten in honderden numerieke kenmerken, stelt radiomics computers in staat patronen te detecteren die samenhangen met de agressiviteit van een tumor. In dit werk richtten de onderzoekers zich op twee veelgebruikte MRI-sequenties bij colorectale kanker: T2-gewogen beelden, die anatomie en vocht laten zien, en diffusie-gewogen beelden, die vastleggen hoe water zich binnen weefsels beweegt en gevoelig zijn voor de dichtheid van tumorcellen.
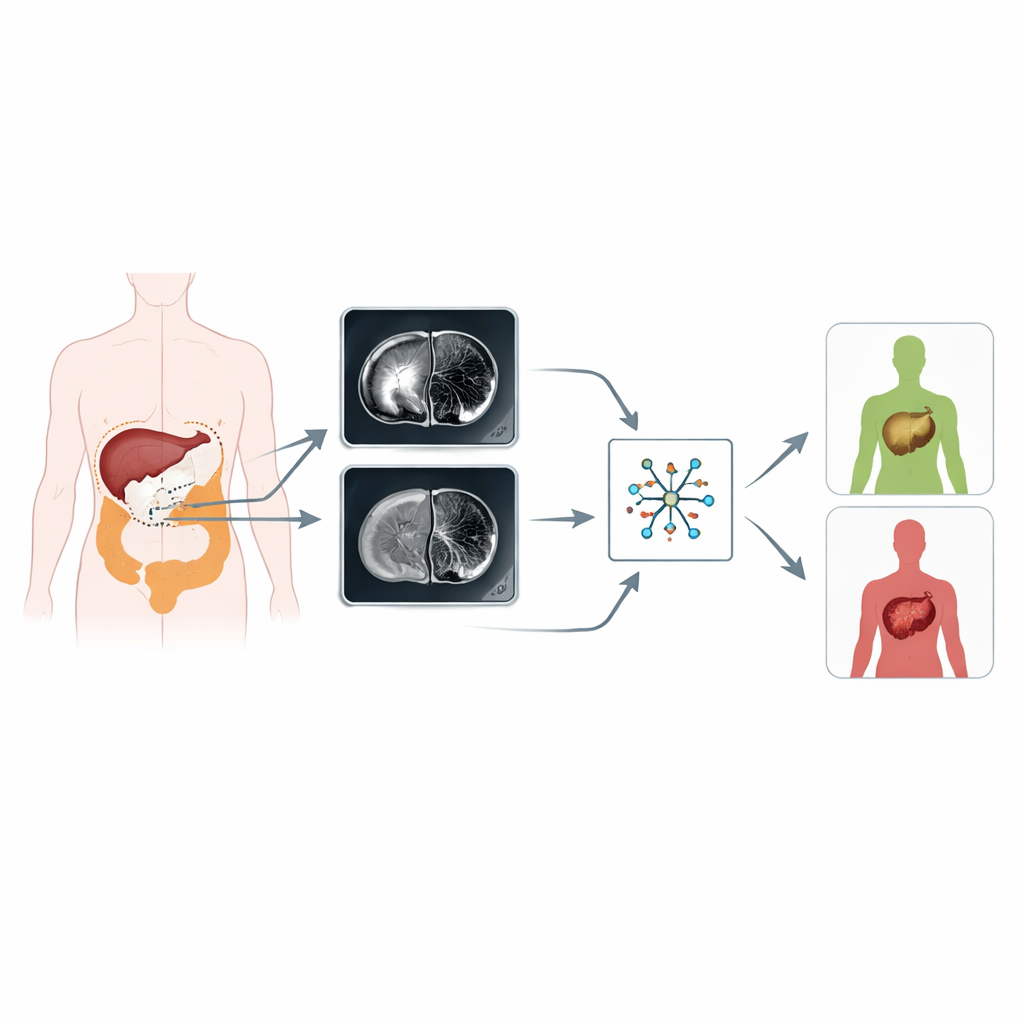
Hoe de studie is uitgevoerd
Het team analyseerde 194 patiënten met pathologisch bevestigde colorectale kanker uit twee ziekenhuizen. Alle patiënten ondergingen MRI-scans vóór enige behandeling en werden ten minste een jaar gevolgd om te zien wie levermetastasen ontwikkelde. Met gespecialiseerde software tekenden radiologen elke primaire tumor zorgvuldig af op de T2-gewogen en diffusie-gewogen beelden, snee voor snee, waarbij gas, cysten en omliggend vet werden vermeden. Uit deze regio’s extraheerde de computer 352 radiomische kenmerken die tumorvorm en interne textuur beschrijven. Statistische technieken werden vervolgens gebruikt om te controleren of deze metingen betrouwbaar waren tussen verschillende waarnemers en scanners, redundante informatie te filteren en de lijst terug te brengen tot de meest informatieve kenmerken.
Opbouw en testen van voorspellingsmodellen
Met de meest bruikbare kenmerken bouwden de onderzoekers verschillende voorspellingsmodellen. Eén model gebruikte alleen eenvoudige klinische informatie zoals leeftijd en tumormarkers in het bloed; andere modellen vertrouwden afzonderlijk op radiomics van T2-gewogen beelden of diffusie-gewogen beelden. Een gecombineerd radiomodel voegde kenmerken van beide MRI-sequenties samen, en een laatste “uniet” model mengde deze beeldvormingskenmerken met klinische risicofactoren. Het team trainde deze modellen in de grotere patiëntengroep van het ene ziekenhuis en testte ze vervolgens in een onafhankelijke groep van een tweede ziekenhuis, om te beoordelen hoe nauwkeurig elk model patiënten kon onderscheiden die wel of geen levermetastasen ontwikkelden.
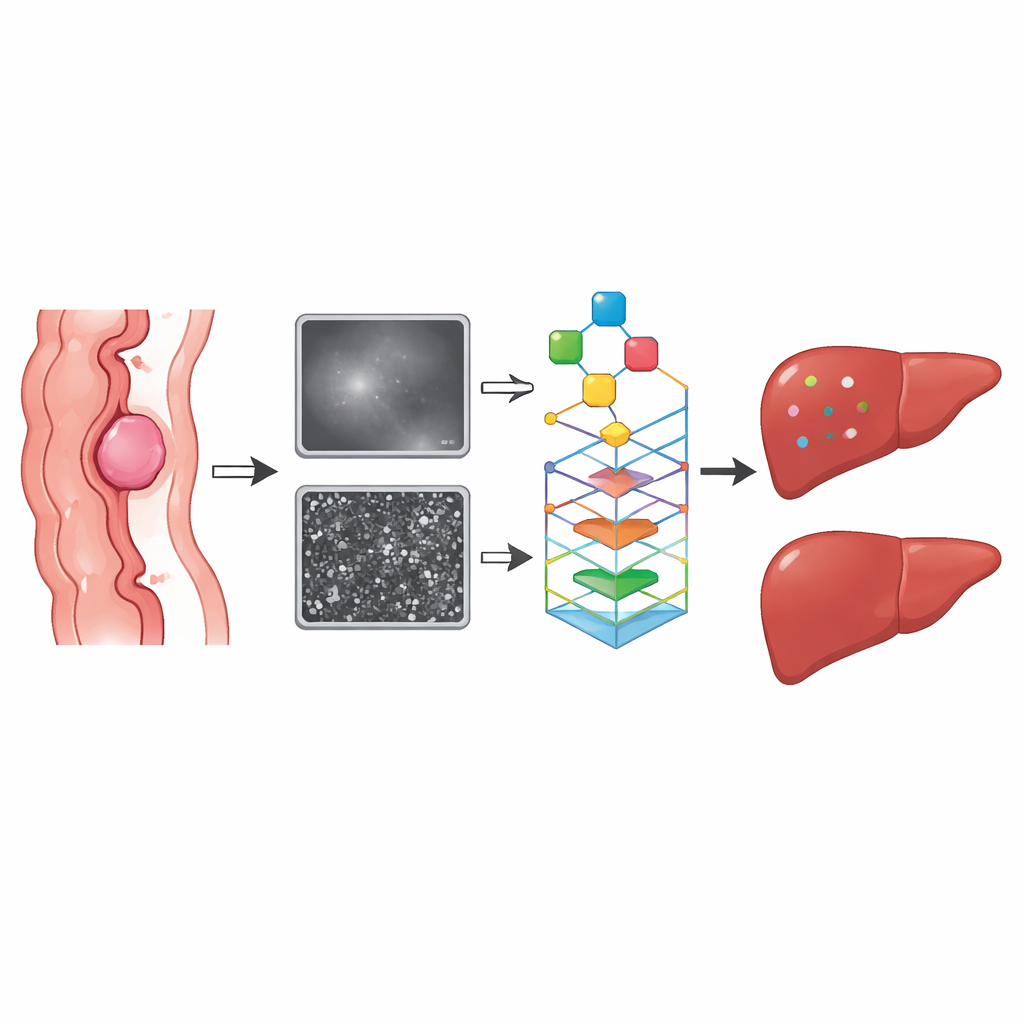
Wat de modellen onthulden
Het gecombineerde beeldvorming–klinische model presteerde het beste. Zowel in de trainings- als in de validatiegroepen overtrof het de modellen die alleen op klinische gegevens waren gebaseerd of op één enkele MRI-sequentie. Het vermogen om hoge- van lage-risicopatiënten te scheiden, gemeten met de oppervlakte onder de ROC-curve, viel in het hoge “goede” bereik. Kenmerken die tumortextuur en -vorm vastlegden, bleken vooral belangrijk: meer onregelmatige, heterogene tumoren waren waarschijnlijker geassocieerd met latere leveruitzaaiing. Een bloedmarker, carcino-embryonaal antigeen (CEA), bleek een onafhankelijke klinische risicofactor te zijn en verhoogde de nauwkeurigheid van het model verder wanneer deze met de radiomische kenmerken werd geïntegreerd.
De zwarte doos openen
Om dit complexe model transparanter te maken, pasten de onderzoekers een methode toe die bekendstaat als SHAP, die elk kenmerk een bijdrage toekent aan elke individuele voorspelling. Deze analyse toonde aan dat een bepaald textuurkenmerk uit de diffusie-gewogen beelden de sterkste invloed had op de vraag of het model een patiënt als hoog risico labelde. Door te benadrukken welke beeldpatronen het meest van belang zijn, kunnen zulke interpreteerbaarheidsinstrumenten het vertrouwen van clinici vergroten bij het gebruik van door kunstmatige intelligentie aangedreven voorspellingen in besluitvorming in de praktijk.
Wat dit voor patiënten betekent
De studie suggereert dat routinematig verworven MRI-scans van de primaire colorectale tumor verborgen aanwijzingen bevatten over de vraag of kankercellen waarschijnlijk de lever zullen inzaaien. Door deze subtiele beeldhandtekeningen te combineren met standaardbloedtesten, zou een radiomodel artsen kunnen helpen hoogrisicopatiënten eerder te identificeren, follow-up-schema’s op maat te maken en intensievere of gerichte behandelingen te kiezen wanneer dat nodig is. Hoewel grotere, prospectieve studies nog vereist zijn voordat deze benadering breed kan worden toegepast, wijst het op een toekomst waarin computers helpen extra prognostische informatie uit beelden te halen die al worden gemaakt, zonder patiënten aan extra ingrepen bloot te stellen.
Bronvermelding: Wu, YK., Wang, X., Du, PZ. et al. Prediction of colorectal cancer liver metastasis through an MRI radiomic model. Sci Rep 16, 11148 (2026). https://doi.org/10.1038/s41598-026-40970-0
Trefwoorden: colorectale kanker, levermetastasen, MRI-radiomics, kanker voorspelling, medische beeldvorming