Clear Sky Science · nl
Normalisatie van kleuring in histopathologie: methodebenchmarking met een multicenter dataset
Helderdere weefselbeelden voor artsen en computers
Wanneer pathologen weefselmonsters onder de microscoop bekijken, vertrouwen ze op subtiele tinten roze en paars om te beslissen of cellen gezond of kankerachtig zijn. Tegenwoordig kunnen die kleuren sterk variëren van het ene ziekenhuislaboratorium tot het andere, wat niet alleen menselijke diagnoses bemoeilijkt maar ook kunstmatige-intelligentietools in de war brengt die op deze beelden zijn getraind. Deze studie had tot doel precies te meten hoe groot dat kleurprobleem is en te testen welke computermethodes het beste werken om preparaatbeelden meer op elkaar te laten lijken zonder belangrijke details te verliezen.
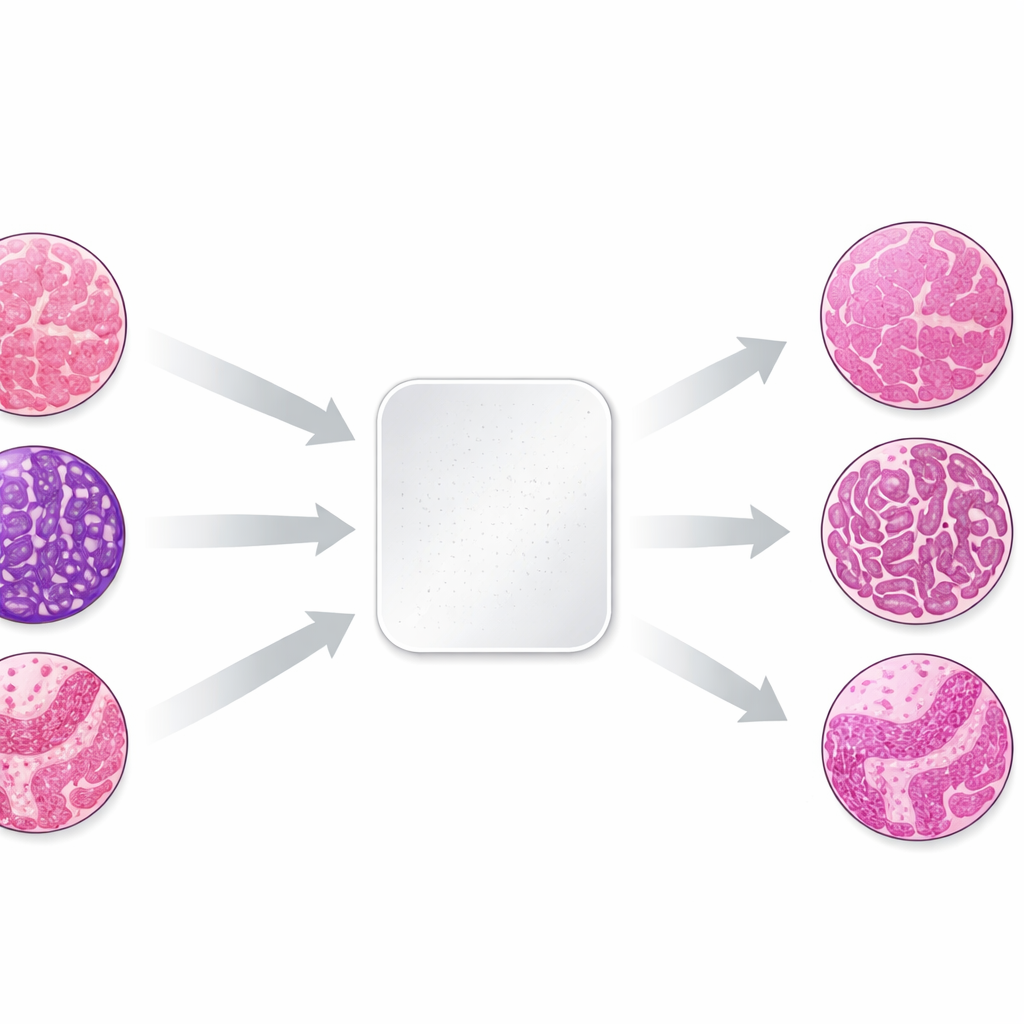
Waarom kleur van lab tot lab verschilt
Het werk richt zich op het meest gebruikte kleurpaar in de pathologie, hematoxyline en eosine, die celnuclei blauw-paars kleuren en het omliggende weefsel roze. Kleine verschillen in hoe laboratoria weefsel fixeren, verwerken en kleuren, en in hoe scanners beelden vastleggen, kunnen deze kleuren drastisch verschuiven. Om dit effect gecontroleerd te bestuderen, namen de auteurs drie kleine weefselmonsters—huid, nier en colon—uit dezelfde donorbokken en stuurden identieke ongekleurde secties naar 66 laboratoria in 11 landen. Elk lab gebruikte zijn routinematige kleuringsprocedure, waarna de voltooide preparaten werden gedigitaliseerd. Omdat het biologische materiaal vrijwel identiek was, weerspiegelden eventuele verschillen in uiterlijk hoofdzakelijk hoe elk lab het weefsel kleurde en afbeeldde.
Een uniek testplatform bouwen voor kleurcorrectie
De resulterende beeldcollectie toonde opvallende variatie: preparaten van hetzelfde weefselblok konden variëren van bleek tot bijna zwart, of verschuiven van koele naar zeer warme tinten. Het team kwantificeerde deze verschillen eerst door de gemiddelde rode en blauwe kleurwaarden in elk preparaat te meten. Vervolgens kozen ze per weefseltype één goed uitgebalanceerd preparaat als referentie en pasten acht verschillende kleurnormalisatiemethoden toe op alle andere. Vier methoden waren ouder, wiskundig gebaseerde benaderingen die globale kleurstatistieken aanpassen of kleurcomponenten scheiden en herschalen. Vier waren gebaseerd op moderne "generatieve" AI, die leert hoe beelden van de ene kleurstijl naar de andere te transformeren met neurale netwerken.
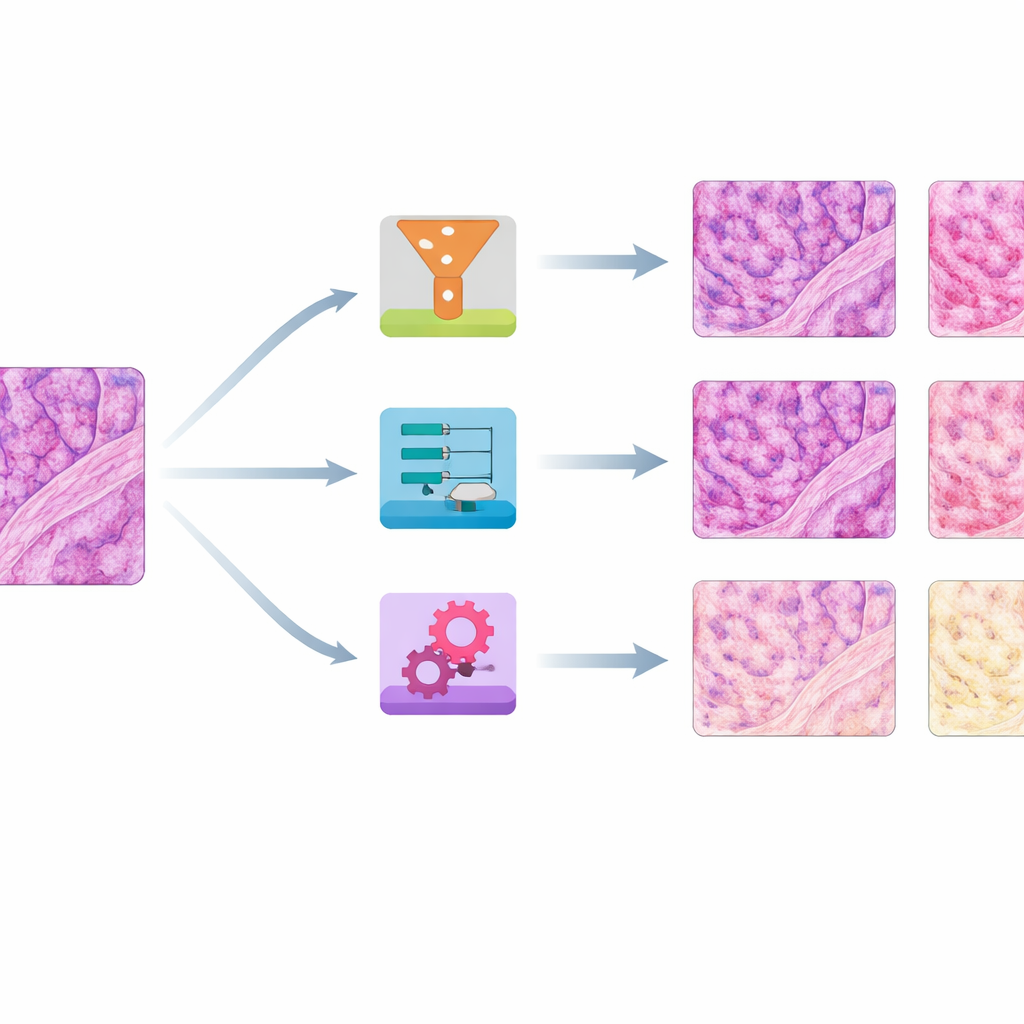
Welke methoden het beste werkten op kleur en structuur
Om de prestaties te beoordelen stelden de auteurs twee hoofdvragen: hoe nauwkeurig kwamen de gecorrigeerde beelden overeen met de referentiekleuren, en hoe goed behielden ze fijne weefselstructuur? Ze gebruikten verschillende numerieke scores die kleurverdelingen vergelijken, een hoog-niveau beeldgelijkheidsmaat uit de computervisie, en een structurele index die gevoelig is voor vervaging of vervormingen. Over huid, nier en colon heen leverde een eenvoudige methode genaamd histogrammatching—in wezen het herschikken van de kleurbalans van elk preparaat om de referentie na te bootsen—consistente de beste kleurmatch terwijl structuren grotendeels intact bleven. Een andere traditionele aanpak, Reinhard-normalisatie, presteerde vaak bijna even goed. Een derde, Vahadane, blonk uit in het behouden van structuur maar neigde ertoe alles naar een roze toon te duwen en de blauwe nucleaire kleur te onderdrukken.
Hoe de beelden eruitzagen voor menselijke experts en AI-tools
Ervaren pathologen beoordeelden genormaliseerde colon-preparaten om te zien hoe de methoden de interpretatie in de praktijk beïnvloedden. Ze controleerden of belangrijke lagen en celtypen goed te onderscheiden bleven, of over- of ondergekleurd materiaal verbeterde, en of er vreemde digitale artefacten verschenen. Geen enkele methode loste elk probleem op, maar histogrammatching leverde over het algemeen gelijkmatige, referentieachtige kleuren zonder duidelijke artefacten, vooral in sterk overgekleurd materiaal. Sommige AI-gebaseerde methoden, met name bepaalde varianten van CycleGAN en Pix2pix, produceerden realistisch ogende resultaten maar introduceerden af en toe subtiele gefingeerde structuren of kleurfoutjes in bloedcellen en achtergrondgebieden. Het team toonde ook aan dat normalisatie beïnvloedde hoe een geavanceerd cellendetectie-algoritme kernen telde en hoe een groot "foundation"-model de preparaten voorstelde, wat benadrukt dat kleurcorrectie downstream AI-gedrag sterk kan beïnvloeden.
Wat dit betekent voor toekomstige digitale diagnostiek
Samenvattend toont de studie aan dat kleurverschillen tussen laboratoria groot genoeg zijn om van belang te zijn voor zowel menselijke beoordelaars als geautomatiseerde systemen, en dat het uniformer maken van beelden een belangrijke stap is richting betrouwbare, gedeelde digitale pathologie. Verrassend genoeg presteerden in deze zorgvuldig gecontroleerde dataset met zeer vergelijkbare weefselinhoud eenvoudige globale methoden zoals histogrammatching vaak beter dan complexere deep-learningtechnieken, die veel meer trainingsdata nodig hebben dan één preparaat per lab. De auteurs maken hun 66-centrums dataset openbaar zodat anderen nieuwe methoden kunnen benchmarken en trainingsdata beter kunnen ontwerpen om real-world variatie te weerspiegelen. Voor patiënten kan vooruitgang op dit gebied resulteren in AI-systemen die goed overdraagbaar zijn tussen ziekenhuizen, wat consistentere diagnoses mogelijk maakt ongeacht waar een biopsie wordt verwerkt.
Bronvermelding: Khan, U., Härkönen, J., Friman, M. et al. Staining normalization in histopathology: Method benchmarking using multicenter dataset. Sci Rep 16, 11097 (2026). https://doi.org/10.1038/s41598-026-40943-3
Trefwoorden: digitale pathologie, kleurnormalisatie, histologiebeeldvorming, medische AI, kleurvariatie