Clear Sky Science · nl
Pan-cancer bevroren sectieclassificatie met een zachte mixture-of-experts vision transformer onder zwakke supervisie
Waarom dit telt in de operatiekamer
Wanneer chirurgen een vermoedelijke tumor wegnemen, hebben ze vaak slechts enkele minuten om te bepalen of alle kankercellen verwijderd zijn. Pathologen haasten zich om een snel ingevroren weefselvlak te beoordelen en een oordeel te geven terwijl de patiënt nog op de operatietafel ligt. Dit proces onder hoge druk kan worden bemoeilijkt door wazige preparaten, subtiele tumoren en eenvoudige tijdsdruk. De hier beschreven studie onderzoekt hoe een kunstmatige intelligentie (AI)-systeem pathologen kan helpen snel en betrouwbaar goedaardig van kwaadaardig weefsel te onderscheiden in verschillende organen, met apparatuur die realistisch is voor alledaagse ziekenhuizen.
Een snelle test met ingebouwde uitdagingen
Analyse van bevroren secties is een standaardprocedure in de moderne chirurgie: een dun stukje weefsel wordt ingevroren, in plakjes gesneden, gekleurd en onder de microscoop bekeken om te beoordelen of het goedaardig of kwaadaardig is en of de resectierand schoon is. In tegenstelling tot permanente laboratoriemonsters lijden bevroren secties vaak aan scheuren, vouwen en ongelijkmatige kleurreacties. Verschillende pathologen kunnen het oneens zijn bij grensgevallen, en de tijd dringt voortdurend. Deze problemen zijn vooral ernstig in kleinere of drukke ziekenhuizen, waar slechts een paar specialisten veel verschillende kankertypen moeten behandelen. De auteurs stellen dat een robuuste computerondersteuning beslissingen over bevroren secties consistenter, sneller en breder toegankelijk zou kunnen maken.
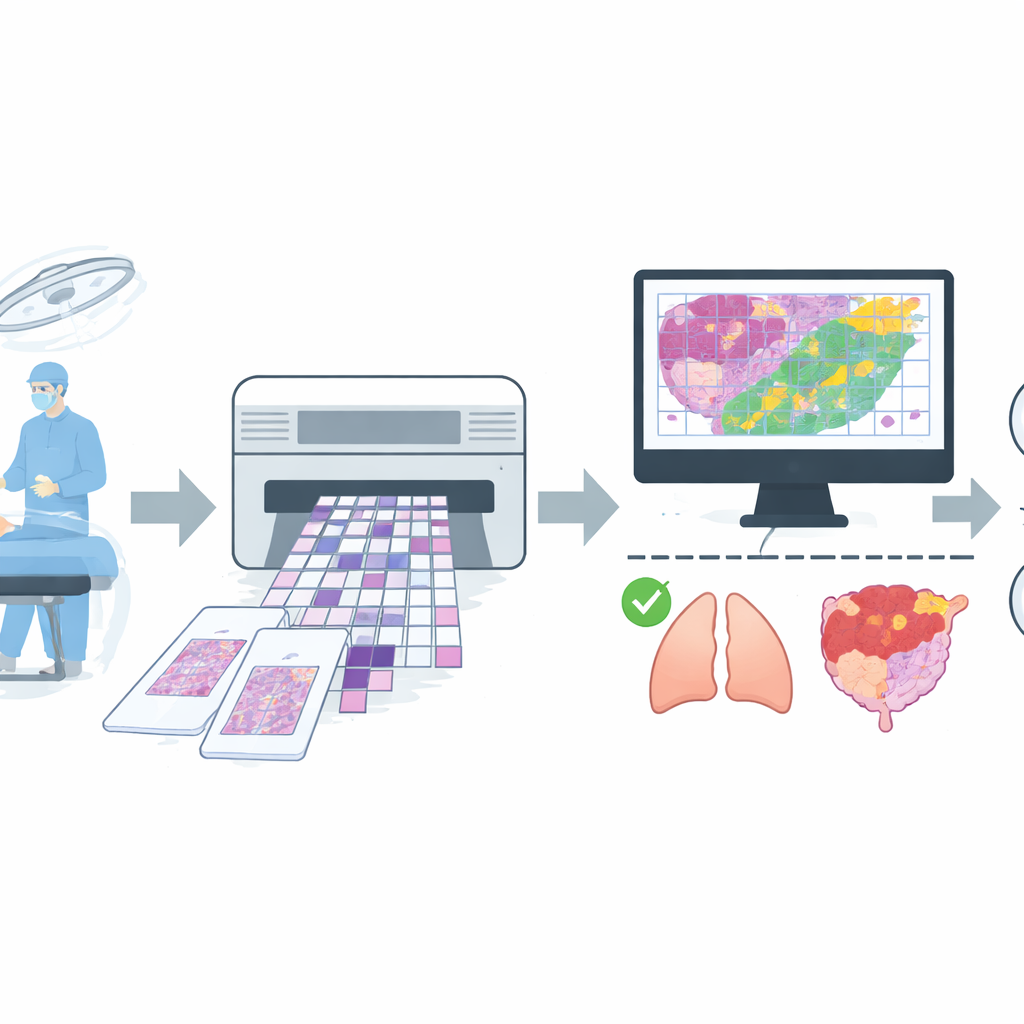
Het opbouwen van een veelzijdige real-world beeldenset
Om zo’n assistent te trainen, verzamelde het team een grote collectie digitale beelden uit routinematige operaties in een groot ziekenhuis. Ze verzamelden 4.754 whole-slide images van bevroren weefsel van meer dan 2.600 patiënten en pasten strikte kwaliteitsregels toe om preparaten met ernstige artefacten of onzekere diagnoses te verwijderen. De uiteindelijke dataset bevatte 4.667 slides, elk eenvoudig gelabeld als goedaardig of kwaadaardig op basis van overeenstemming tussen de snelle bevroren beoordeling en het latere, zorgvuldiger opgezette permanente sectierapport. De slides besloegen veelvoorkomende locaties zoals long, borst, schildklier, lymfeklieren en vrouwelijke voortplantingsorganen, plus een gemengde groep minder frequente locaties zoals maag, lever en huid. De data werden opgesplitst in afzonderlijke groepen voor training, verfijning en eindtesten, waarbij erop werd gelet dat beelden van dezelfde patiënt nooit in meer dan één groep voorkwamen.
Hoe de AI leert van zwakke aanwijzingen
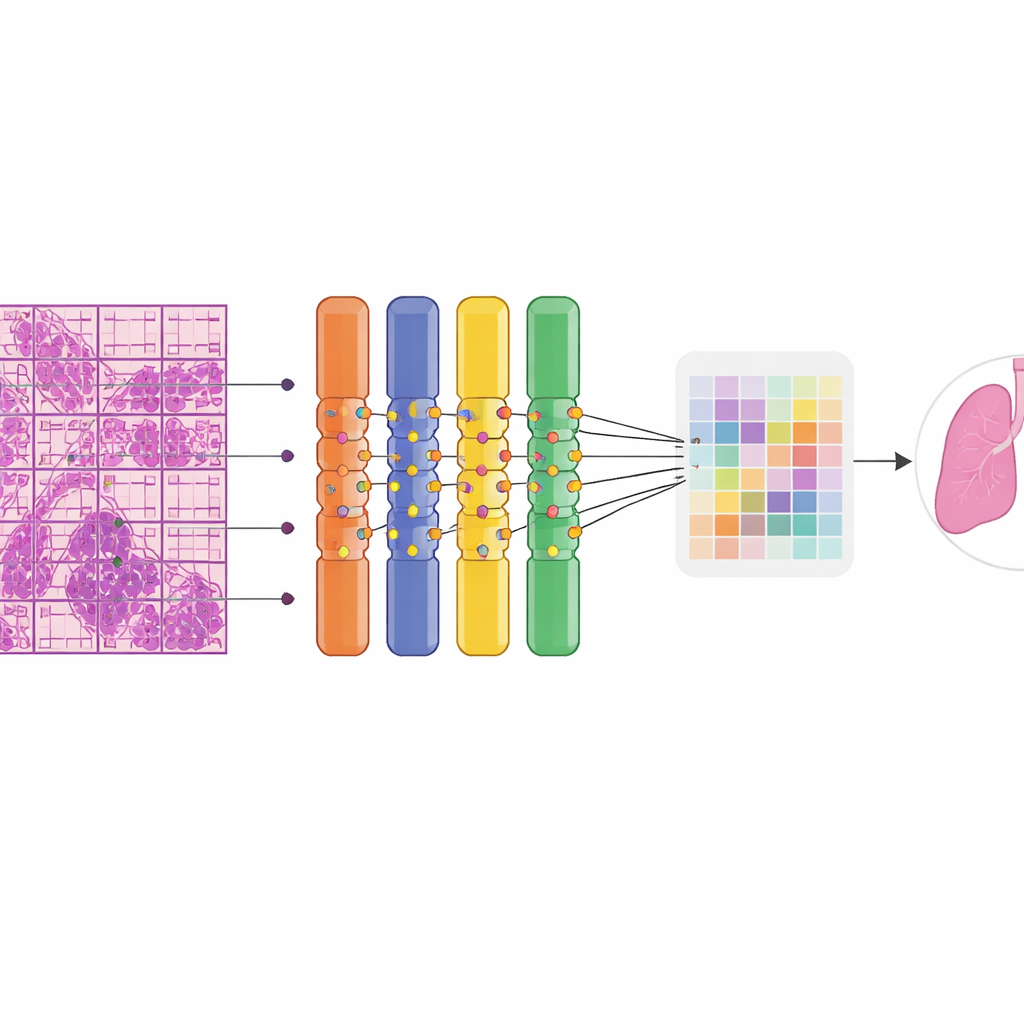
De onderzoekers bouwden hun model op een klasse neurale netwerken genaamd Vision Transformer, die uitblinkt in het vinden van patronen over grote beelden. Elk groot weefselbeeld werd automatisch in vele kleinere tegels en patches geknipt zodat het op standaard grafische hardware verwerkt kon worden. Een belangrijke innovatie was het vervangen van een deel van het netwerk door een “soft mixture of experts”, een verzameling van veel kleine gespecialiseerde takken die elk op verschillende visuele patronen focussen. In plaats van experts aan of uit te zetten, mengt het systeem hun bijdragen vloeiend, wat de training stabiliseert en betere benutting van beperkte data mogelijk maakt. Omdat pathologen geen contouren rond tumoren tekenden, moest het model leren van zwakke supervisie: het wist alleen of een gehele slide goedaardig of kwaadaardig was. Een multiple-instance learning-strategie bevorderde de meest verdachte patches binnen een kwaadaardige slide tot positieve voorbeelden, waardoor het netwerk geleidelijk de meest informatieve regio’s kon ontdekken.
Hoe goed het systeem in de praktijk werkt
Bij test op 669 niet eerder geziene slides onderscheidde de AI goedaardig van kwaadaardig weefsel met hoge accuraatheid. Het classificeerde ongeveer 90% van de gevallen correct en toonde een uitstekende capaciteit om de twee groepen te scheiden over verschillende waarschijnlijkheidsdrempels. Sensitiviteit, de kans om een werkelijk kwaadaardige slide te signaleren, lag rond vier op de vijf, terwijl specificiteit, de kans om een goedaardige slide terecht als goedaardig te bestempelen, nog hoger was. Belangrijk is dat de prestaties consistent bleven over organen: het detecteerde in de testset alle kwaadaardige long- en borstgevallen perfect en presteerde goed op zeldzamere groepen zoals adnexale tumoren van de vrouw en de gemengde “overige” organen. Kleurgecodeerde heatmaps overgelegd op de slides toonden dat de aandacht van het model samenviel met regio’s die door expert-pathologen als tumor werden herkend, inclusief metastatische haarden in lymfeklieren, terwijl normale structuren grotendeels werden genegeerd. Het systeem draaide efficiënt en had minder dan 5 GB geheugen nodig, waardoor het geschikt is voor gebruik op algemeen beschikbare grafische kaarten in plaats van op dure clusters.
Beperkingen, misstappen en ruimte voor verbetering
De auteurs onderzochten ook waar de AI de mist in ging. Vals-negatieve resultaten betroffen vaak extreem schaars aanwezige kankercellen, wazige scangebieden of hevige ontsteking die kwaadaardige nestjes verborg. Vals-positieven ontstonden vaak bij goedaardige aandoeningen die onder de microscoop op kanker lijken, zoals reactieve overgroei of vervormd bevroren weefsel. Omdat routinematige chirurgische workflows geen gedetailleerde tumorcontouren bevatten, kon het team niet exact kwantificeren hoe goed de heatmaps overeenkwamen met expertmarkeringen en was men aangewezen op kwalitatieve beoordeling. Sommige orgaantypen, zoals tong of bepaalde weke-delen tumoren, bleven ondervertegenwoordigd, wat erop wijst dat grotere, multicenterverzamelingen nodig zullen zijn om het bereik van het systeem uit te breiden.
Wat dit kan betekenen voor patiënten en ziekenhuizen
Al met al laat de studie zien dat een zorgvuldig ontworpen AI-systeem accuraat en interpreteerbaar kan assisteren bij een kernfunctie van de chirurgische pathologie: in realtime beslissen of weefsel goedaardig of kwaadaardig is over veel orgaantypen. Door te werken met alleen slide-niveau labels, te draaien op breed beschikbare hardware en verdachte gebieden voor menselijke controle te markeren, biedt het model een praktische route naar consistenter genomen beslissingen bij bevroren secties. Voor patiënten kan dit vertalen naar beter geïnformeerde operaties in één ingreep; voor ziekenhuizen, vooral die met beperkte deskundige staf, wijst het op een toekomst waarin geavanceerde digitale hulpmiddelen helpen hoogwaardige kankerzorg eerlijker te leveren.
Bronvermelding: Wu, J., Yang, M., Li, J. et al. Pan-cancer frozen section classification using a soft mixture of experts vision transformer under weak supervision. Sci Rep 16, 10297 (2026). https://doi.org/10.1038/s41598-026-40924-6
Trefwoorden: bevroren sectie, digitale pathologie, kankerdiagnose, vision transformer, zwak gesuperviseerd leren