Clear Sky Science · nl
Verklaarbare AI voor surveillance van gastro-intestinale laesies en precisiegerichte medicijnafgifte
Slimmere scans, veiligere behandelingen
Veel mensen zien op tegen kankerbehandelingen vanwege de ingrijpende bijwerkingen. Dit onderzoek verkent een toekomst waarin kleine inslikbare camera’s, slimme algoritmen en microscopische geneesmiddeldragers samenwerken zodat krachtige medicijnen alleen daar worden afgeleverd waar ze echt nodig zijn. Door de lus te sluiten tussen het opsporen van een probleem in het maag-darmkanaal en het direct ter plaatse behandelen ervan, streven de auteurs ernaar de zorg voor het maag-darmstelsel nauwkeuriger, minder invasief en veel veiliger te maken.
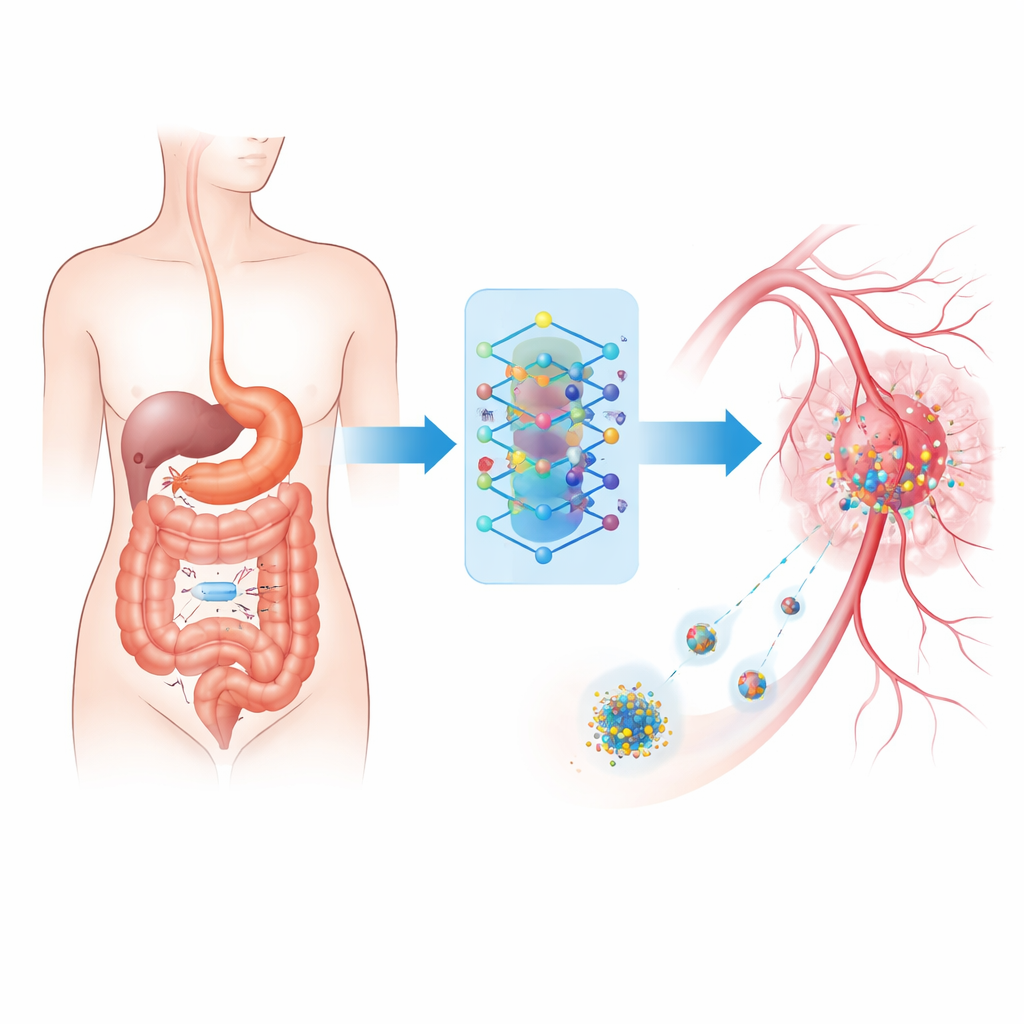
Kleine camera op reis
Het hart van het systeem is een draadloos inslikbaar beeldvormend apparaat — een vitaminegrootte capsule die op natuurlijke wijze door het spijsverteringskanaal beweegt en tienduizenden foto’s maakt. In plaats van uitsluitend te vertrouwen op een arts om de stroom van beelden te beoordelen, stuurt de capsule ze naar een draagbaar apparaat buiten het lichaam. Daar gebruikt een compacte computer geavanceerde patroonherkenningssoftware om normaal weefsel te scheiden van verdachte laesies die kankerachtig of ernstig ontstoken kunnen zijn. Deze opzet lijkt op bestaande capsule-endoscopie in ziekenhuizen, maar is geüpgraded om in realtime te werken en rechtstreeks te verbinden met behandelingsinstrumenten.
Kunstmatige intelligentie als beslisser
Het draagbare apparaat draait een zorgvuldig getraind beeldanalysemode l op basis van moderne computervisiemethoden. Het leerde 25 verschillende gastro-intestinale aandoeningen te herkennen — van poliepen en zweren tot ernstige ontstekingen — met behulp van een grote openbare verzameling endoscopie- en weefselfoto’s. Om om te gaan met het gegeven dat sommige ziekten veel zeldzamer zijn dan andere, trainden de auteurs het systeem in twee fasen: eerst om algemene visuele kenmerken van elke aandoening te leren, en daarna om het fijn af te stemmen zodat gevaarlijke maar ongewone bevindingen niet worden genegeerd. In tests classificeerde deze aanpak beelden in meer dan negen van de tien gevallen correct en presteerde bijzonder goed op kankergerelateerde categorieën.
Inzicht in de "zwarte doos"
Aangezien medisch personeel elk geautomatiseerd oordeel dat een medicatiedosis zou beïnvloeden moet kunnen vertrouwen, gebruikten de auteurs technieken van verklaarbare AI om te laten zien welke delen van elk beeld de beslissing van het model aansturen. Heatmap-achtige overlays benadrukken de exacte regio’s die het systeem belangrijk vond. Deze verklaringskaarten werden niet alleen visueel bekeken; ze werden ook gekwantificeerd met tests die maten hoe sterk het vertrouwen van het model veranderde wanneer gemarkeerde regio’s werden verwijderd of toegevoegd, hoe stabiel de verklaringen waren over herhaalde trainingsruns en hoe goed ze overlappen met door experts getekende laesiecontouren. Van de geteste methoden leverde een methode genaamd LayerCAM de meest getrouwe en consistente verklaringen, waardoor artsen konden verifiëren dat het systeem op de juiste plaats "kijkt".
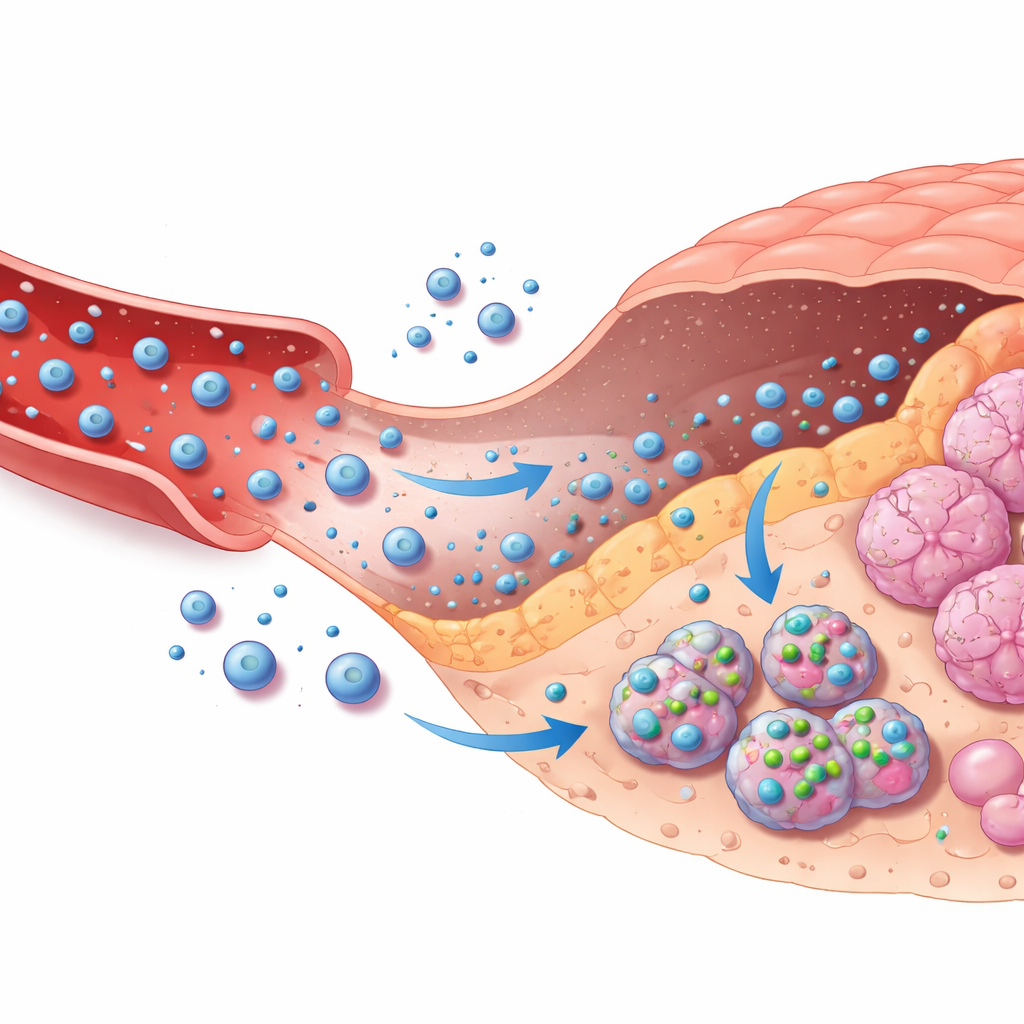
Het begeleiden van geneesmiddeldragers door het lichaam
Het tweede deel van het raamwerk koppelt deze op beelden gebaseerde beslissingen aan gerichte chemotherapie-afgifte. De auteurs modelleren hoe een veelgebruikt kankermedicijn, doxorubicine, reist vanaf een extern pompje door de bloedbaan, in tumorweefsel lekt, tumorcellen binnendringt en uiteindelijk wordt geklaard. Dit wordt vastgelegd in een meercompartimenten wiskundig model dat de medicijnniveaus in bloed, omringend weefsel en binnen cellen volgt. Op basis van de AI’s vertrouwen dat een laesie kwaadaardig is en hoe ernstig die lijkt, kiest een eenvoudige regelsysteem tussen geen behandeling, matige behandeling of intensieve behandeling, en past het aan hoe snel met geneesmiddel beladen nanodeeltjes hun lading afgeven en hoe lang de infusie duurt. Een veiligheidslaag controleert constant de voorspelde medicijnniveaus binnen cellen en verlaagt automatisch de dosering als een veilige bovengrens wordt benaderd, zelfs als de AI te veel vertrouwen toont.
Privacy beschermen en misbruik voorkomen
Aangezien dezelfde verbinding die beelden draagt ook behandelingscommando’s kan overbrengen, is beveiliging cruciaal. De auteurs introduceren een lichtgewicht privacy-systeem dat biomedische signalen verstoort met behulp van een chaotische wiskundige kaart voordat ze door het nano-netwerk van het lichaam reizen, waardoor onderschepte gegevens zeer moeilijk te interpreteren zijn. Daarnaast authenticeert de draagbare gateway apparaten en verifieert dat controlesignalen overeenkomen met verwachte fysieke patronen, wat helpt valse commando’s te blokkeren. Simulaties tonen hoe verschillende privacy-instellingen een kleine afname in detectienauwkeurigheid ruilen voor sterkere bescherming en identificeren gebruikspunten die de klinische prestaties hoog houden terwijl datalekken scherp worden beperkt. Samen met strikte doseringslimieten, nooduitschakelregels en veiligheidslogboeken, zijn deze maatregelen bedoeld om het systeem veerkrachtig te maken tegen zowel ongevallen als aanvallen.
Wat dit voor patiënten zou kunnen betekenen
Simpel gezegd schetst dit werk hoe een "zien-en-behandelen" lus in het lichaam zou kunnen werken: een inslikbare camera vindt verdachte plekken, een intelligente assistent interpreteert wat hij ziet met transparante redenering, en een gecontroleerd systeem voor medicijnafgifte reageert met zorgvuldig begrensde doses gericht op ziek weefsel. De studie is nog theoretisch en gebaseerd op simulaties, maar toont aan dat een dergelijke gesloten-lus-architectuur zowel therapeutische doelen kan bereiken als strikte veiligheidslimieten kan respecteren, zelfs wanneer de AI fouten maakt of wanneer omstandigheden van persoon tot persoon variëren. Indien in de praktijk gerealiseerd, zou dit soort systeem kunnen helpen om botte chemotherapie te veranderen in een veel preciezer en gepersonaliseerder instrument voor gastro-intestinale aandoeningen.
Bronvermelding: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
Trefwoorden: gastro-intestinale beeldvorming, verklaarbare AI, gerichte medicijnafgifte, nanomedicijnen, capsule-endoscopie