Clear Sky Science · nl
Gerichte activatie van Nrf2 via sulforafaan‑geladen exosomen verminderde azoöspermie in een rattenmodel
Waarom dit belangrijk is voor de gezondheid van mannen
Azoöspermie, het volledige ontbreken van zaadcellen in het sperma, is een van de moeilijkst behandelbare vormen van mannelijke onvruchtbaarheid. Veel mannen ontwikkelen deze aandoening nadat chemotherapie de testes heeft beschadigd. Huidige behandelingen kunnen vaak de zaadproductie niet opnieuw opstarten, waardoor kunstmatige voortplanting de enige optie blijft. Deze studie onderzoekt een meer natuurlijke herstelstrategie: het gebruik van piepkleine biologische belletjes, exosomen genoemd, om een uit broccoli afgeleid bestanddeel rechtstreeks in beschadigde testes te brengen en ze te stimuleren weer sperma te produceren.
Schade door kankerbehandeling
Chemotherapiemiddelen zoals busulfan zijn krachtige kankerbestrijders, maar kunnen ook de kiemcellen in de testes die zaadcellen produceren, vernietigen. In het hier gebruikte rattenmodel leidde een enkele injectie van busulfan in de testes tot een scherpe daling van zaadtelling en beweeglijkheid, een toename van misvormde zaadcellen en verlies van testisgewicht. Microscopisch onderzoek toonde dat de normale gelaagde structuur van de zaadproducerende buisjes was ingestort, met veel dode of ontbrekende cellen en littekenachtig weefsel ertussen. Ook daalden de testosteronniveaus, wat aangeeft dat de hormoonproductie eveneens was aangetast.
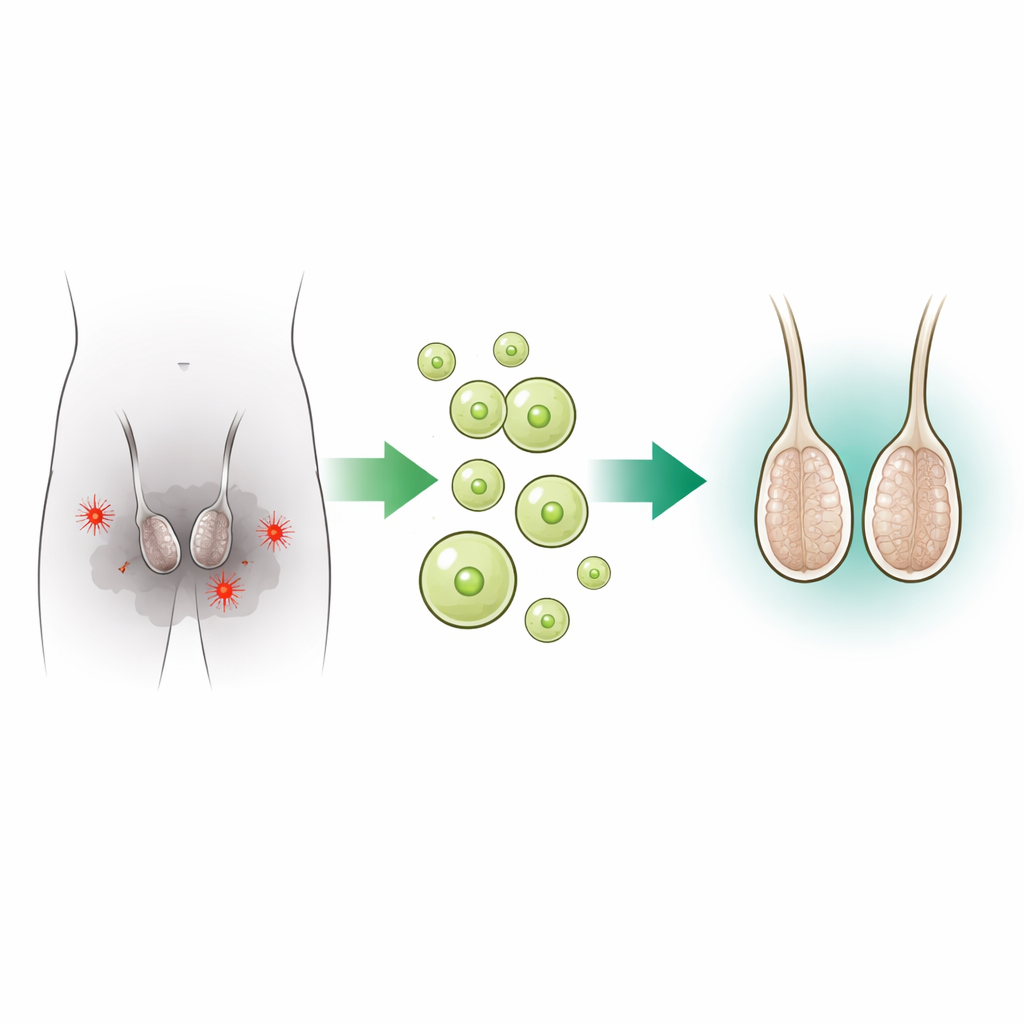
Exosomen omvormen tot kleine aflevercapsules
Om deze schade aan te pakken, richtten de onderzoekers zich op exosomen, natuurlijke nanogrote pakketjes die cellen gebruiken om moleculen naar elkaar te sturen. Ze isoleerden exosomen uit gedoneerd menselijk bloedserum en bevestigden hun grootte en vorm met meerdere technieken. Vervolgens laadden ze deze vesikels met sulforafaan, een plantverbinding die vooral bekend is uit broccoli en andere kruisbloemige groenten. Sulforafaan is een krachtige activator van Nrf2, een eiwit dat cellen helpt hun antioxidatieve afweer te activeren en met stress om te gaan. Door sulforafaan in exosomen te verpakken en ze rechtstreeks in ratten‑testes te injecteren, hoopte het team het lokale effect te vergroten en tegelijk de instabiliteit en lage opname te vermijden die sulforafaan in vrije vorm beperken.
Herstel van zaadcellen en weefselopbouw
Ratten werden verdeeld in vijf groepen: gezonde controles, onbehandelde azoöspermische dieren, en drie behandelingsgroepen die sulforafaan alleen, lege exosomen alleen, of sulforafaan‑geladen exosomen ontvingen. Twee maanden na een enkele injectie stak de combinatiebehandeling duidelijk boven de rest uit. Ratten die sulforafaan‑geladen exosomen kregen, vertoonden veel hogere zaadtellingen en beweeglijkheid, minder misvormde zaadcellen en een hogere testisgewichtindex dan onbehandelde dieren of dieren die slechts één van de componenten kregen. Onder de microscoop toonden hun testes een bijna normale rangschikking van kiemcellen in alle ontwikkelingsstadia, van stamachtige voorlopercellen tot rijpe zaadcellen, en veel minder vezelvorming. De expressie van sleutelgenen voor kiemcellen, DAZL en VASA, die door busulfan sterk verlaagd waren, keerde alleen in de combinatiegroep terug naar niveaus vergelijkbaar met gezonde controles.
Het herinstellen van celstress‑ en opruimsystemen
De studie onderzocht ook hoe de behandeling interne stress‑reactiebanen beïnvloedde. Na busulfan‑schade toonden de testes tekenen van oxidatieve ontregeling: het Nrf2‑gen, dat de antioxidatieve verdediging coördineert, was abnormaal verhoogd, en genen die betrokken zijn bij cellulaire “opruiming” via autophagie waren eveneens overactief. Zo’n aanhoudende activatie kan duiden op onopgeloste schade in plaats van bescherming. Sulforafaan‑geladen exosomen brachten Nrf2 en de autophagiegerelateerde genen LC3, Beclin1 en p62 weer richting normale niveaus, terwijl ze de activiteit van antioxidantenzystemen zoals glutathionperoxidase en de totale antioxidatieve capaciteit versterkten. Sulforafaan of exosomen alleen verschoof deze markers wel in de goede richting, maar normaliseerden ze niet zo volledig. Ook de testosteronniveaus verbeterden het meest in de combinatiegroep, wat wijst op beter herstel van hormoonproducerende cellen.
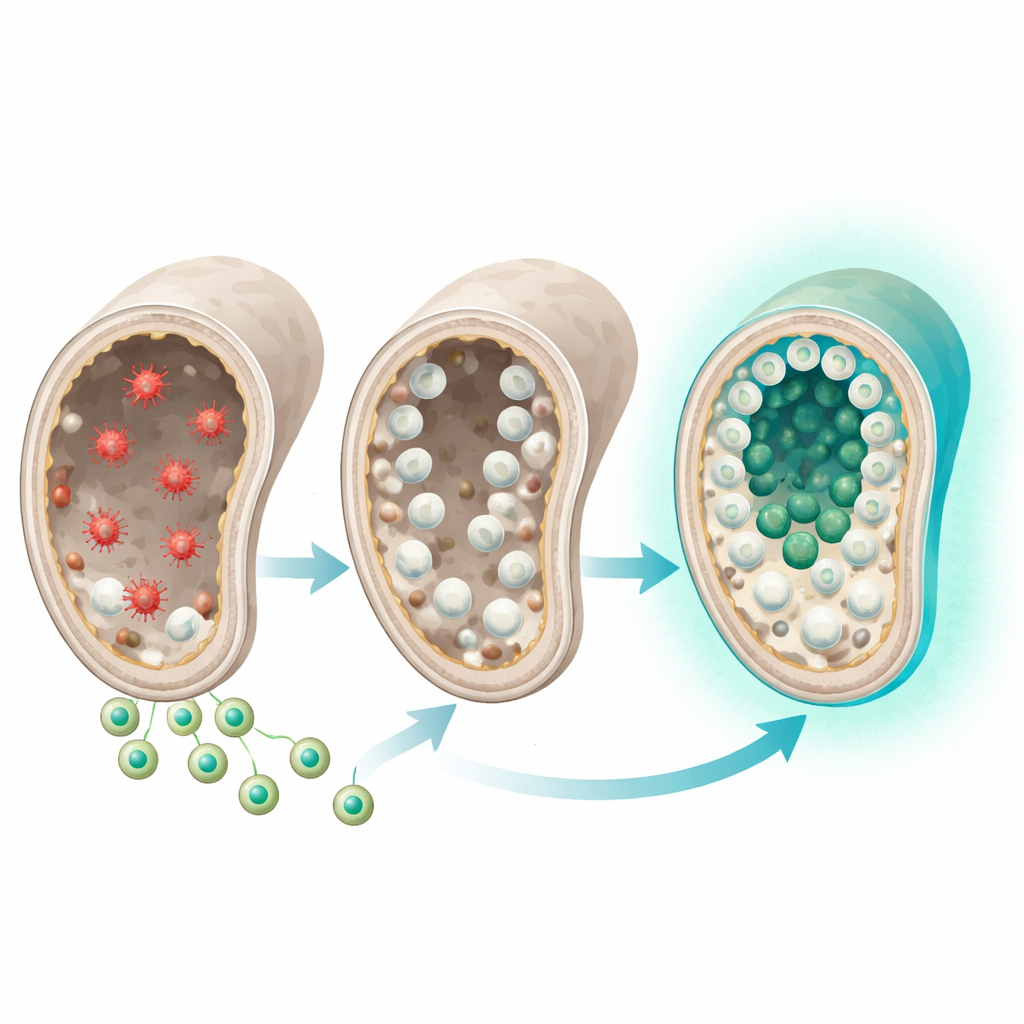
Een nieuwe weg naar herstel van vruchtbaarheid
Alles bij elkaar suggereren de bevindingen dat sulforafaan‑geladen exosomen beschadigde testes kunnen sturen weg van een chronische stressstatus en naar gebalanceerd zelfherstel. Door geruisloos antioxidant‑ en opruimroutes bij te stellen, maakte deze gerichte therapie het mogelijk dat kiemcelstam‑populaties herstelden en weer rijpe zaadcellen gingen vormen in een rattenmodel van chemotherapie‑geïnduceerde azoöspermie. Hoewel nog veel werk nodig is — zoals het testen van langetermijnveiligheid, het optimaliseren van doses en het bevestigen dat nakomelingen gezond zijn — wijst deze benadering op een toekomst waarin sommige vormen van mannelijke onvruchtbaarheid mogelijk niet alleen worden behandeld door zeldzame resterende zaadcellen te oogsten, maar door de testes te helpen hun natuurlijke zaadproducerende mechanisme te regenereren.
Bronvermelding: Ahmadian, S., Fajri, M., Roelen, B.A. et al. Targeted activation of Nrf2 via sulforaphane-loaded exosomes attenuated azoospermic condition in the rat model. Sci Rep 16, 9752 (2026). https://doi.org/10.1038/s41598-026-40709-x
Trefwoorden: azoöspermie, mannelijke onvruchtbaarheid, exosoomtherapie, sulforafaan, oxiderende stress