Clear Sky Science · nl
ABE9 gefuseerd met SpRY Cas9 nickase maakt nauwkeurige creatie van muismodellen zonder bijstanders mogelijk
Fijnere instrumenten voor het bouwen van betere ziektemodellen
Veel ernstige ziekten worden veroorzaakt door enkelvoudige letterfoutjes in ons DNA. Om deze aandoeningen te begrijpen en uiteindelijk te behandelen, maken onderzoekers vaak muizen met dezelfde mutaties als menselijke patiënten. Dergelijk precies herschrijven van DNA blijkt echter verrassend moeilijk: oudere methoden kunnen het genoom beschadigen, extra mutaties introduceren en experimentele resultaten vertroebelen. Deze studie introduceert een verfijnd genbewerkingsinstrument, ABE9-SpRY, dat is ontworpen om één specifiek DNA‑lettertje te veranderen terwijl omliggende letters — en de rest van het genoom — grotendeels ongemoeid blijven.
Van grof knippen naar subtiele DNA-aanpassingen
Traditionele CRISPR‑Cas9‑bewerking werkt als een moleculaire schaar die beide DNA‑strengen knipt. Cellen repareren die breuken onvolmaakt, vaak met kleine inserties of deleties die genen op onvoorspelbare manieren verstoren. Dat is nuttig om genen uit te schakelen, maar niet om een precieze ziekteveroorzakende mutatie na te bootsen. Basisbewerkers knippen het DNA juist niet. In plaats daarvan zetten ze chemisch één DNA‑letter om in een andere — hier A in G — terwijl de dubbele helix intact blijft. Deze aanpak verkleint grote deleties en herschikkingen aanzienlijk, maar eerdere adenine‑base‑editors hadden nog drie belangrijke nadelen: ze bewerkten soms nabije “bijstander”-letters, konden alleen doelwitten naast specifieke korte sequentietekens bereiken, en veroorzaakten soms wijzigingen op onbedoelde plaatsen in het genoom.
Het ontwerp van een selectievere moleculaire pen
De onderzoekers wilden al die beperkingen tegelijk aanpakken. Ze begonnen met ABE9, een nieuwere variant van een base‑editor die zijn activiteit richt op een zeer smalle DNA‑strook, waardoor het “bewerkingsvenster” krimpt en veel minder nabije letters per ongeluk veranderen. Vervolgens fuseerden ze ABE9 met een gemodificeerde Cas9‑nickase genaamd SpRY. In tegenstelling tot standaard Cas9, dat een strikt “NGG”-motief naast het doel vereist, kan SpRY een veel breder scala aan DNA‑sequenties herkennen. Daardoor worden ziektegerelateerde posities in het genoom bereikbaar die voorheen buiten bereik lagen. Het resulterende fusiegereedschap, ABE9‑SpRY, is bedoeld om zowel zeer precies als veel flexibeler te zijn in waar het kan werken.
De nieuwe editor testen in cellen en embryo’s
Om te beoordelen of ABE9‑SpRY zijn belofte waarmaakte, vergeleek het team het met een veelgebruikte, agressievere editor genaamd ABE8e‑SpRY. Ze richtten zich op vier ziekte‑relevante posities in genen die ionkanalen coderen (TPC1, TPC2 en TRPM4), die belangrijke rollen spelen in hart‑ en leverfunctie. In muizencellen gekweekt in het laboratorium bewerkte ABE8e‑SpRY de doeltreffende letter efficiënter maar veranderde ook veel nabijgelegen basen. ABE9‑SpRY daarentegen leverde minder totale bewerkingen maar een veel hoger aandeel “schone” uitkomsten — sequenties waarin alleen de beoogde letter veranderde, zonder extra mutaties in de lokale regio. Ditzelfde patroon werd waargenomen in muisembryo’s. Wanneer de onderzoekers bewerkingscomponenten in bevruchte eieren injecteerden, zette ABE8e‑SpRY vaak bijna alle kopieën van het doelgen om, maar met veel bijstanderwijzigingen. ABE9‑SpRY bewerkte in totaal minder kopieën, maar waar het wel werkte, was de DNA‑sequentie doorgaans exact gecorrigeerd zoals gepland.
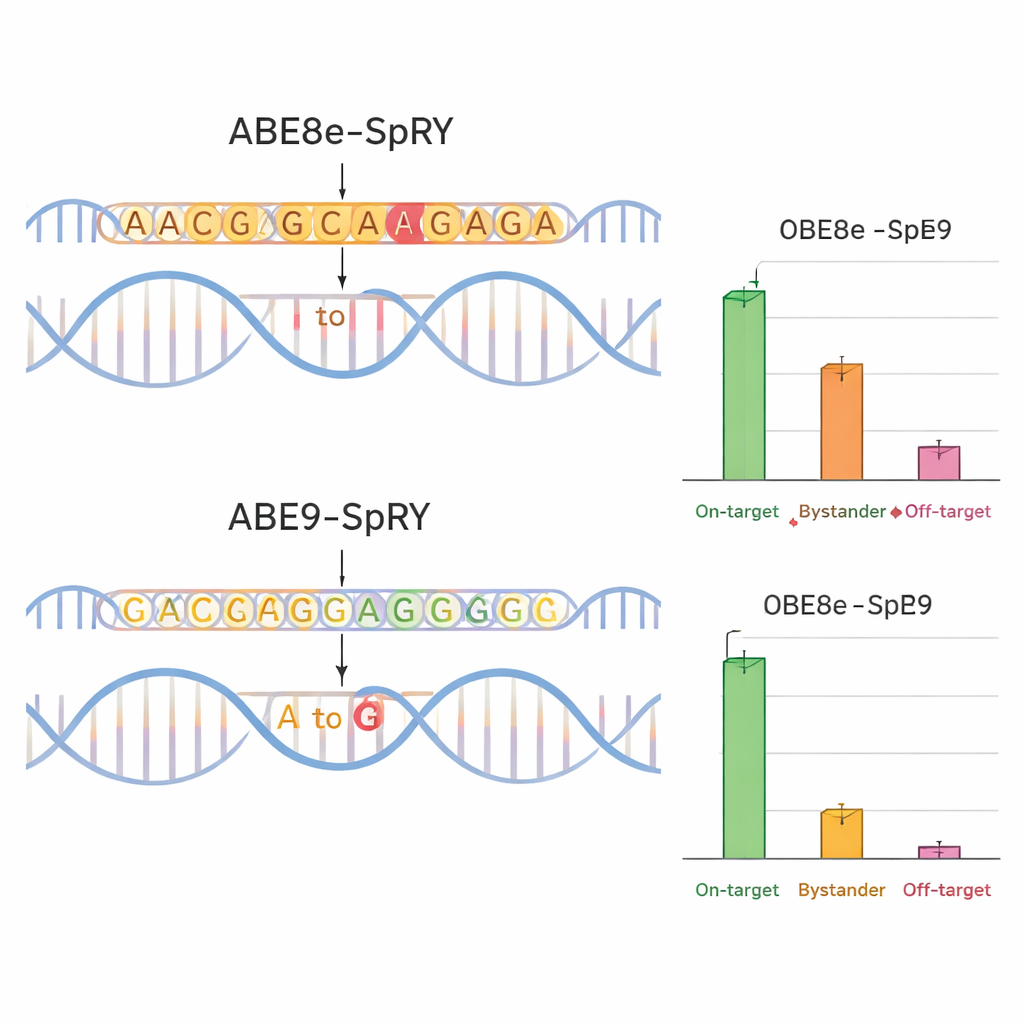
Schonere bewerkingen, minder bijwerkingen
Nauwkeurigheid gaat niet alleen over de lokale DNA‑buurt. Het team onderzocht ook of hun editor verre regio’s van het genoom veranderde. Met behulp van computationele voorspellingen en gerichte sequenering maten ze off‑target wijzigingen op waarschijnlijke look‑alike locaties in muisembryo’s. ABE8e‑SpRY introduceerde vaak onbedoelde A‑naar‑G wijzigingen op deze plekken, soms op verrassend hoge niveaus. ABE9‑SpRY toonde veel minder van dergelijke gebeurtenissen, met slechts zeldzame off‑target bewerkingen en geen detecteerbare activiteit in een gespecialiseerde test voor Cas9‑onafhankelijke DNA‑schade. Belangrijk is dat, wanneer ABE9‑SpRY afzonderlijk — niet in pooled tests — werd gebruikt om twee specifieke mutaties in muizen in te brengen, het veel founder‑dieren genereerde waarin de gewenste correctie op hoge niveaus aanwezig was en betrouwbaar aan nakomelingen werd doorgegeven, wederom met minimale bijstanderwijzigingen of kleine inserties en deleties.
Precisiebewerking uitbreiden naar menselijke stamcellen
Aangezien patiëntspecifieke stamcellen steeds vaker worden gebruikt om ziekte te bestuderen en medicijnen te testen, probeerden de onderzoekers ABE9‑SpRY ook in humane geïnduceerde pluripotente stamcellen. Ze richtten zich op de menselijke versie van het TPC1‑gen op een positie equivalent aan één van de muissites. Met een fluorescerende reporter om voor bewerkte cellen te verrijken, vonden ze dat ABE8e‑SpRY hogere ruwe bewerkingspercentages opleverde maar opnieuw meerdere nabijgelegen basen wijzigde. ABE9‑SpRY bewerkte in totaal minder allelen, maar het aandeel perfect bewerkte reeksen — één beoogde verandering en niets anders — was opvallend hoger, met minder verstorende inserties of deleties. In stamcelonderzoek, waar individuele klonen worden uitgebreid voor gedetailleerde studie, is dit soort “schone” bewerking doorgaans waardevoller dan brute‑force efficiëntie.
Waarom dit belangrijk is voor toekomstig ziekteonderzoek
Voor onderzoekers die willen begrijpen hoe één DNA‑letter verandering tot ziekte leidt, kunnen extra onbedoelde mutaties misleidend zijn. Deze studie toont aan dat ABE9‑SpRY, hoewel iets minder krachtig in ruwe bewerksnelheid, enkele letterveranderingen met opvallende nauwkeurigheid en brede targetflexibiliteit in de genomen van muizen en menselijke stamcellen kan schrijven. Dat maakt het een veelbelovende werktuig voor het bouwen van getrouwe dier‑ en celmodellen van menselijke genetische aandoeningen, vooral in situaties waarin zelfs één willekeurige mutatie de biologie zou kunnen verwarring of een potentiële therapie zou kunnen ontsporen.
Bronvermelding: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Trefwoorden: adenine basisbewerking, CRISPR ziektmodellen, muugenetica, off-target effecten, hiPSC genbewerking