Clear Sky Science · nl
Pancreatitis-geassocieerde chymotrypsine C (CTRC)-variant p.R240Q belemmert selectief de afbraak van trypsinogeen door verstoring van langeafstands-elektrostatische interacties
Waarom dit van belang is voor de gezondheid van de alvleesklier
Chronische pancreatitis is een pijnlijke, langdurige ontsteking van de alvleesklier die kan leiden tot diabetes, problemen met de spijsvertering en een ernstige aantasting van de levenskwaliteit. Deze studie onderzoekt waarom sommige mensen kwetsbaarder zijn door kleine erfelijke veranderingen in hun spijsverteringsenzymen. Door in te zoomen op één genetische variant in een beschermend enzym, laten de onderzoekers zien hoe een subtiele moleculaire verandering de balans kan verschuiven van bescherming naar zelfbeschadiging binnen de alvleesklier.
Een ingebouwd beveiligingssysteem in de spijsvertering
Onze alvleesklier produceert krachtige eiwitten afbrekende enzymen die normaal gesproken in een inactieve vorm naar de darm worden afgegeven. Een van deze voorlopers, trypsinogeen, kan soms te vroeg actief worden, namelijk binnen de alvleesklier zelf. Wanneer dat gebeurt, kan het orgaan van binnenuit worden afgebroken en ontsteking veroorzaken. Om dit onder controle te houden, gebruikt het lichaam beveiligingsmechanismen, waaronder een remmend eiwit (SPINK1) en een ander spijsverteringsenzym, chymotrypsine C (CTRC). CTRC heeft een dubbele rol: het helpt spijsverteringsenzymen te activeren waar en wanneer dat nodig is, maar het knipt ook overtollig trypsinogeen af voordat het actief trypsine kan worden en schade veroorzaakt. Mensen die verzwakte vormen van CTRC erven, hebben een bekend verhoogd risico op chronische pancreatitis.
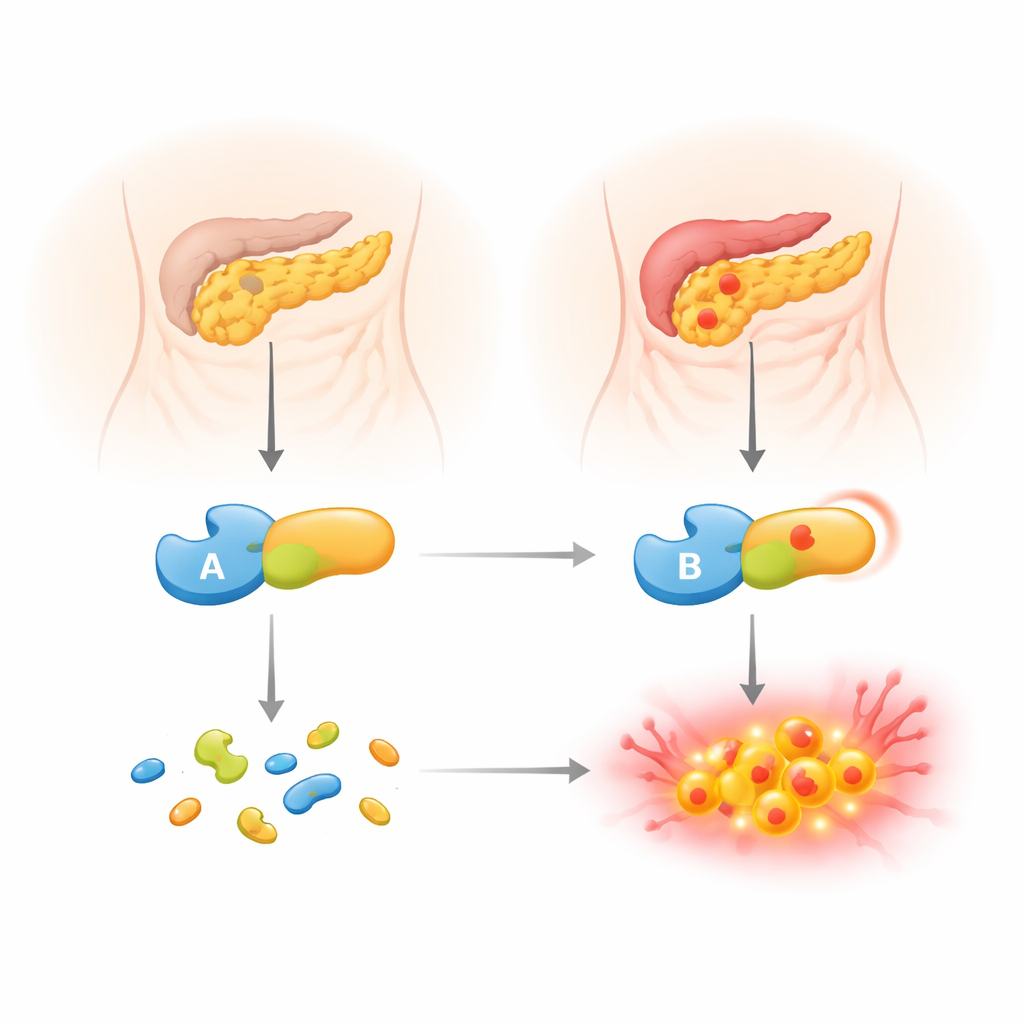
Een zeldzame genetische verandering onder de microscoop
Het team richtte zich op een ongewone CTRC-variant die p.R240Q wordt genoemd, gevonden bij een jongen uit Slowakije met in de kindertijd ontstane chronische pancreatitis en bij zijn aangedane vader. Deze variant verandert één bouwsteen op het enzymoppervlak en vervangt een positief geladen eenheid door een neutrale. Grote genetische databanken classificeren het als waarschijnlijk onschadelijk, maar het is in meerdere jonge patiënten met de ziekte gevonden. Om uit te vinden wat het echt doet, combineerden de auteurs genetische informatie uit het gezin met gedetailleerde laboratoriumexperimenten. Ze vergeleken het variantenzym naast normaal CTRC en onderzochten hoe goed het door cellen wordt geproduceerd, hoe actief het is op standaard testsubstraten en hoe het interacteert met trypsinogeen, de sleutelstof die het zou moeten beheersen.
Normale kracht, maar misplaatste richting
In eerste instantie toonden de onderzoekers aan dat cellen het p.R240Q-enzym net zo goed maken en uitscheiden als de normale versie, dus de variant veroorzaakt geen verkeerde vouwing of productiefout. In reageerbuisassays met een klein synthetisch peptide en een melkproteïne (beta-caseïne) werkte de variant even goed of zelfs iets beter dan normaal CTRC. Dit betekent dat de knipkracht intact is. De verrassing kwam toen ze de reactie onderzochten die het meest relevant is voor pancreatitis: het afbreken van menselijk kationisch trypsinogeen. Hier was het variantenzym veel minder effectief—ongeveer vier- tot vijfmaal langzamer in het kapotmaken van trypsinogeen en veel minder goed in het voorkomen dat trypsinogeen vanzelf activeert tot trypsine. In autoactivatie-experimenten was veel meer variant-CTRC nodig om de trypsinespiegels onder controle te houden vergeleken met het normale enzym.
Een verstoorde elektrostatische "tractorstraal"
Om te begrijpen waarom dit gebeurt, baseerden de auteurs zich op structurele modellen van CTRC. Rond de groeve waar CTRC zijn substraten vastgrijpt, bevindt zich een ring van positieve elektrische lading gevormd door meerdere geladen aminozuren, waaronder de bij p.R240Q gewijzigde positie. De regio’s van trypsinogeen die CTRC moet knippen zijn sterk negatief, zodat deze positief geladen ring fungeert als een langeafstands "tractorstraal" die trypsinogeen in de juiste positie stuurt. Door één van deze positieve plekken te neutraliseren, verzwakt de p.R240Q-variant deze verre aantrekking. Het enzym is nog steeds scherp, maar het beschadigde geleidingssysteem zorgt ervoor dat trypsinogeen niet zo efficiënt bindt, waardoor er minder veilig wordt afgebroken. Andere substraten die niet zo sterk afhankelijk zijn van dit ladingspatroon worden normaal verwerkt, wat de zeer selectieve defecten verklaart die in de experimenten werden gezien.
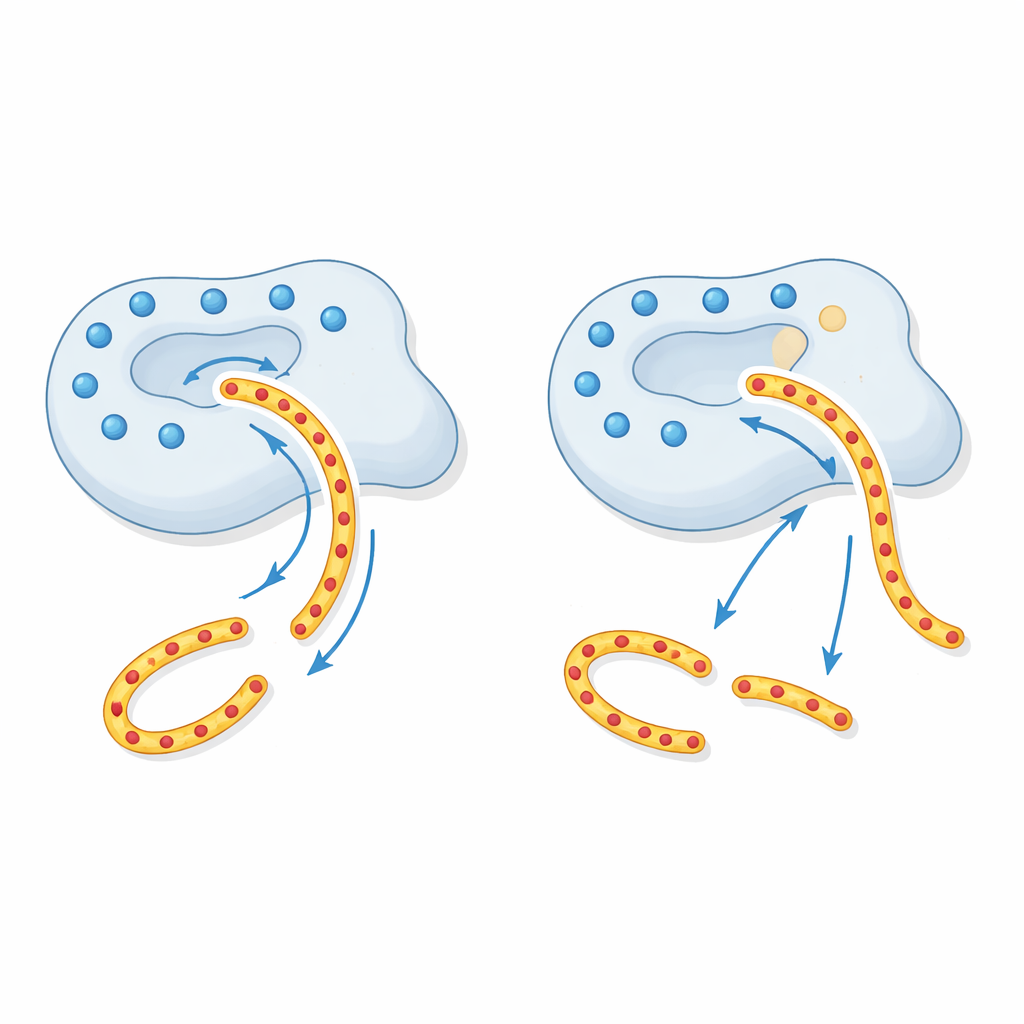
Wat dit betekent voor patiënten en testen
Klinisch droegen zowel de aangedane jongen als zijn vader een tweede schadelijke CTRC-variant, en de vader had aanvullende risicofactoren in zijn levensstijl, zoals zwaar alcoholgebruik. Dit past bij het idee dat chronische pancreatitis vaak het gevolg is van meerdere gecombineerde genetische en omgevingsfactoren. Het werk toont aan dat een variant die onschadelijk lijkt volgens algemene voorspellingshulpmiddelen toch op een zeer specifieke manier gevaarlijk kan zijn. Voor genetische testing is de boodschap duidelijk: bij het beoordelen of een CTRC-variant het pancreatitisrisico verhoogt, moeten wetenschappers het testen op het echte doelmolecuul, trypsinogeen, en niet alleen op generieke laboratoriumsubstraten. In gewone bewoordingen laat deze studie zien hoe een kleine verandering in het "geleidingsoppervlak" van het enzym stilletjes één van de belangrijke beveiligingssloten van de alvleesklier kan ondermijnen en vatbare personen naar chronische ontsteking kan duwen.
Bronvermelding: Nagy, Z.A., Sándor, M., Hegyi, E. et al. Pancreatitis-associated chymotrypsin C (CTRC) variant p.R240Q selectively impairs trypsinogen degradation through disruption of long-range electrostatic interactions. Sci Rep 16, 8937 (2026). https://doi.org/10.1038/s41598-026-40633-0
Trefwoorden: chronische pancreatitis, chymotrypsine C, trypsinogeen, genetische variant, spijsverteringsenzymen