Clear Sky Science · nl
Laag-affiniteitsbinding van anti-B7-H3 kloon MJ18 aan muizen B7-H3 faalt in het induceren van tumorreductie
Waarom dit belangrijk is voor kankeronderzoek
Kankerimmunotherapie berust vaak op antilichamen—laboratoriumgemaakte eiwitten die zich aan tumorcellen binden en het immuunsysteem helpen deze te vernietigen. Een veelbelovende doelmolecule is B7-H3, die overvloedig aanwezig is op veel menselijke kankers maar schaars op gezonde weefsels. Dit artikel onderzoekt kritisch een veelgebruikt onderzoeksantilichaam, MJ18, dat verondersteld werd B7-H3 in muizen te blokkeren. De auteurs vinden dat MJ18 nauwelijks aan zijn beoogde target hecht en de tumorgroei niet vertraagt, wat vragen oproept over de interpretatie van eerdere dierstudies die dit middel gebruikten.
De belofte van een kankervlag op tumorcellen
B7-H3 trok veel aandacht omdat het fungeert als een moleculair schild: tumoren met veel van dit eiwit hebben doorgaans minder agressieve immuuncellen in hun weefsel en worden geassocieerd met slechtere uitkomsten voor patiënten. In verschillende muismodellen leidt het verwijderen van het B7-H3-gen in tumorcellen tot een sterkere immuunreactie en kan dit tumoren laten krimpen of verdwijnen. Deze observaties hebben inspanningen aangespoord om geneesmiddelen, gemanipuleerde immuuncellen en antilichaam–drugconjugaten te ontwikkelen die zich richten op B7-H3 op menselijke kankers. Toch blijft de precieze manier waarop B7-H3 de immuniteit dempt—en zelfs welke receptor het aanspreekt op immuuncellen—onzeker, vooral omdat de muis- en menselijke vormen van B7-H3 structureel van elkaar verschillen.
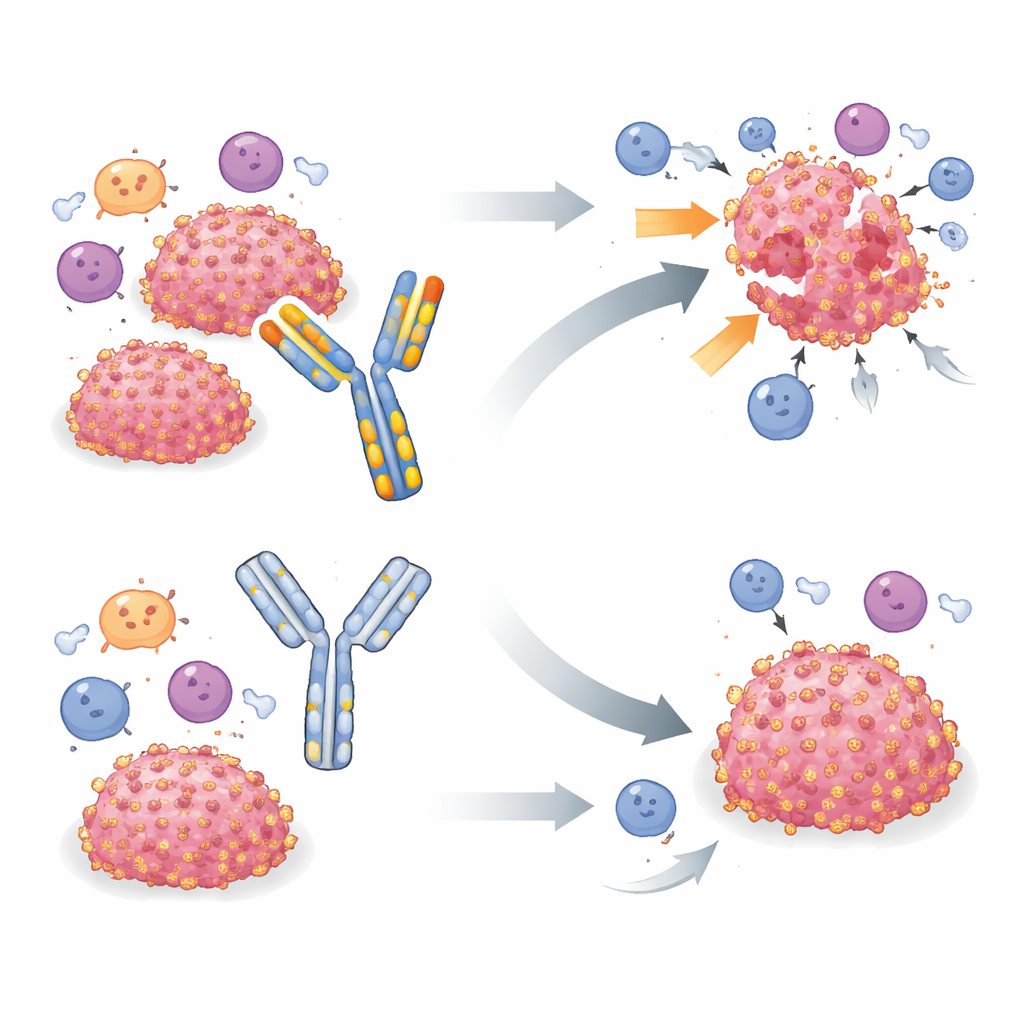
Een veelgebruikt hulpmiddel onder de loep
Om B7-H3 in levende muizen te bestuderen, hebben veel groepen vertrouwd op een enkel rat-afgeleid antilichaam genaamd MJ18, waarvan werd gerapporteerd dat het muizen B7-H3 herkent en diens immuunsuppressieve werking blokkeert. Eerdere studies met MJ18 in diverse ziektemodellen, waaronder kanker, rapporteerden vaak tragere tumorgroei en betere overleving. Het huidige team probeerde MJ18 aanvankelijk in een muismodel van rhabdomyosarcoom, een kinderkanker van zacht weefsel waarbij B7-H3 eerder als een belangrijk ontsnappingsmechanisme werd aangemerkt. Toen MJ18 geen verbetering van tumorcontrole gaf, breidden de onderzoekers hun testen uit naar twee andere B7-H3-positieve tumortypes—pancreas- en mammatumoren—die duidelijk gevoelig zijn voor verwijdering van het B7-H3-gen. In alle drie de modellen vertraagde of elimineerde het uitzetten van B7-H3 in tumorcellen de tumoren sterk, maar behandeling van muizen met MJ18 bij doseringen en schema’s vergelijkbaar met die in de literatuur had geen detecteerbaar effect op tumorgroei of overleving.
Testen of MJ18 echt zijn doel raakt
De auteurs stelden vervolgens een fundamentele vraag die verrassend genoeg nooit rigoureus was aangepakt: bindt MJ18 werkelijk aan muizen B7-H3, en hoe sterk? Met flowcytometrie vergeleken ze MJ18 met een ander antilichaam, EPNCIR122, dat bekendstond B7-H3 te detecteren. Op meerdere muizen tumorcellijnen gaf EPNCIR122 een duidelijk signaal dat verdween wanneer het B7-H3-gen werd uitgeschakeld, wat de specificiteit bevestigde. MJ18 daarentegen toonde geen overtuigende binding, zelfs niet bij hoge concentratie. Bij onderzoek van immuuncellen uit de milt week MJ18 wel binding, maar het patroon kwam niet overeen met B7-H3, en EPNCIR122 detecteerde helemaal geen B7-H3 op deze cellen, wat suggereert dat MJ18 zich aan iets anders hechtte.
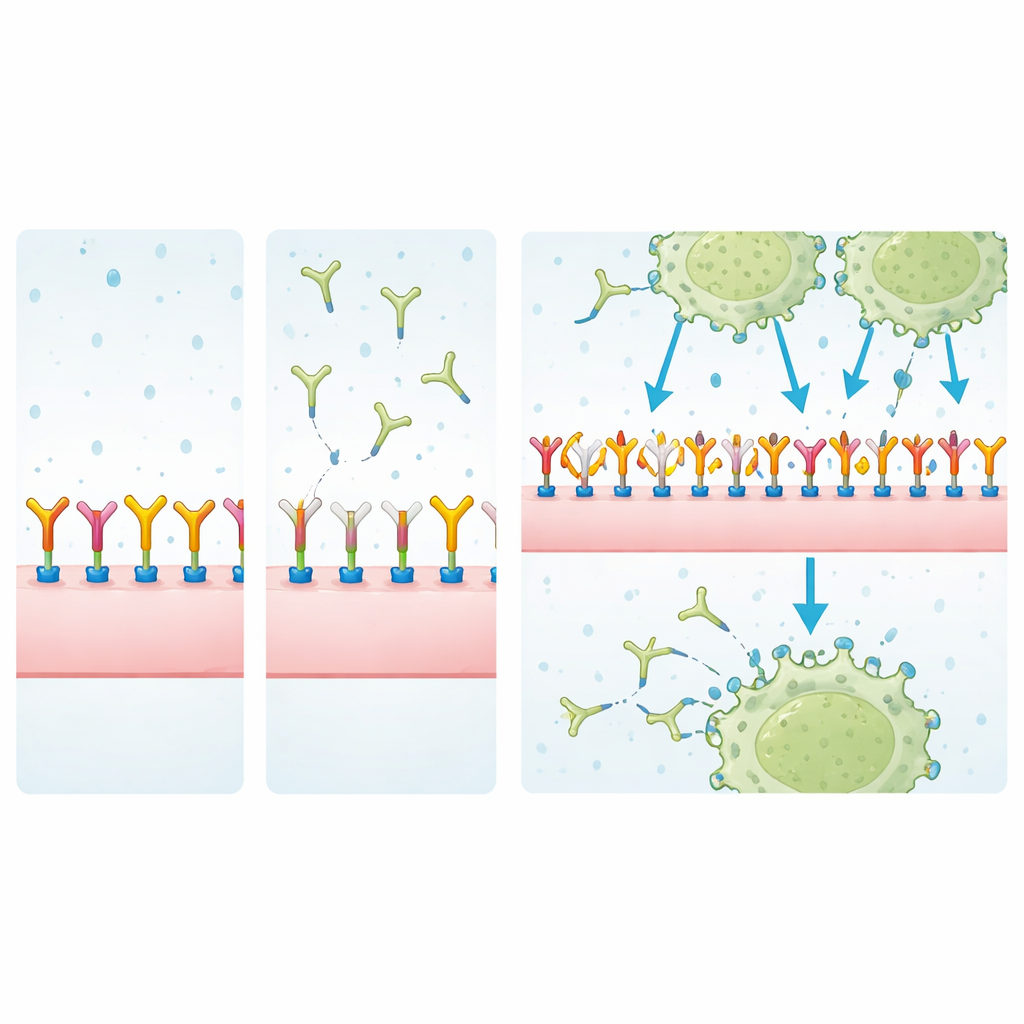
Dieper graven naar de bindingspartners
Om te identificeren wat MJ18 mogelijkerwijs werkelijk herkent, trokken de onderzoekers celoppervlakte-eiwitten naar beneden met MJ18 of EPNCIR122 en analyseerden die met massaspectrometrie, terwijl ze veelvoorkomende achtergrondcontaminanten wegfilterden. In tumorcellen verrijkte EPNCIR122 sterk voor B7-H3 boven andere eiwitten, wat bevestigt dat het een zeer specifiek reagens is. MJ18 trok echter een mix van eiwitten mee waarbij B7-H3 slechts zwak aanwezig was en op niveaus die vergelijkbaar waren met niet-specifieke binders. Metingen met oppervlaktespron-resonantie, een gevoelige techniek om moleculaire interacties te kwantificeren, zetten de zaak kracht bij: de affiniteit van MJ18 voor muizen B7-H3 was ruwweg 7.000 keer zwakker dan die van EPNCIR122—ver onder wat gebruikelijk is voor therapeutische antilichamen.
Wanneer antilichamen door de verkeerde cellen worden gegrepen
Het verhaal eindigde niet bij zwakke binding. In miltcellen toonden aanvullende tests aan dat MJ18 en soortgelijke ratantilichamen werden herkend door muis Fc-receptoren—moleculen op immuuncellen die van nature het staartdeel van antilichamen binden. Het blokkeren van deze receptoren verminderde het MJ18-signaal sterk, wat impliceert dat veel van de schijnbare binding voortkwam uit immuuncellen die het antilichaam zelf grepen, in plaats van dat MJ18 een specifiek celoppervlakte-eiwit targette. Pogingen om een uniek eiwitpartner voor MJ18 op immuuncellen aan te wijzen leverden alleen kandidaten op die op niveaus zaten die niet te onderscheiden waren van achtergrondruis. Al met al suggereren de gegevens dat MJ18 zich gedraagt als een veelal laag-affiniteit, niet-specifiek antilichaam waarvan de interacties worden gedomineerd door Fc-receptorbinding in plaats van precieze herkenning van B7-H3.
Wat dit betekent voor de toekomst
Voor niet-specialisten is de kernboodschap helder: hoewel B7-H3 een overtuigend doelwit blijft op veel kankers, is het MJ18-antilichaam geen betrouwbare pijl. Het bindt B7-H3 in muizen slechts zwak en reproduceert niet de krachtige tumorcontrole die wordt gezien wanneer het B7-H3-gen wordt verwijderd. Eerdere muisstudies die dramatische voordelen met MJ18 rapporteerden, kunnen daarom andere effecten reflecteren—zoals hoe de staart van het antilichaam immuuncelreceptoren aantrekt—in plaats van een werkelijke blokkade van B7-H3. De auteurs betogen dat het veld met urgentie goed-geverifieerde, hoog-affinitaire antilichamen tegen muizen B7-H3 nodig heeft, en dat onderzoekers routinematig de specificiteit en sterkte van dergelijke tools moeten bevestigen. Alleen met betrouwbare reagentia kunnen inzichten uit diermodellen worden vertrouwd om de ontwikkeling van de volgende generatie B7-H3–gerichte therapieën voor patiënten te begeleiden.
Bronvermelding: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Trefwoorden: B7-H3, kankerimmunotherapie, validatie van antilichamen, immuuncheckpoints, tumormodellen