Clear Sky Science · nl
Grote variaties in totale en allelspecifieke transcriptexpressie onafhankelijk van ziekteveroorzakende mutatie
Waarom dit van belang is voor mensen met cystische fibrose
Cystische fibrose (CF) wordt vaak beschreven als een klassiek "één-gen"-ziekte, maar mensen met precies dezelfde mutatie kunnen opvallend verschillende symptomen en levenspaden hebben. Deze studie stelt een ogenschijnlijk eenvoudige vraag met verstrekkende gevolgen: zelfs wanneer het defecte gen hetzelfde is, maken patiënten dan daadwerkelijk verschillende hoeveelheden van het genbericht aan, en kan dat helpen verklaren waarom hun ziekte zo verschillend verloopt — en hoe goed ze reageren op moderne medicijnen?
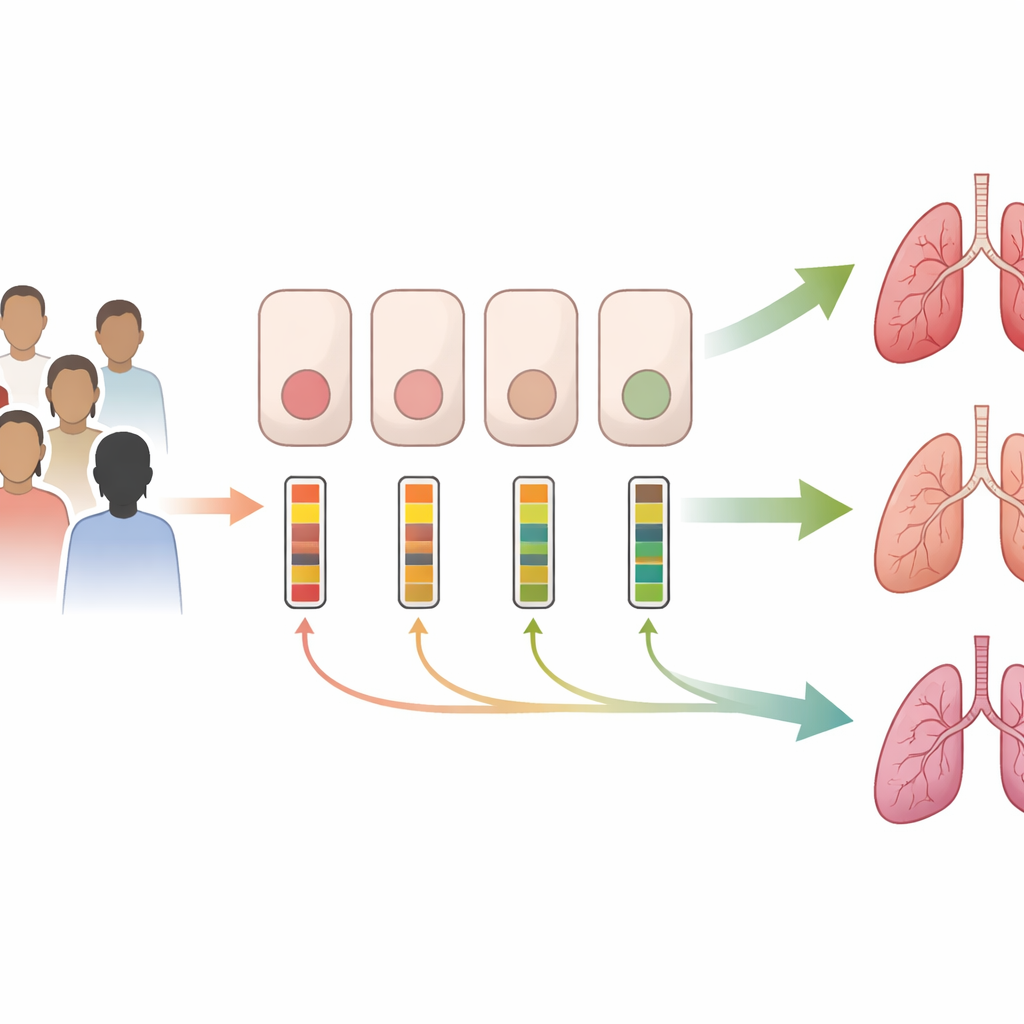
Verschillende patiënten, dezelfde mutatie, heel verschillende genactiviteit
De onderzoekers concentreerden zich op het CFTR-gen, waarvan defecte varianten CF veroorzaken. In plaats van alleen naar DNA-veranderingen te kijken, maten ze hoeveel CFTR-messenger RNA (mRNA) — het werkende "script" van het gen om eiwit te maken — aanwezig is in luchtwegcellen die zijn verkregen met zachte neusswabs. Over vijf jaar verzamelden ze monsters van kinderen en volwassenen met CF, en een kleine groep zonder CF. Veel patiënten droegen de veelvoorkomende F508del-mutatie, hetzij op beide genkopieën, hetzij op één kopie gecombineerd met een andere fout. Zelfs binnen deze groepen varieerden de CFTR-mRNA-niveaus sterk — meerdere keren verschil van persoon tot persoon. Gezonde vrijwilligers vertoonden ook brede variatie, wat erop wijst dat CFTR-expressie van nature tussen individuen verschilt en dat deze ingebouwde variabiliteit ook bij CF doorwerkt.
Als de twee genkopieën niet gelijk bijdragen
Voor patiënten die twee verschillende CFTR-mutaties droegen — één F508del en één andere variant — ging het team een stap verder. Met zeer specifieke moleculaire tests telden ze hoeveel mRNA van elke genkopie afzonderlijk afkomstig was. In plaats van dat elk allel ongeveer de helft van het totaal bijdroeg, vonden ze vaak een sterke scheefheid, of "skewing": het niet-F508del-allel produceerde doorgaans veel meer mRNA dan het F508del-allel. Bij sommige patiënten droeg de F508del-kopie slechts een klein deel van het totale CFTR-bericht bij. Deze ongelijke output trad zelfs op onder mensen met hetzelfde paar mutaties, wat erop wijst dat aanvullende DNA-veranderingen nabij het gen, of bredere regulerende mechanismen, bepalen hoeveel boodschap elke kopie produceert.
Celstudies bevestigen ingebouwde variabiliteit
Om enkele van de reële complicaties door infecties en ontsteking in de luchtwegen uit te sluiten, lieten de wetenschappers ook neus- en bronchiële cellen van patiënten in het laboratorium groeien. Ook daar detecteerden ze grote verschillen in de totale CFTR-mRNA-niveaus tussen personen met dezelfde genetische achtergrond. In een subset van gekweekte cellen van compound-heterozygote patiënten was de expressie van de twee allelen dichter bij evenwicht dan in verse neussamples, wat onderstreept hoe kweekomstandigheden en de omgeving van het lichaam genactiviteit kunnen veranderen. Samen ondersteunen deze observaties het idee dat zowel de totale CFTR-output als de relatieve bijdrage van elk allel flexibele eigenschappen zijn, en niet uitsluitend worden bepaald door de DNA-sequentie van de hoofdmutaties.
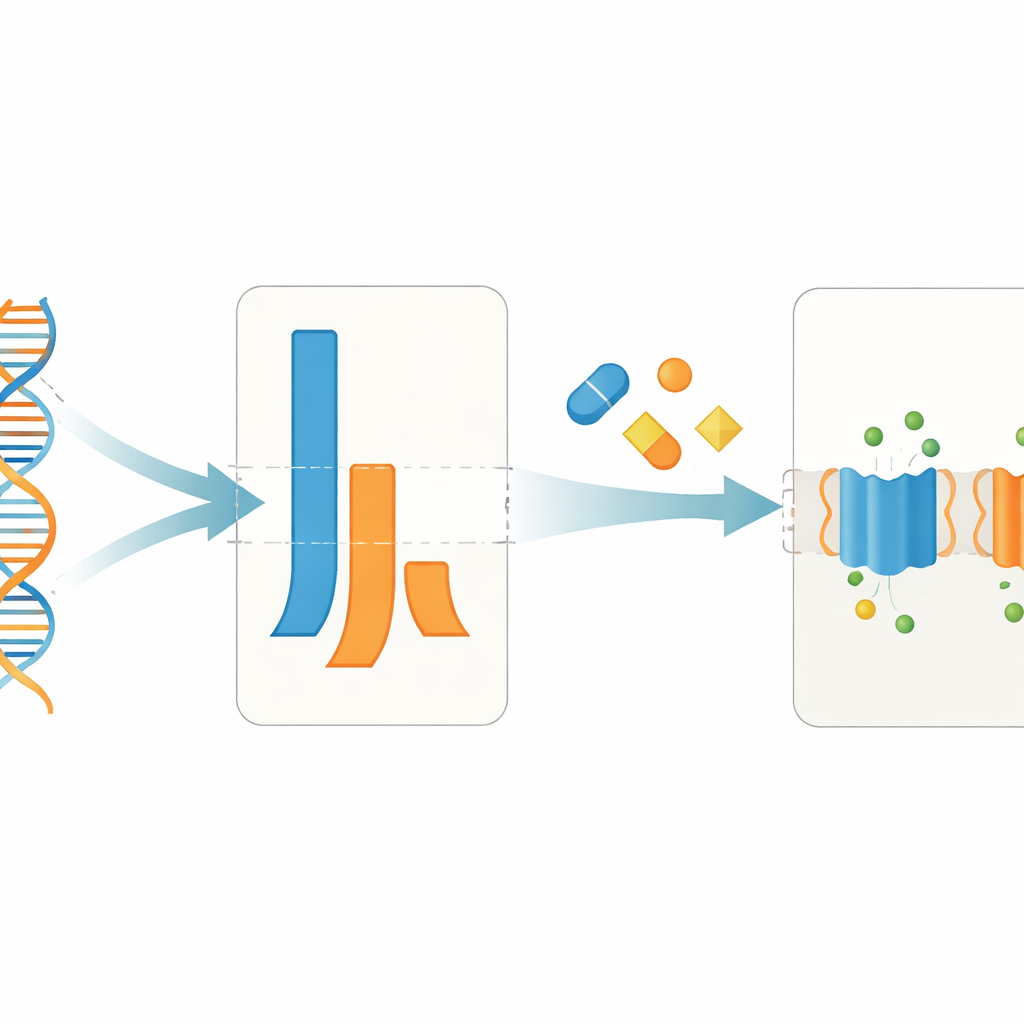
Moderne CF-medicijnen verschuiven het evenwicht tussen genkopieën
De studie onderzocht ook een kleine groep patiënten vóór en na het starten van veelgebruikte CFTR-"modulatortherapieën", inclusief de drievoudige combinatie elexacaftor–tezacaftor–ivacaftor en een tweedrugsregime. Verrassend genoeg verhoogden of verlaagden deze medicijnen niet consistent de totale hoeveelheid CFTR-mRNA in neuscellen. In plaats daarvan verschoven ze welke allel meer bijdroeg. Na behandeling produceerde het F508del-allel vaak een groter aandeel van het totale CFTR-bericht en werd het in sommige gevallen de dominante bron. Deze verandering in allelbalans trad op naast de verwachte klinische verbeteringen, zoals betere longfunctie en lagere zweetzoutwaarden, wat suggereert dat het verhogen van de boodschapproductie uit een hersteld mutant eiwit de bekende effecten van de medicijnen op vouwing en functie van het eiwit kan aanvullen.
Wat dit betekent voor gepersonaliseerde behandeling
Voor mensen met cystische fibrose benadrukken deze bevindingen dat DNA-mutaties slechts een deel van het verhaal vertellen. Hoeveel CFTR-mRNA iemand aanmaakt — en hoe die productie verdeeld is tussen de twee genkopieën — kan sterk variëren en op manieren die niet door het mutatietype alleen worden voorspeld. Deze variatie kan helpen verklaren waarom patiënten met hetzelfde genotype verschillende ziekte-ernst en uiteenlopende therapieresponsen hebben. Het suggereert ook dat toekomstige gepersonaliseerde benaderingen mogelijk moeten meten niet alleen welke CFTR-mutaties iemand draagt, maar ook hoe actief elke kopie van het gen wordt gebruikt, zowel vóór als tijdens behandeling. Het begrijpen en uiteindelijk beheersen van deze verborgen laag van genactiviteit kan helpen therapieën voor CF en andere één-gen-ziekten te verfijnen.
Bronvermelding: Freyberg, M., Bewig, M., Bampi, G.B. et al. Large variations in total and allele-specific transcript expression in a disease mutation-independent manner. Sci Rep 16, 7831 (2026). https://doi.org/10.1038/s41598-026-40624-1
Trefwoorden: cystische fibrose, CFTR, genexpressie, allelonevenwicht, CFTR-modulatoren