Clear Sky Science · nl
Theoretische analyse van laag-vermogen optogenetische onderdrukking van actiepotentialen in humane ventriculaire cardiomyocyten die kalium-selectieve channelrhodopsines tot expressie brengen
Een zachtere, lichtgebaseerde manier om een hardlopend hart te kalmeren
Snel en chaotisch hartritme kan flauwvallen, beroerte of plotselinge dood veroorzaken. De huidige behandelingen — krachtige medicijnen, geïmplanteerde defibrillatoren of schokken met hoge energie — kunnen levensreddend zijn maar ook pijnlijk en onnauwkeurig. Deze studie onderzoekt een heel ander idee: het gebruik van zwakke lichtflitsen en speciaal ontworpen eiwitten om hartcellen geruisloos terug te geleiden naar een veilige, stabiele ritme, en daarbij veel minder energie te verbruiken dan bij bestaande methoden.
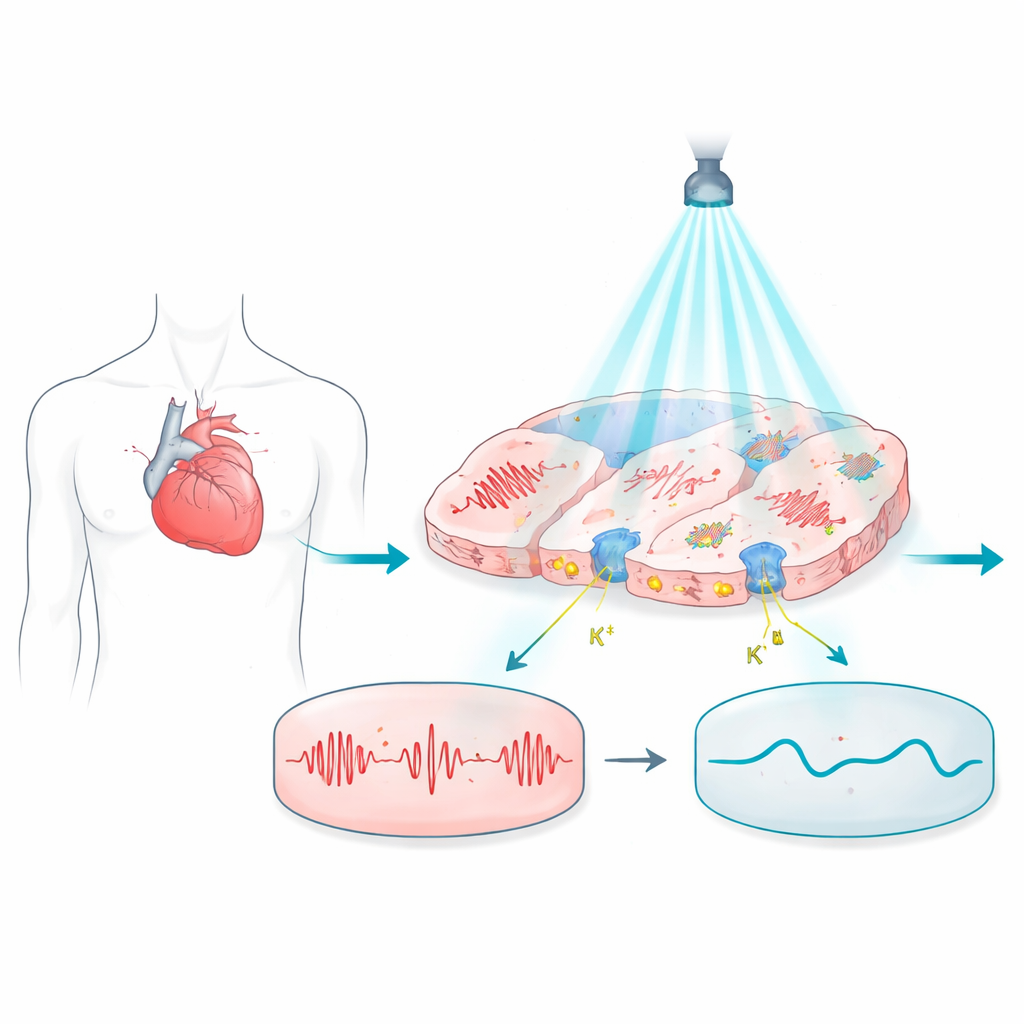
Het licht laten schijnen op probleemslagen
Het werk bouwt voort op optogenetica, een techniek waarbij cellen worden uitgerust met lichtgevoelige eiwitten zodat hun elektrische activiteit met lichtflitsen kan worden gestuurd. In het hart kunnen deze eiwitten in principe metalen elektroden vervangen en contactloze, pijnvrije controle bieden. Maar de meeste tot nu gebruikte lichtgestuurde eiwitten duwen de membraanpotentiaal naar boven, naar een geprikkelde toestand, wat het moeilijk maakt cellen rustig in rust te houden of de duur van elke hartslag precies bij te stellen. Dat beperkt hun bruikbaarheid voor het veilig uitschakelen van gevaarlijke ritmes of het corrigeren van elektrische stoornissen die afhangen van subtiele timing.
Nieuwe lichtschakelaars afgestemd op de hart"ruststand"
Onlangs ontdekte eiwitten, kalium-selectieve channelrhodopsines zoals WiChR en HcKCR1, beloven dit probleem te verhelpen. In tegenstelling tot oudere eiwitten die een mengsel van geladen deeltjes doorlaten, geven deze kanalen sterk de voorkeur aan kalium en trekken ze de membraanpotentiaal natuurlijk richting hetzelfde negatieve niveau dat de cel in rust zou aannemen. De auteurs bouwden gedetailleerde computermodellen van humane ventriculaire hartcellen die deze nieuwere kanalen tot expressie brengen en vergeleken die met twee bekende, meer exciterende opsines, ChR2(H134R) en ChRmine. Door te simuleren hoe deze cellen reageren op verschillende kleuren en intensiteiten van licht, konden ze veilig condities verkennen die moeilijk of tijdrovend in echte harten te testen zouden zijn.
Zacht licht, sterke controle
De simulaties laten zien dat kalium-selectieve kanalen veel zuiniger en stabieler controleren. Vooral WiChR kon actiepotentialen — de kortdurende elektrische pieken die elke hartslag triggeren — volledig uitschakelen met lichtintensiteiten die honderden tot duizenden keren lager liggen dan die nodig zijn voor veel eerdere instrumenten. Onder continu licht hielden WiChR en HcKCR1 de membraanpotentiaal dicht bij het normale rustniveau en hielden zo de cel in een rustige, veilige toestand. Daartegenover duwden ChR2 en ChRmine de potentiaal vaker naar meer positieve waarden, soms met blokkade van activiteit, maar dan meestal pas nadat de cel in een gestreste, overgeprikkelde toestand was gedwongen. WiChR werkte ook goed met korte lichtpulsen en voorkwam betrouwbaar hartcelspikes slag na slag, wat suggereert dat het snelle hartritmes kan bijhouden zonder weefsel te oververhitten of energie te verspillen.
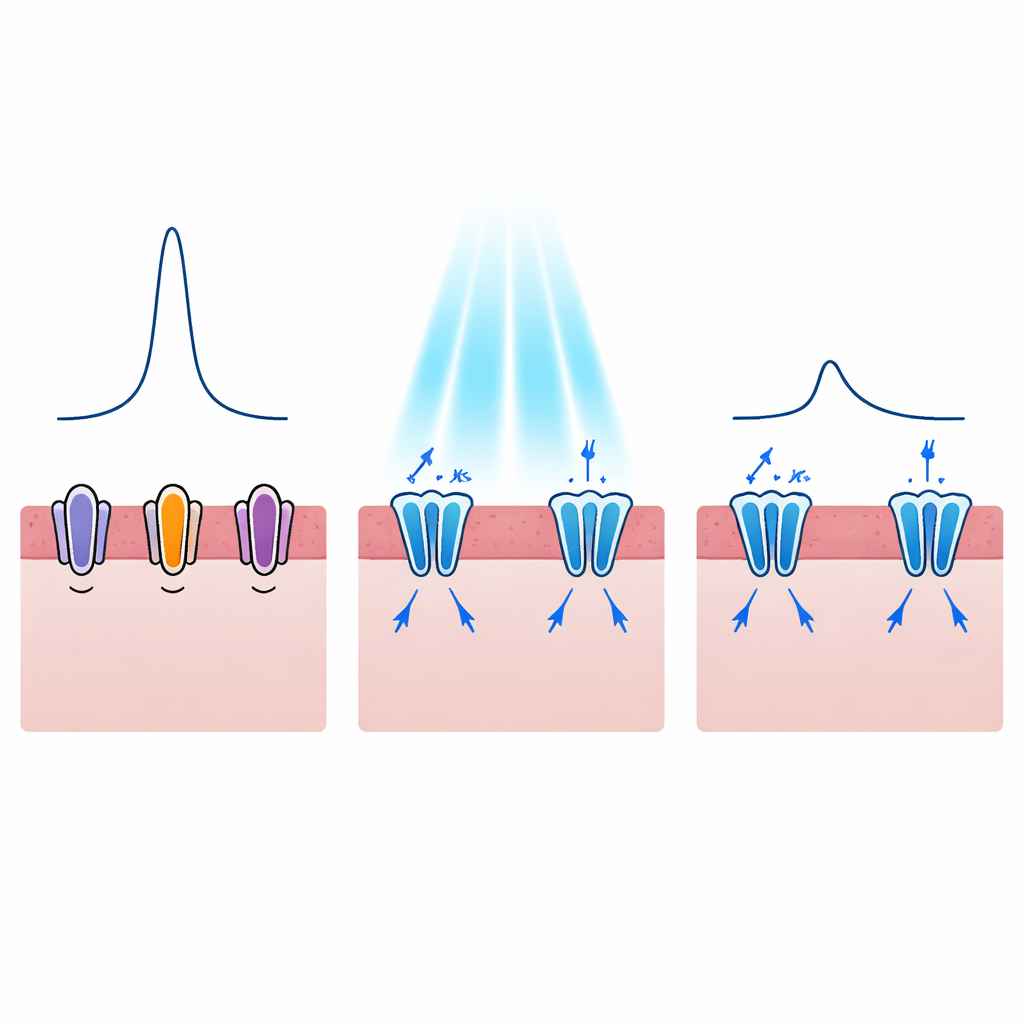
Elke hartslag hervormen, niet alleen stoppen
Gevaarlijke aritmieën hangen vaak niet alleen samen met of een hartcel vuurt, maar ook met hoe lang die cel geprikkeld blijft. Bij aandoeningen zoals het lang QT-syndroom is de elektrische puls van elke slag verlengd, wat de kans op overgaan in fatale ritmes vergroot. De auteurs vroegen zich daarom af of lichtgeactiveerde kaliumkanalen deze puls op een gecontroleerde manier konden verkorten. Hun modellen toonden aan dat het inschakelen van WiChR of HcKCR1 tijdens het plateau van het actiepotentiaal sterke naar buiten gerichte kaliumstromen veroorzaakte die de potentiaal sneller terugtrokken. Naarmate het lichtniveau toenam, daalde de duur van de elektrische puls van ongeveer 300 milliseconden tot grofweg de helft, en dit effect kon al met zeer korte lichtflitsen worden bereikt. WiChR neigde ertoe langere stilteperioden te produceren, terwijl HcKCR1 snellere herstelmomenten bood zodra het licht uitging, wat wijst op verschillende potentiële klinische toepassingen.
Van computermodellen naar toekomstige therapieën
Al met al concluderen de onderzoekers dat kalium-selectieve lichtgestuurde kanalen, met name WiChR, veelbelovende middelen zijn voor zachte, laagvermogencontrole van het hart. Ze kunnen zowel weggelopen elektrische activiteit stilleggen als te lange hartslagen inkorten, terwijl ze de membraanpotentiaal dicht bij de natuurlijke rust houden. Hoewel de resultaten voortkomen uit gedetailleerde simulaties van enkele cellen in plaats van experimenten op het hele hart, bieden ze kwantitatieve aanwijzingen over hoe veel licht nodig kan zijn, wanneer het moet worden toegepast en welke eiwitvarianten het beste geschikt zijn voor verschillende doelen. Op de lange termijn wijst dit werk in de richting van een toekomst waarin cardiologen fijn afgestelde lichtbundels gebruiken in plaats van pijnlijke schokken om levensbedreigende aritmieën te voorkomen of te stoppen.
Bronvermelding: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Trefwoorden: cardiale optogenetica, onderdrukking van aritmieën, kalium-channelrhodopsines, duur van actiepotentiaal, lang QT-syndroom