Clear Sky Science · nl
In ovo sexing en genotypering met PCR-technieken: een bijdrage aan de 3R-principes in de kippenfokkerij
Waarom wat er binnenin een ei gebeurt ertoe doet
Elk jaar worden miljoenen hanenk kuikens kort na het uitkomen gedood omdat ze niet bruikbaar zijn voor de eierproductie. Tegelijkertijd brengen onderzoekslaboratoria wereldwijd meer dieren uit dan ze eigenlijk nodig hebben, simpelweg omdat ze het geslacht of de genetische samenstelling van een embryo niet vroeg genoeg kunnen bepalen. Deze studie presenteert een praktische methode om het geslacht en de genen van een kuiken af te lezen terwijl het zich nog in het ei ontwikkelt, met behulp van standaard DNA-tests. Door dit vroeg en voorzichtig te doen, heeft de methode tot doel overbodige uitkomst te voorkomen en lijden te verminderen, zonder dat dure industriële apparatuur nodig is.
In het ei kijken zonder het te openen
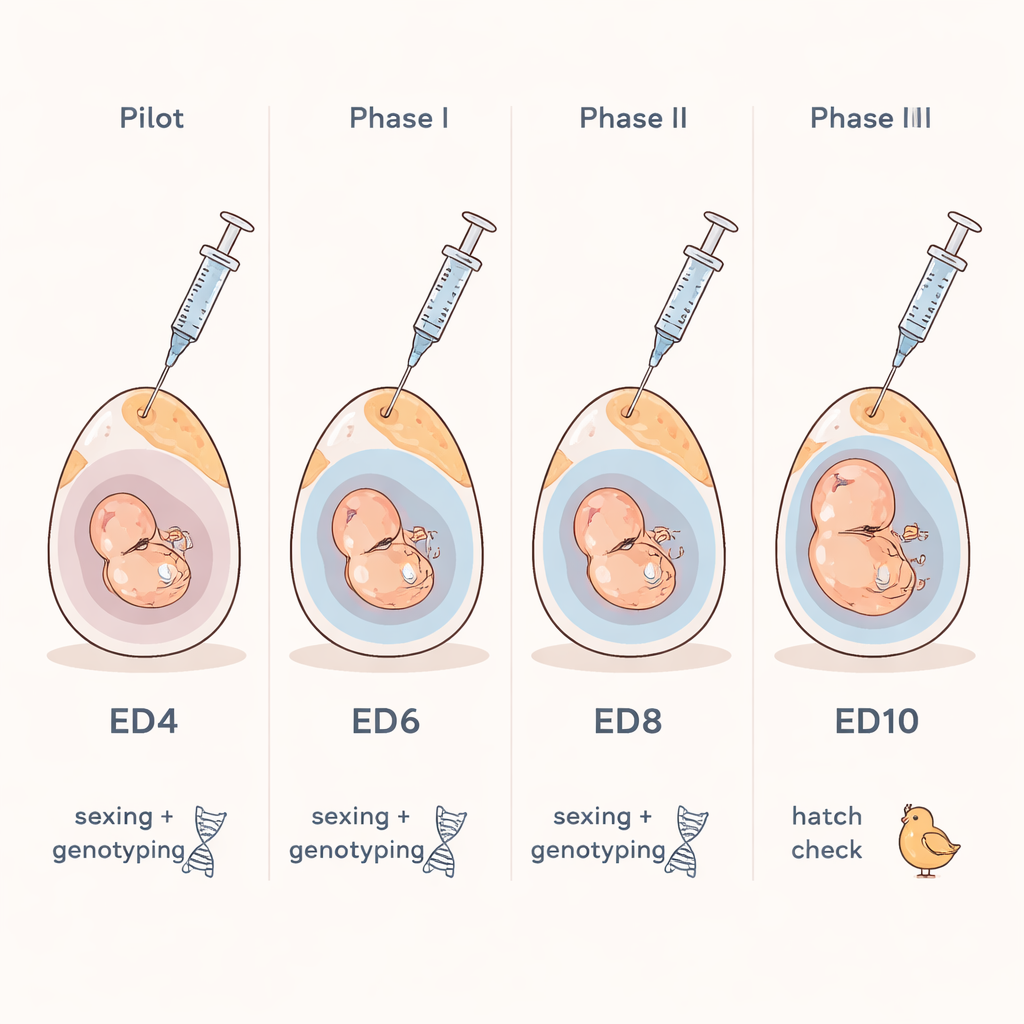
De onderzoekers richtten zich op een eenvoudige vraag: kunnen we veilig een minuscuul vloeistofmonster uit een bevrucht kippenei nemen en daarmee het geslacht en belangrijke genetische eigenschappen van het embryo identificeren? Ze bouwden voort op een concept dat bekend is uit de menselijke geneeskunde, waar artsen het vruchtwater rond een foetus testen op genetische aandoeningen. Bij kippen vormt zich een dun, met vocht gevulde zak, de allantois, rond het embryo naarmate het groeit. Op dag zeven van de incubatie bevat deze zak voldoende vocht zodat een fijne naald hem kan bereiken zonder het embryo zelf te raken. Het team gebruikte een helder licht om de luchtkamer aan het stompe uiteinde van het ei te lokaliseren, maakte een poriëngroot gaatje in de schaal en trok met een kleine spuit slechts een paar druppels vloeistof eruit.
Van een paar druppels naar een genetische vingerafdruk
De vloeistof die vroeg in de ontwikkeling uit eieren wordt gehaald bevat slechts minuscule hoeveelheden DNA. Om dit te omzeilen versterkten de wetenschappers eerst al het genetische materiaal in elk monster, waarbij ze vele kopieën maakten zonder de inhoud te veranderen. Daarna pasten ze twee routinematige laboratoriumtests toe: een standaard polymerasekettingreactie (PCR) en een variant genaamd Kompetitive Allele Specific PCR (KASP). Beide tests kunnen onderscheid maken tussen de geslachtschromosomen van mannelijke en vrouwelijke kuikens en kunnen ook specifieke genetische markers detecteren, zoals de mutatie die blauwe eierschalen veroorzaakt of de aanwezigheid van een in het laboratorium ingebracht gen in gespecialiseerde onderzoekslijnen. Over meer dan 800 eieren van verschillende rassen—waaronder commerciële leglijnen, kleurige Araucana-kruisingen en een genetisch gemodificeerde onderzoekslijn—leidden deze methoden in ongeveer 92–100% van de gevallen tot correcte identificaties.
Het veiligste moment voor bemonstering vinden
Te vroeg bemonsteren brengt het risico mee dat kwetsbare structuren die essentieel zijn voor het embryo beschadigd worden, terwijl te laat bemonsteren weinig tijd laat om op de resultaten te reageren. Om het ideale tijdvenster vast te stellen, kweekte het team eerst embryo’s in een schaal-loze cultuur om te observeren hoe de membranen en vloeistofruimten zich in de tijd uitbreiden. Vervolgens voerden ze een reeks gestage proeven uit in intacte eieren. Vloeistof kon vanaf dag vier worden verzameld, maar de succeskansen voor DNA-tests waren in die vroege dagen lager en de procedure was technisch moeilijker. Toen ze de uitkomstpercentages tussen geprikte en ongemoeide controleeieren vergeleken, bleek dag zeven de beste balans te bieden: er was voldoende heldere allantoïsvloeistof, DNA-tests werkten betrouwbaar en de meeste embryo’s overleefden het uitkomen. Op dit punt is er nog enkele dagen tijd vóór de waarschijnlijke aanvang van pijnwaarneming bij het kuikenembryo, wat een ethische buffer biedt voor beslissingen.
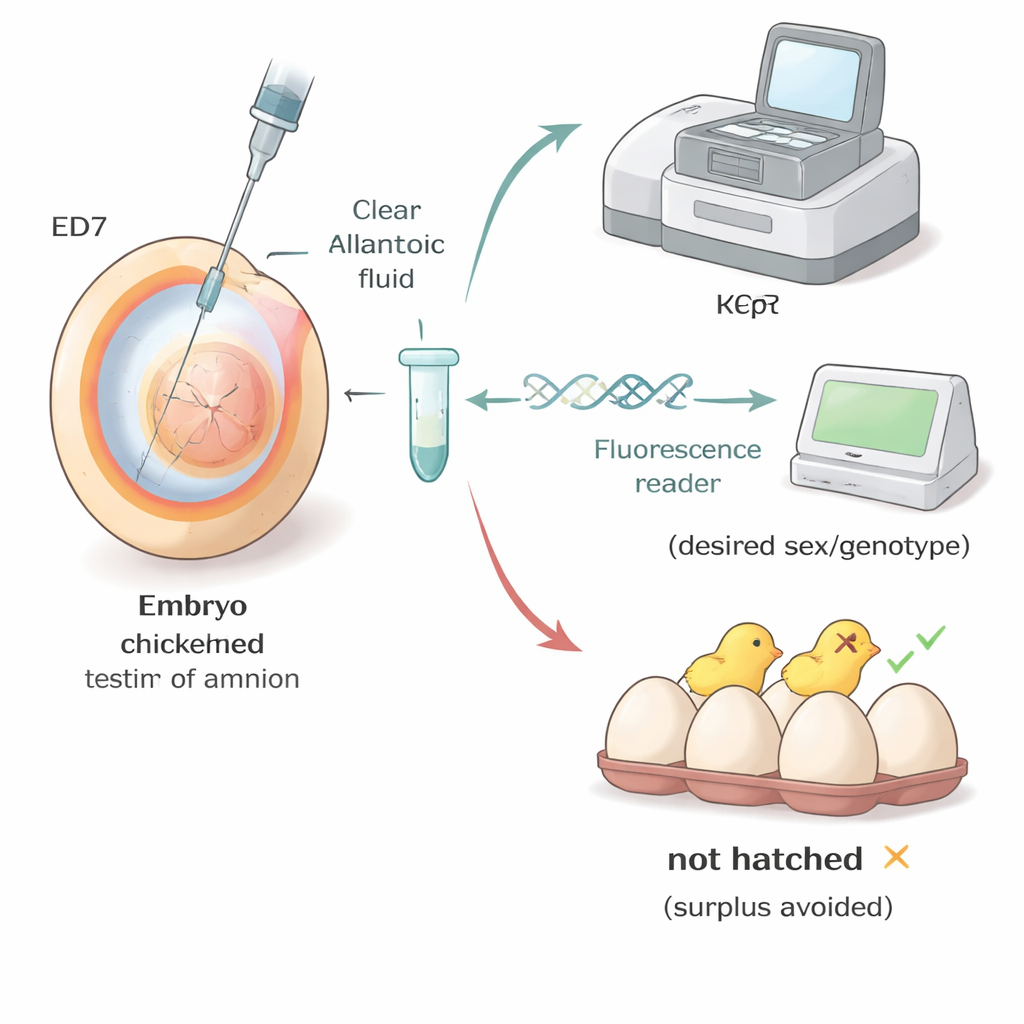
De methode toepassen in echte kassen
De onderzoekers hebben hun workflow getest onder omstandigheden die vergelijkbaar zijn met die in fokfaciliteiten en universiteitslaboratoria. Bij commerciële bruine en witte leglijnen lieten eieren die tussen dag vier en zeven werden bemonsterd zien dat de uitkomstbaarheid over het algemeen verbeterde wanneer bemonstering later plaatsvond, met wederom de beste resultaten op dag zeven. In een gespecialiseerde "surrogaatgastheer"-lijn die wordt gebruikt voor geavanceerde genetica ging het team nog een stap verder: ze bepaalden op dag zeven zowel het geslacht als het genotype van embryo’s en lieten alleen die met de gewenste geslachts- en genetische combinatie uitkomen. Bijna alle geselecteerde embryo’s kwamen uit tot gezonde kuikens die naar verwachting groeiden, wat aantoont dat vroege selectie het aantal ongewenste dieren aanzienlijk kan verminderen zonder de kwaliteit van de kuikens aan te tasten.
Wat dit betekent voor dierwelzijn en onderzoek
Voor een niet‑specialist is de kernboodschap helder: met een speldenprik en routinematige labmiddelen is het nu mogelijk om, terwijl het kuiken nog veilig in het ei zit, te weten of het mannelijk of vrouwelijk is en of het bepaalde genetische kenmerken draagt. De studie toont aan dat dit rond dag zeven van de incubatie zowel technisch betrouwbaar is als voorzichtig genoeg dat de meeste embryo’s overleven. Door ongewenste embryo’s te verwijderen voordat ze waarschijnlijk pijn kunnen voelen, ondersteunt de aanpak de breed geaccepteerde 3R-principes: vervangen, verminderen en verfijnen van het gebruik van dieren in de wetenschap. Voor broederijen en onderzoekslaboratoria biedt deze techniek een realistisch pad naar minder overtollige dieren, efficiënter gebruik van middelen en hogere welzijnsnormen—zonder de noodzaak van complexe industriële machines.
Bronvermelding: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Trefwoorden: kuikenembryo, in ovo seksering, PCR-genotypering, dierwelzijn, 3R-principes