Clear Sky Science · nl
Genomische karakterisering van multiresistente Escherichia coli-stammen geïdentificeerd bij patiënten met urineweginfecties in Egypte
Waarom deze hardnekkige infecties ertoe doen
Urineweginfecties behoren tot de meest voorkomende redenen voor ziekenhuis- en kliniekbezoeken. Veel worden veroorzaakt door de bacterie Escherichia coli en zijn doorgaans behandelbaar met standaardantibiotica. Maar wereldwijd, ook in Egypte, zijn sommige E. coli-stammen zo resistent geworden dat artsen steeds minder behandelingsopties hebben. Deze studie bekijkt genetisch nauwkeurig twee van zulke moeilijk te behandelen stammen van Egyptische patiënten om te begrijpen hoe ze meerdere geneesmiddelen ontwijken en hoe gemakkelijk hun resistentie zich mogelijk verspreidt.
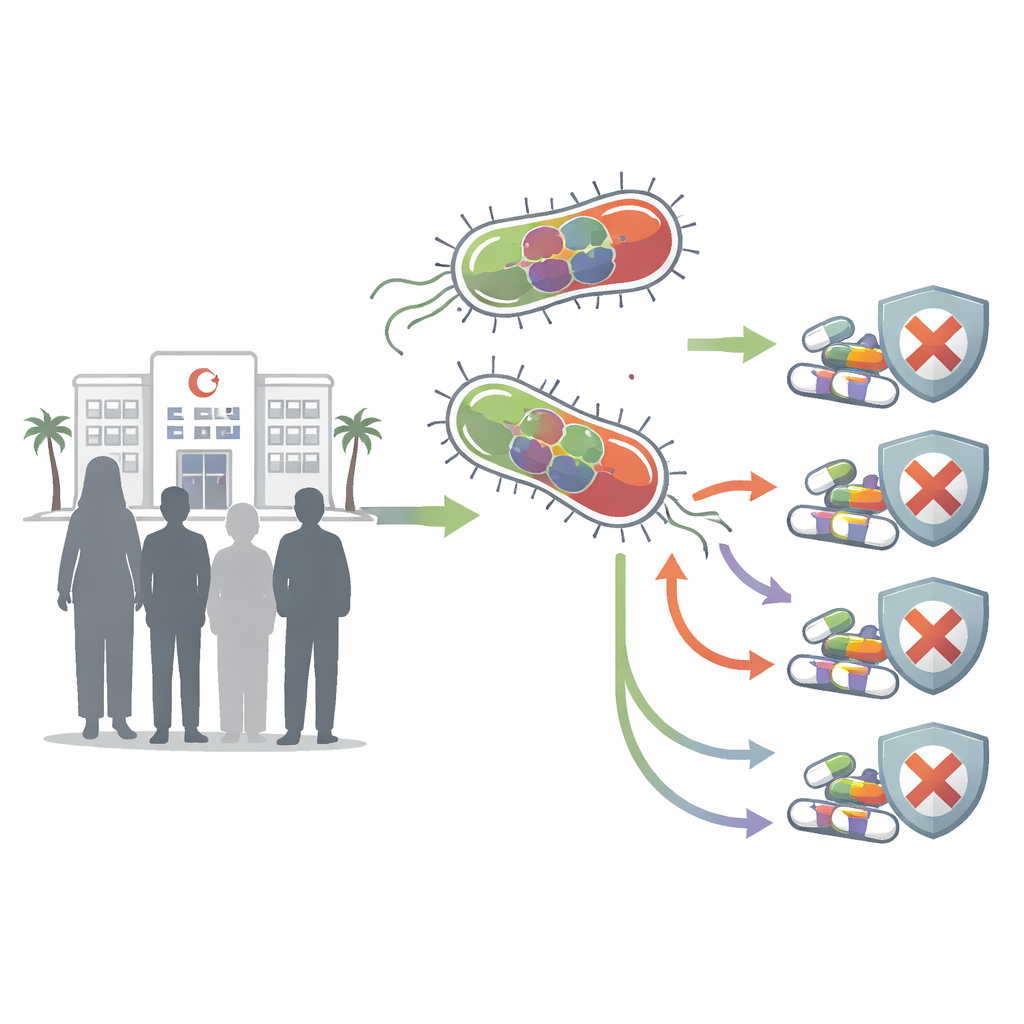
Twee patiënten, twee gevaarlijke microben
De onderzoekers concentreerden zich op twee E. coli-stammen, genoemd UPE7 en UPE139, geïsoleerd uit vrouwen met urineweginfecties in een ziekenhuis in Mansoura, Egypte. Bij testen tegen een breed scala aan antibiotica weerstonden beide stammen veel van de middelen die artsen normaal voorschrijven, waaronder meerdere reservemiddelen. Ze toonden resistentie tegen veelgebruikte penicillines en cefalosporines, krachtige carbapenems, veelgebruikte fluoroquinolonen en andere medicijnklassen. Dit patroon plaatste ze duidelijk in de categorie multiresistente bacteriën, waardoor infecties moeilijker en kostbaarder te behandelen zijn en het risico op complicaties toeneemt.
Het DNA-spelboek van de bacterie lezen
Om te achterhalen hoe deze stammen zo sterk werden, sequentieerden het team hun volledige genomen met next-generation DNA-technologie. Vervolgens gebruikten ze gespecialiseerde computertools om de genomen te scannen op genen die aan antibioticaresistentie gekoppeld zijn en op kenmerken die de bacterie helpen ziekten te veroorzaken. Beide stammen droegen talrijke resistentiegenen die overeenkwamen met hun gedrag in het laboratorium. Zo bezaten ze meerdere beta-lactamase-genen die belangrijke antibiotica afbreken, evenals genen die beschermen tegen middelen zoals aminoglycosiden, tetracyclines, macroliden, sulfonamiden en trimethoprim. Veranderingen in kern-DNA-hanterende enzymen, de doelwitten van fluoroquinolonmiddelen, kwamen overeen met hun sterke resistentie tegen levofloxacine. Beide stammen hadden ook een operon dat bekendstaat om de buitenkant van de cel te wijzigen op manieren die de werking van polymyxine-antibiotica verzwakken.
Verborgen hulpjes die resistentie verspreiden
Buiten individuele resistentiegenen benadrukt de studie de genetische voertuigen die deze eigenschappen verplaatsen. Veel van de resistentiegenen lagen naast mobiele genetische elementen zoals insertiesequenties en transposons—kleine DNA-eenheden die van plaats kunnen springen—en op plasmiden, cirkelvormige DNA-moleculen die bacteriën onderling uitwisselen. Zo werd een wijdverspreid gen voor extended-spectrum beta-lactamase, CTX-M-15, in beide stammen gekoppeld aan dergelijke mobiele elementen, terwijl UPE139 ook OXA-244 droeg, een carbapenem-afbrekend enzym ingebed tussen springende DNA-segmenten op het chromosoom. Dezelfde plasmide-types die hier zijn gevonden, zijn elders in verband gebracht met clusters van resistentiegenen, wat de zorg wekt dat deze stammen hun verdedigingen kunnen overdragen op andere bacteriën in ziekenhuizen en de gemeenschap.
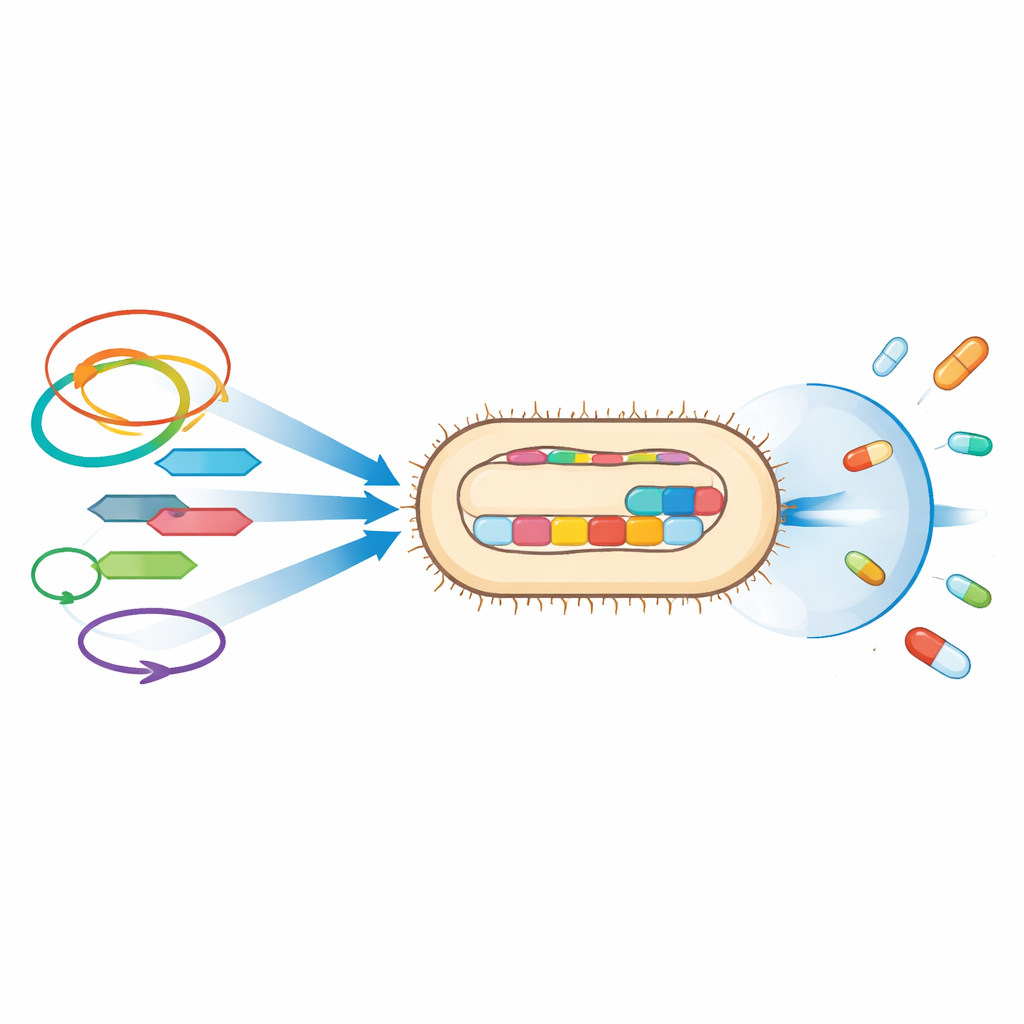
Gereedschap voor infectie en overleving
De genetische analyse bracht ook vele eigenschappen aan het licht die deze E. coli-stammen helpen de urinewegen te koloniseren en weefsels van de gastheer te beschadigen. Zowel UPE7 als UPE139 droegen meerdere adhesiestructuren die hen in staat stellen zich aan cellen vast te hechten en biofilms te vormen, beschermende gemeenschappen die moeilijker door medicijnen en het immuunsysteem worden verwijderd. Ze codeerden toxines zoals hemolysine, dat gastheercellen kan beschadigen, en ijzeropnamsystemen die de bacteriën in staat stellen te gedijen in de ijzerarme omgeving van het lichaam. UPE139 had in het bijzonder aanvullende genen gerelateerd aan kapselvorming, invasie en immuunontwijking, wat suggereert dat deze stam een bijzondere aanleg heeft om aan te houden en zich binnen patiënten te verspreiden.
Wat dit betekent voor patiënten en artsen
Door traditionele gevoeligheidstests te combineren met volledige genoomsequentiering laat deze studie zien hoe een klein aantal genen en mobiele elementen gewone urinebacteriën kan veranderen in formidabele, multiresistente ziekteverwekkers. Het toont ook aan dat deze gevaarlijke eigenschappen op DNA-segmenten zitten die zich goed lenen voor overdracht naar andere stammen, wat het risico op bredere lokale en regionale verspreiding vergroot. Voor patiënten betekent dit dat sommige veelvoorkomende infecties moeilijker te genezen kunnen worden. Voor clinici en volksgezondheidsfunctionarissen onderstreept het onderzoek de noodzaak van voortdurende genomische surveillance, zorgvuldig antibioticagebruik en bredere studies van veel meer isolaten om risico-clones te volgen, behandelrichtlijnen te verfijnen en de opmars van resistentie te vertragen.
Bronvermelding: El Halfawy, N.M., Gouda, M.K., Elgayar, F.A. et al. Genomic characterization of multidrug-resistant Escherichia coli strains identified from patients with urinary tract infection in Egypt. Sci Rep 16, 8958 (2026). https://doi.org/10.1038/s41598-026-40536-0
Trefwoorden: antibioticaresistentie, urineweginfectie, Escherichia coli, genoomsequencing, mobiele genetische elementen