Clear Sky Science · nl
Ontdekking van hydroxytriazool als potentiële glyoxalase‑I‑remmer met behulp van computerondersteunde geneesmiddeldesigntechnieken
Waarom het uitschakelen van een klein cellulair opruimer kanker kan bestrijden
Kankercellen groeien vaak zo snel dat ze verdrinken in hun eigen afval. Een van hun overlevingstrucs is een ingebouwd opruimteam dat schadelijke bijproducten van suikerafbraak neutraliseert. Deze studie onderzoekt hoe je één sleutellid van dat team, een enzym genaamd glyoxalase‑I, kunt uitschakelen door computers te gebruiken om tienduizenden moleculen te doorzoeken en experimenten om de beste kandidaten te testen. Het doel is nieuwe uitgangspunten voor geneesmiddelen te vinden die artsen op termijn in staat kunnen stellen kankercellen selectief van binnenuit te vergiftigen.
Een verborgen afvalsysteem in onze cellen
Elke cel breekt voortdurend suiker af om energie te maken, en dit proces produceert een reactief afvalmolecuul dat methylglyoxal heet. In normale hoeveelheden zetten onze lichamen methylglyoxal om in onschadelijk melkzuur via het glyoxalase‑systeem, een tweestapsroute die afhankelijk is van de hulpstof glutathion. Glyoxalase‑I is de eerste en meest cruciale stap in deze keten. Kankercellen, die suiker in razend tempo verbranden, zijn sterk afhankelijk van glyoxalase‑I om te voorkomen dat methylglyoxal toxische niveaus bereikt. Als dit enzym wordt geblokkeerd, hoopt methylglyoxal zich op en kan het beschadigde cellen naar geprogrammeerde celdood duwen. Dat maakt glyoxalase‑I tot een aantrekkelijk doelwit voor anticancermiddelen die een fundamentele zwakte van tumormetabolisme aanvallen.
Chemische ruimte doorzoeken met siliconen en statistiek
In plaats van willekeurige stoffen in het laboratorium te testen, gebruikten de onderzoekers computerondersteund geneesmiddeldesign om een grote commerciële verzameling van meer dan 50.000 kleine moleculen te doorzoeken. Gespecialiseerde software maakte eerst elke molecule schoon en standaardiseerde deze, en voorspelde vervolgens de 3D‑vorm en het gedrag bij fysiologische pH. Een snelle virtuele screeningsstap scoorde hoe goed elke kandidaat mogelijk in het actieve centrum van glyoxalase‑I zou passen. Het team paste daarna eenvoudige regels toe over grootte, oplosbaarheid en andere drug‑likeness‑eigenschappen om moleculen weg te gooien die waarschijnlijk niet in het lichaam zouden werken. Een uitgebreider dockingsprogramma onderzocht hoe de meest veelbelovende moleculen zich in het enzym konden oriënteren, vooral hoe ze het zinkmetaalatomen dat in het hart van de chemie van glyoxalase‑I zit zouden kunnen bereiken en grijpen.
Een nieuwe manier om het metalen kern van het enzym vast te pakken
Eerdere pogingen om glyoxalase‑I te blokkeren richtten zich op bekende functionele groepen, zoals carbonzuren en hydroxaminezuren, die goed zijn in metaalbinding maar vaak lijden onder slechte stabiliteit of ongewenste bijwerkingen. De huidige studie onthulde in plaats daarvan een ander type "metaalgrijpend" element: een hydroxytriazoolring. Van de zestien hooggewaardeerde moleculen die zijn gekozen voor aankoop en laboratoriumtesten, kwam er één met deze ring — gecodeerd SPB07393SC — naar voren als uitblinker. In virtuele docking reikte de hydroxytriazoolgroep naar het zinkatoom, terwijl de twee aromatische ringen zich in nabijgelegen vettere holten van het enzym staken. Computersimulaties van het complex over tientallen nanoseconden suggereerden dat het molecuul stevig gebonden bleef, met stabiele afstanden, compacte eiwitstructuur en een persistent netwerk van waterstofbruggen.
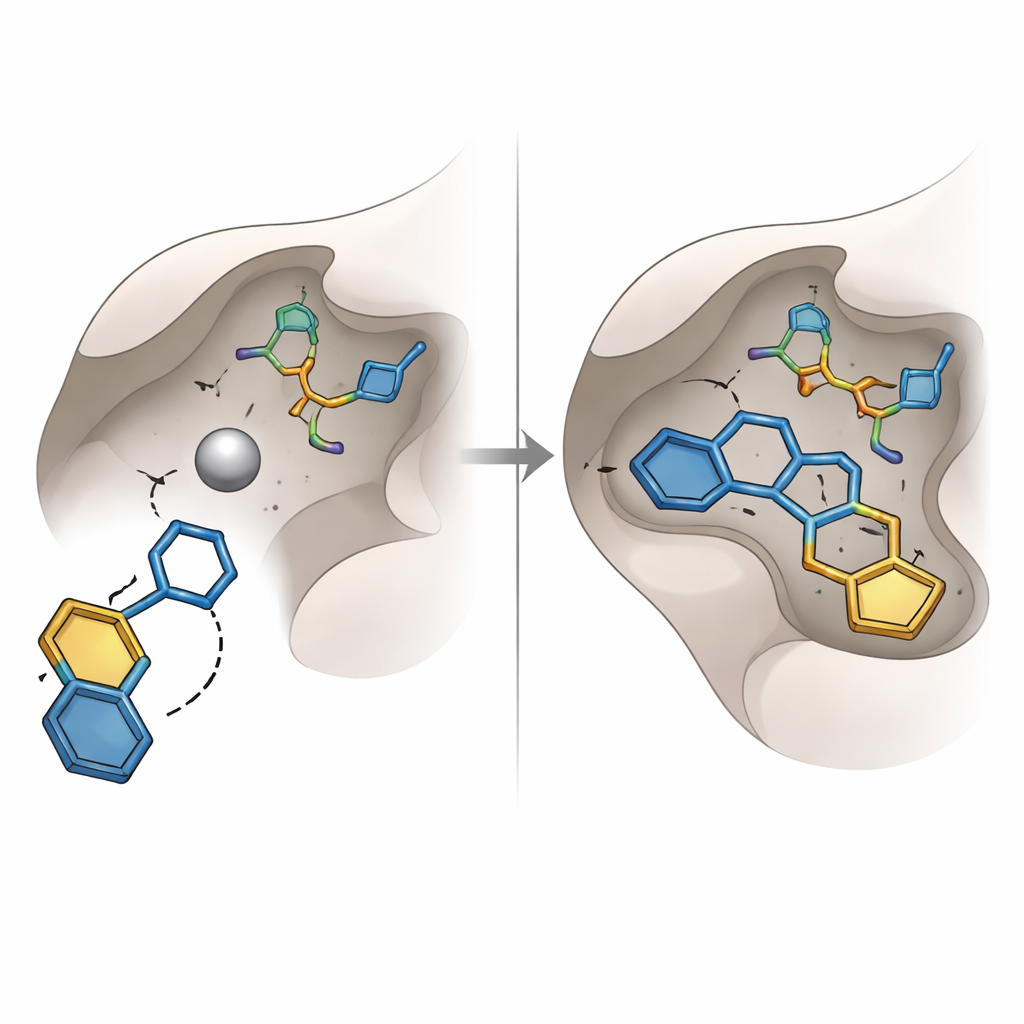
De voorspellingen op de proef stellen
Om te zien of de computermodellen zich vertaalden naar effecten in de echte wereld, mat het team hoe goed de geselecteerde moleculen de activiteit van gezuiverd humaan glyoxalase‑I in een plaatgebaseerde assay vertraagden. Vijftien van de zestien kandidaten toonden slechts zwakke of verwaarloosbare remming onder de geteste condities, wat de valkuilen benadrukt van uitsluitend vertrouwen op statische docking‑scores. In contrast remde SPB07393SC het enzym sterk, met een middelijk micromolaire potentie die het tot een solide vroege "hit" maakt in plaats van een afgewerkt geneesmiddel. Aanvullende softwaretools voorspelden dat dit molecuul acceptabele oplosbaarheid, goede absorptie, het vermogen om de hersenen te bereiken indien nodig, en een lage kans op bepaalde genetische of levergerelateerde toxiciteiten zou hebben, hoewel deze veiligheidsvoorspellingen nog experimentele bevestiging vereisen.
Wat dit betekent voor toekomstige kankertherapieën
Het werk introduceert hydroxytriazool als een nieuwe manier om kandidaat‑geneesmiddelen aan het zinkatoom in het hart van glyoxalase‑I te ankeren, en vergroot daarmee het repertoire van chemische strategieën voor geneesmiddeldesigners. Hoewel SPB07393SC zelf slechts een uitgangspunt is, maakt de combinatie van enzymremmende kracht, voorspeld drug‑achtig gedrag en stabiele binding in bewegingsgebaseerde simulaties het tot een veelbelovend skelet voor verdere verfijning. Breder gezien toont de studie zowel de sterktes als de grenzen van computergeleide screening: het kan snel enorme chemische bibliotheken terugbrengen tot enkele realistische kanshebbers, maar zorgvuldige laboratoriumexperimenten blijven essentieel om te onthullen welke moleculen het enzym daadwerkelijk uitschakelen waarop kankercellen vertrouwen om hun toxische afval te beheersen.
Bronvermelding: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Trefwoorden: glyoxalase I, kankermetabolisme, computerondersteund geneesmiddeldesign, zinkbindende remmers, moleculair docken