Clear Sky Science · nl
Alternatieve splicing en differentiële genexpressie tijdens veranderingen in endometriale receptiviteit bij patiënten met terugkerend implantatiefalen
Waarom sommige embryo’s niet innestelen
Veel paren die een in-vitrofertilisatie ondergaan stuiten op een frustrerend raadsel: zelfs wanneer hoogwaardige embryo’s worden getransfereerd, treedt er soms geen zwangerschap op. Deze studie onderzoekt nauwkeurig het baarmoederslijmvlies — het endometrium — om te begrijpen waarom sommige vrouwen herhaaldelijk mislukte innestelingen ervaren. Door te bestuderen hoe genen aan- en uitgeschakeld worden, hoe hun boodschappen geknipt en herschikt worden, en hoe immuuncellen zich gedragen tijdens het korte venster waarin de baarmoeder klaar is om een embryo te ontvangen, onthult het onderzoek nieuwe moleculaire aanwijzingen die mogelijk ooit kunnen leiden tot meer precieze tests en behandelingen.
Het korte welkomstvenster van de baarmoeder
Innesting kan alleen plaatsvinden gedurende een korte periode in elke cyclus waarin het baarmoederslijmvlies ‘‘receptief’’ wordt. De onderzoekers vergeleken weefselmonsters van 90 vruchtbare vrouwen en 73 vrouwen met terugkerend implantatiefalen, allemaal genomen op drie cruciale tijdstippen: net voordat het slijmvlies receptief wordt, tijdens het receptieve venster, en kort nadat het weer sluit. Met behulp van hoogdoorvoer RNA-sequencing bepaalden ze welke genen actief waren en hoe hun RNA-boodschappen werden verwerkt. Dit ontwerp stelde hen in staat bij te houden hoe een gezond slijmvlies zich voorbereidt op een embryo en hoe die voorbereiding misgaat bij vrouwen die herhaaldelijk niet innestelen ondanks goede embryo’s. 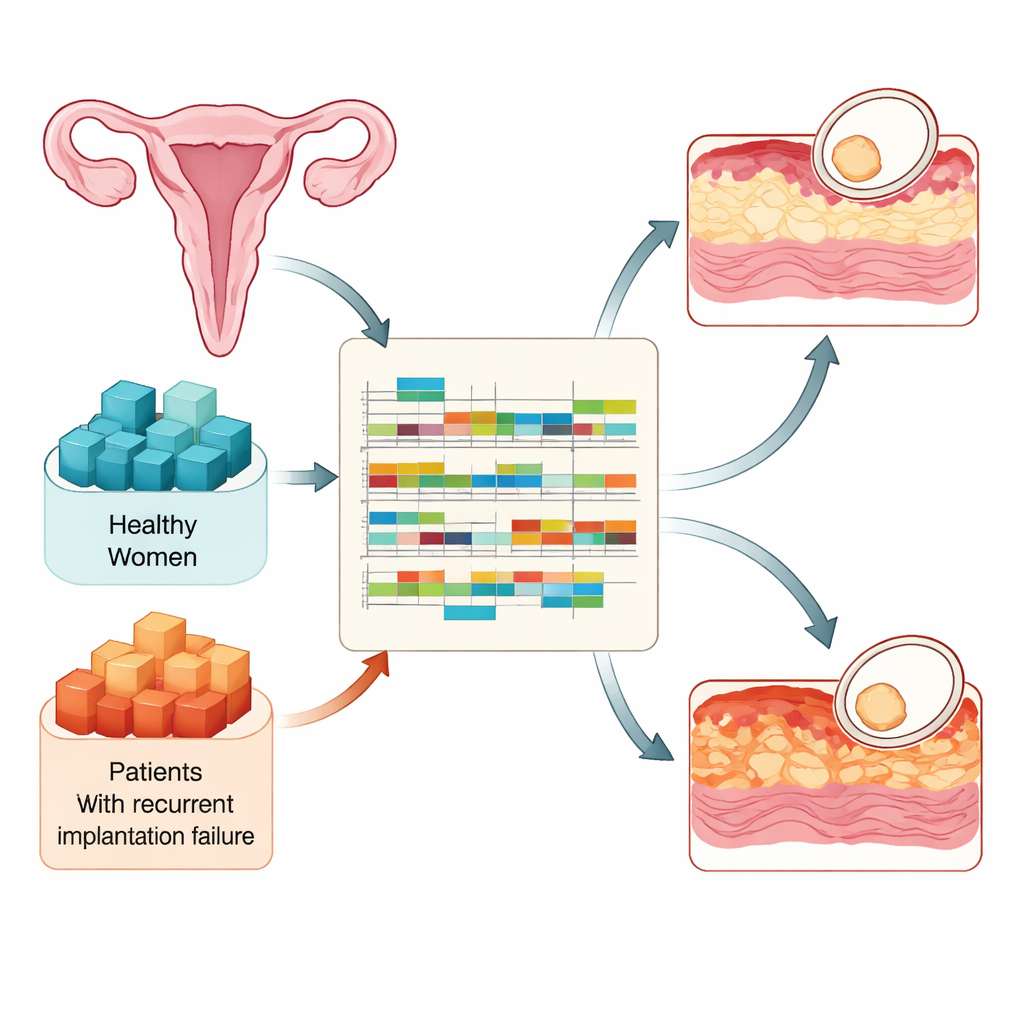
Genboodschappen geknipt en herschikt
Naast het simpelweg tellen van hoeveel van elk gen actief is, richtte het team zich op alternatieve splicing — het proces waarbij één gen in verschillende boodschapvarianten kan worden geknipt, wat leidt tot verschillende eiwitvormen. Ze vonden meer dan een miljoen splicinggebeurtenissen in de vergelijkingen, waarbij twee typen — het weglaten van gehele segmenten en het kiezen tussen elkaar uitsluitende segmenten — bijzonder vaak voorkwamen. Wanneer ze alleen keken naar veranderingen die zowel frequent als statistisch robuust waren, zagen ze honderden tot duizenden splicingverschuivingen toen het slijmvlies overging van de niet-receptieve naar de receptieve fase, met name van de vroege (pre-receptieve) fase naar het implantatievenster. Veel van deze veranderingen deden zich voor terwijl de totale hoeveelheid van het gen gelijk bleef, wat betekent dat de vorm van het eiwit veranderde zonder dat de totale genactiviteit veranderde.
Cellen plakken, hervormen en communiceren met het immuunsysteem
Genen die werden beïnvloed door gewijzigde splicing en door veranderingen in activiteit waren sterk betrokken bij hoe cellen aan elkaar hechten, hoe hun interne steigerwerk wordt herschikt, en hoe ze immuun-signalen zenden en ontvangen. Deze functies zijn cruciaal wanneer het baarmoederslijmvlies verandert van een eenvoudige barrière in een oppervlak dat een embryo kan verwelkomen en verankeren terwijl de bloedvaten worden geremodelleerd. Zowel bij vruchtbare vrouwen als bij vrouwen met implantatiefalen werd de receptieve fase gekenmerkt door sterke remodelering in deze paden, maar vrouwen met terugkerend falen vertoonden vaker of anders gepatteerde splicingveranderingen. Sommige van de betrokken genen zijn al voorgesteld als markers van het ideale implantatievenster, wat het idee versterkt dat niet alleen genactiviteit, maar ook de exacte vorm van hun producten bepaalt wanneer het slijmvlies echt klaar is.
Immuuncellen en een sleutelregulator van splicing
Het team schatte ook de typen immuuncellen die in het weefsel aanwezig waren op basis van dezelfde RNA-gegevens. Bij vrouwen met implantatiefalen liet de receptieve fase minder cytotoxische T-cellen en meer rustende natural killer-cellen zien, maar meer monocyten en bepaalde macrofagen vergeleken met eerdere fasen. Later, nadat het venster gesloten was, verschoven de patronen opnieuw, met veranderingen in geactiveerde natural killer-cellen en macrofaag-subtypes. Verschillende van deze immuuncelveranderingen volgden specifiek bepaalde splicinggebeurtenissen nauw, wat suggereert dat het herschikken van genboodschappen en de immuunbalans met elkaar verbonden zijn. Onder eiwitten die splicing reguleren, stak er één genaamd KHDRBS3 uit als een centraal knooppunt dat gekoppeld was aan veel van de veranderde gebeurtenissen en dat consequent in niveau daalde toen het slijmvlies receptief werd, zowel bij vruchtbare als bij getroffen vrouwen. Dit suggereert dat het kan helpen de switch in splicingpatronen aan te sturen die samenvalt met het openen van het implantatievenster. 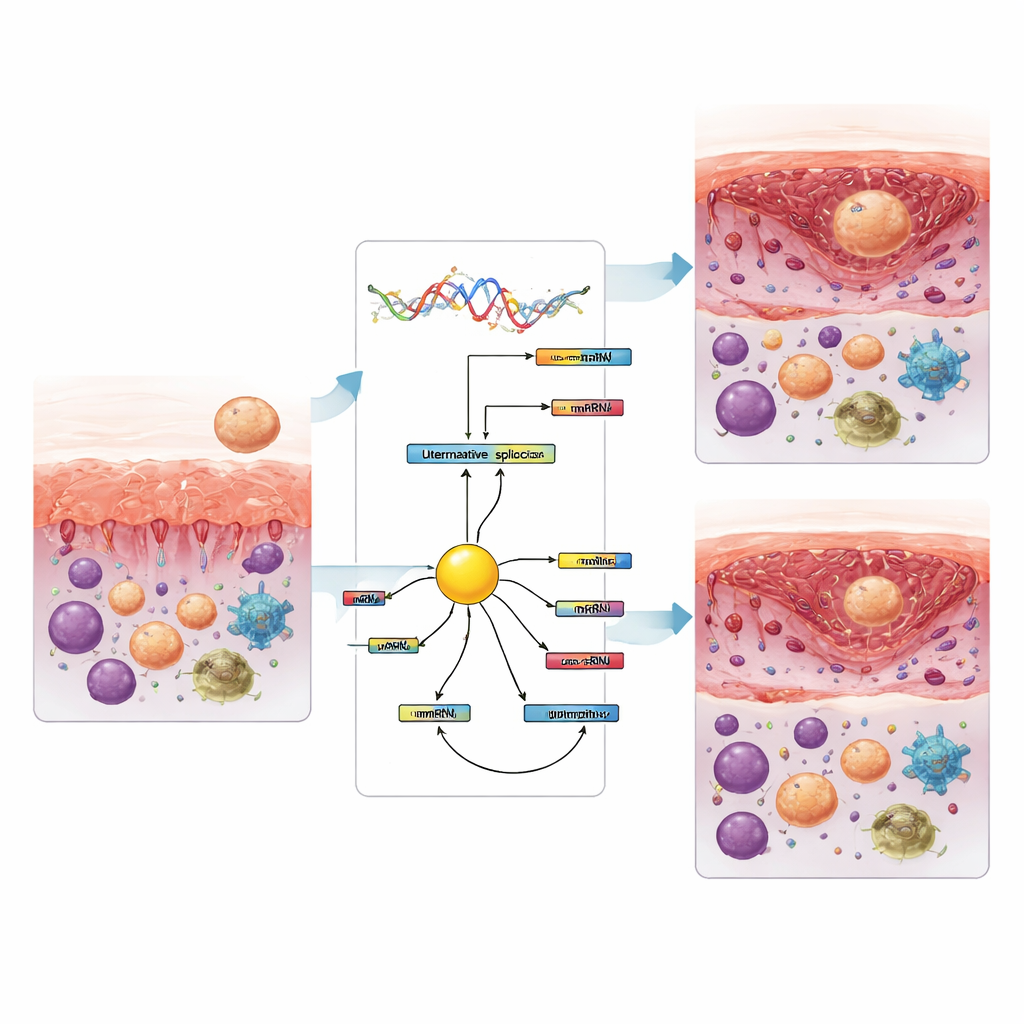
Wegwijzer naar toekomstige tests en behandelingen
Om deze moleculaire patronen naar mogelijke therapieën te vertalen, vroegen de onderzoekers zich af of bestaande kleine-molecuul geneesmiddelen de abnormale splicingssignaturen die ze observeerden, zouden kunnen tegenwerken. Door hun genlijsten te matchen met grote databanken van geneesmiddelresponsen identificeerden ze verschillende goedgekeurde of experimentele verbindingen die genen beïnvloeden die met innesteling te maken hebben, inclusief middelen die immuunreacties of hormoongerelateerde paden beïnvloeden. Hoewel deze nog lang niet klaar zijn voor klinisch gebruik in deze context, vormen ze een beginpunt voor laboratoriumonderzoek.
Wat dit betekent voor patiënten
Al met al laat de studie zien dat implantatiefalen niet simpelweg een kwestie is van het hebben van de ‘‘verkeerde’’ genen, maar van hoe die genen worden bewerkt tot verschillende boodschappen en hoe de immuunomgeving van de baarmoeder in de tijd wordt afgestemd. Het werk belicht KHDRBS3 en gerelateerde factoren als veelbelovende regelaars van dit proces en onthult gecoördineerde verschuivingen in immuuncellen die een embryo kunnen ondersteunen of tegenwerken bij zijn poging zich te vestigen. Op de lange termijn zouden dergelijke inzichten kunnen leiden tot verfijnde tests die het werkelijke tijdstip en de kwaliteit van het receptieve venster bepalen, evenals gerichte behandelingen die genboodschappen of immuunbalans voorzichtig bijsturen om embryo’s een betere kans te geven zich in te nestelen.
Bronvermelding: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Trefwoorden: endometriumreceptiviteit, terugkerend implantatiefalen, alternatieve splicing, uteriene immuuncellen, geassisteerde voortplanting