Clear Sky Science · nl
Trabectedine plus CD13-gericht weefselfactor tTF-NGR tegen gevorderd terugkerend of refractair weke-delen-sarcoom: translationele gegevens, klinische veiligheid en werkzaamheid
Waarom dit onderzoek ertoe doet
Mensen met gevorderde weke-delen-sarcomen — zeldzame kankers die in spieren, vet of ander steunweefsel groeien — raken vaak door hun effectieve behandelingsopties heen. Deze studie onderzoekt een nieuwe twee-stappen medicijnstrategie die bedoeld is om een bestaand chemotherapiemiddel in de tumor te vangen en de bloedtoevoer naar de tumor af te sluiten, met de hoop de ziekte beter onder controle te krijgen terwijl bijwerkingen beheersbaar blijven.
Een zeldzame kanker die betere opties nodig heeft
Weke-delen-sarcomen vormen slechts ongeveer 1% van de kankers bij volwassenen, maar zijn vaak agressief zodra ze uitzaaien of niet chirurgisch te verwijderen zijn. Standaardchemotherapie kan hun groei vertragen, maar de overleving bij gevorderde ziekte blijft slecht. Trabectedine is een van de belangrijkste middelen die worden gebruikt nadat eerstelijnsbehandelingen falen. Het werkt door het DNA van kankercellen te beschadigen en beïnvloedt ook cellen in de tumoromgeving. Toch groeien veel tumoren uiteindelijk weer, wat onderzoekers ertoe brengt manieren te zoeken om de impact te vergroten zonder de schade voor patiënten sterk te verhogen.
Een twee-stappen “val” voor de tumor
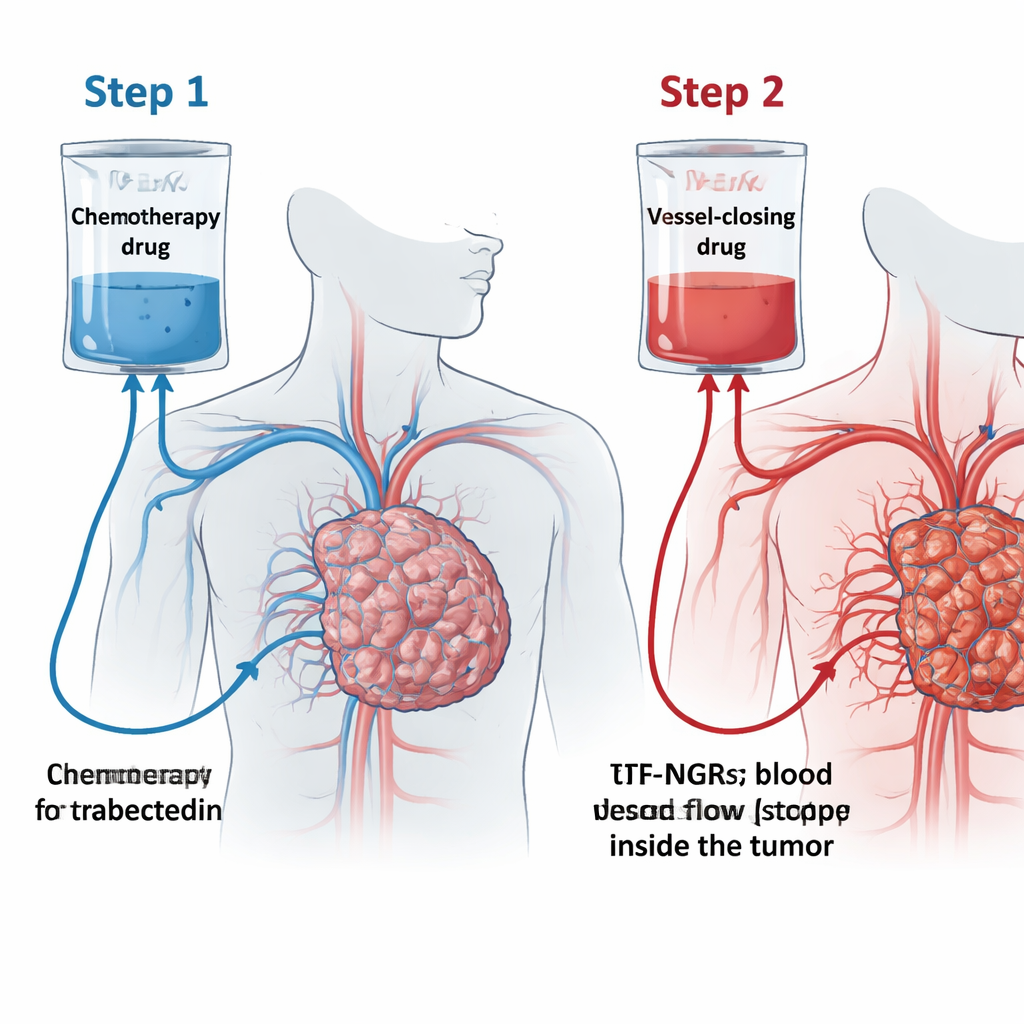
Het team testte een concept dat zij de “trabectedine-val” (TRABTRAP) noemen. Eerst krijgen patiënten trabectedine via een infusie van 24 uur. In de twee of drie daaropvolgende dagen krijgen ze een tweede middel, tTF-NGR. Dit ontworpen eiwit richt zich op een marker genaamd CD13 die vooral op bloedvaten van tumoren voorkomt. Wanneer tTF-NGR zich aan deze vaten hecht, veroorzaakt het lokale bloedstolling en blokkeert het de bloedstroom, waardoor delen van de tumor afsterven. Het idee is dat het eerst toedienen van trabectedine het middel in de tumor laat doordringen, en dat tTF-NGR vervolgens de uitgangen dichtzet door de kleine vaten van de tumor te sluiten, waardoor het medicijn op de plek blijft waar het het meest nodig is en de werking van beide behandelingen wordt versterkt.
Van laboratorium naar vroege patiëntentest
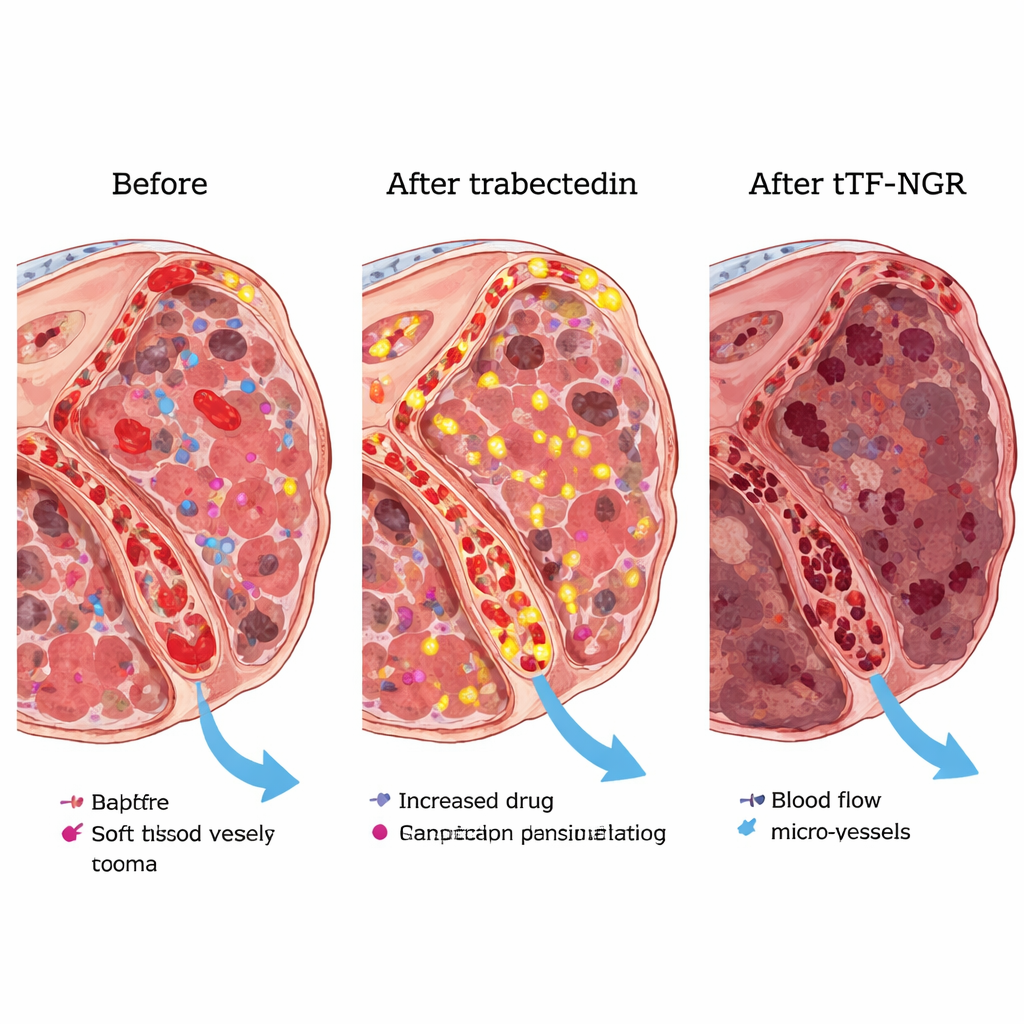
In laboratoriumexperimenten toonden de onderzoekers aan dat trabectedine ervoor zorgt dat bloedvatcellen en sarcomacellen meer van een bepaald vetmolecuul op hun oppervlak tonen dat stolling ondersteunt. Deze verandering maakte tTF-NGR effectiever in het veroorzaken van lokale stolselvorming op deze cellen, wat precies nodig is om tumorvaten af te sluiten. Bij muizen met humane sarcoomtumoren verkleinde de volgorde trabectedine gevolgd door tTF-NGR de tumoren meer dan elk middel afzonderlijk. Omdat de dierlijke tumoren onder de combinatie zo grondig afbraken, kon het team niet betrouwbaar meten hoeveel extra trabectedine werd vastgehouden, maar de sterkere tumorcontrole ondersteunde het basisidee van de “val.”
Een veilige dosis vinden bij echte patiënten
Het hart van dit artikel is de veiligheids "run-in"-fase van de TRABTRAP-studie bij 19 mensen met gevorderde, zwaar voorbehandelde weke-delen-sarcomen. Alle patiënten kregen de standaarddosis trabectedine. Het tweede middel, tTF-NGR, werd gestart op de hoogste dosis die eerder als los middel werd verdragen en vervolgens zorgvuldig verlaagd wanneer ernstige bijwerkingen optraden. Bij hogere doseringen ontwikkelden sommige patiënten aanzienlijke hartgerelateerde of stollingsproblemen, zoals stille schade aan de hartspier zichtbaar in bloedtesten, kleine longembolieën of diepe-veneuze trombose. Deze gebeurtenissen waren omkeerbaar met behandeling en het stoppen of verlagen van tTF-NGR, maar gaven aan dat lagere doses nodig waren. Bij 0,5 mg/m² tTF-NGR gegeven op twee dagen na trabectedine voltooiden zes patiënten ten minste twee cycli zonder dose-limiting toxiciteiten, en sommigen gingen door tot wel 14 cycli.
Vroege aanwijzingen voor voordeel en hoe de middelen op elkaar inwerken
Hoewel dit deel van de studie te klein was om effectiviteit te bewijzen, waren de resultaten bemoedigend. Van de 19 patiënten had de meerderheid ten minste tijdelijke ziektecontrole, en twee lieten duidelijke partiële tumorregressie zien. Bij mensen met liposarcoom of leiomyosarcoom — twee veelvoorkomende sarcoomsubtypen waarbij trabectedine vaak wordt gebruikt — had bijna twee derde stabiele ziekte of partiële responsen bij de eerste grote controle. Gedetailleerde MRI-scans bij één patiënt bevestigden dat tTF-NGR bij de gekozen dosis selectief de bloedstroom in tumordeposities kon verminderen. Bloedtesten toonden aan dat, wanneer tTF-NGR na trabectedine werd gegeven, tTF-NGR langer in de circulatie bleef en actiever leek dan wanneer het alleen werd gebruikt, wat helpt verklaren waarom de veilige dosis in combinatie lager is dan voor het middel alleen.
Wat dit betekent voor patiënten
Voor mensen met gevorderd weke-delen-sarcoom vertegenwoordigt TRABTRAP een zorgvuldig ontworpen poging om meer uit een bestaande chemotherapie te halen door deze te combineren met een vat-sluitend middel dat zich richt op de bloedtoevoer van de tumor zelf. De safety run-in toont dat deze combinatie, bij aangepaste doseringen, herhaaldelijk kan worden gegeven, met bijwerkingen die belangrijk maar over het algemeen beheersbaar en omkeerbaar zijn onder nauw toezicht. Hoewel het nog te vroeg is om te zeggen of dit de levensduur zal verlengen of consequent tumoren zal verkleinen, rechtvaardigen de veelbelovende vroege ziektecontrole en de duidelijke effecten op tumorbloedstroom verdergaan naar een grotere, gerandomiseerde studie. Als toekomstige resultaten positief zijn, zou deze twee-stappenbenadering een nieuw spoor kunnen openen voor de behandeling van sarcomen en vergelijkbare strategieën voor andere moeilijk behandelbare kankers kunnen inspireren.
Bronvermelding: Hessling, K., Brand, C., Schwöppe, C. et al. Trabectedin plus CD13-targeted tissue factor tTF-NGR against advanced relapsed or refractory soft tissue sarcoma: translational data, clinical safety and efficacy. Sci Rep 16, 7389 (2026). https://doi.org/10.1038/s41598-026-40362-4
Trefwoorden: weke-delen-sarcoom, trabectedine, tumorbloedvaten, gerichte stollingstherapie, combinatiechemotherapie