Clear Sky Science · nl
Adaptieve voorbeelduitselectie voor prototype-gebaseerde uitlegbare mitose-detectie in digitale pathologie
Waarom dit belangrijk is voor kankerzorg
Wanneer pathologen kankermonsters onder de microscoop bekijken, helpt het tellen van hoeveel tumorcellen actief delen bij het bepalen hoe agressief een tumor is en welke behandelingen passend zijn. Kunstmatige intelligentie kan deze delende cellen nu snel opsporen in digitale preparaten, maar haar beslissingen zijn vaak een raadsel, zelfs voor experts. Dit artikel introduceert een methode genaamd Adaptive Example Selection (AES) die een AI-systeem laat "zijn werk tonen" door te verwijzen naar echte eerdere gevallen die elke beslissing ondersteunen of tegenspreken, waardoor geautomatiseerde mitose-detectie transparanter en klinisch betrouwbaarder wordt.
De uitdaging van het herkennen van delende cellen
Delende tumorcellen, bekend als mitotische figuren, zijn klein, zeldzaam en visueel divers. Onder de gebruikelijke roze-paars kleuring kunnen ze sterk lijken op onschuldige structuren zoals afstervende cellen of bepaalde immuuncellen. Menselijke experts moeten grote digitale preparaten scannen om ze te vinden, een proces dat traag, vermoeiend en vatbaar voor onenigheid is. Moderne deep-learningsystemen kunnen bij deze taak het niveau van experts evenaren of overtreffen, maar ze gedragen zich als black boxes: ze geven een score voor elke verdachte cel zonder duidelijk uit te leggen waarom. In de geneeskunde, waar behandelingskeuzes levensveranderend kunnen zijn, is dat gebrek aan duidelijkheid een serieus obstakel voor het routinematig inzetten van AI.
Een krachtige maar ondoorzichtige detector bouwen
De auteurs trainen eerst een state-of-the-art objectdetectienetwerk, gebaseerd op de Faster R-CNN-architectuur, om mitotische figuren te vinden in een grote, diverse dataset genaamd MIDOG++. Deze beelden komen zowel van menselijke als canine tumoren, over verschillende kankertypen en laboratoria, en bevatten meer dan elftienhonderd zorgvuldig gelabelde delende cellen. Om fijne details te behouden worden de preparaten in kleine patches gesneden en sterk geaugmenteerd om variaties in kleuring en beeldvorming uit de echte wereld na te bootsen. De resulterende detector behaalt solide prestaties over tumorsoorten heen, met F1-scores tot 0,84, wat bevestigt dat hij nauwkeurig maar complex is — precies het soort systeem dat betere uitleg nodig heeft voordat clinici erop kunnen vertrouwen in de praktijk.
De AI leren zichzelf uit te leggen met voorbeelden
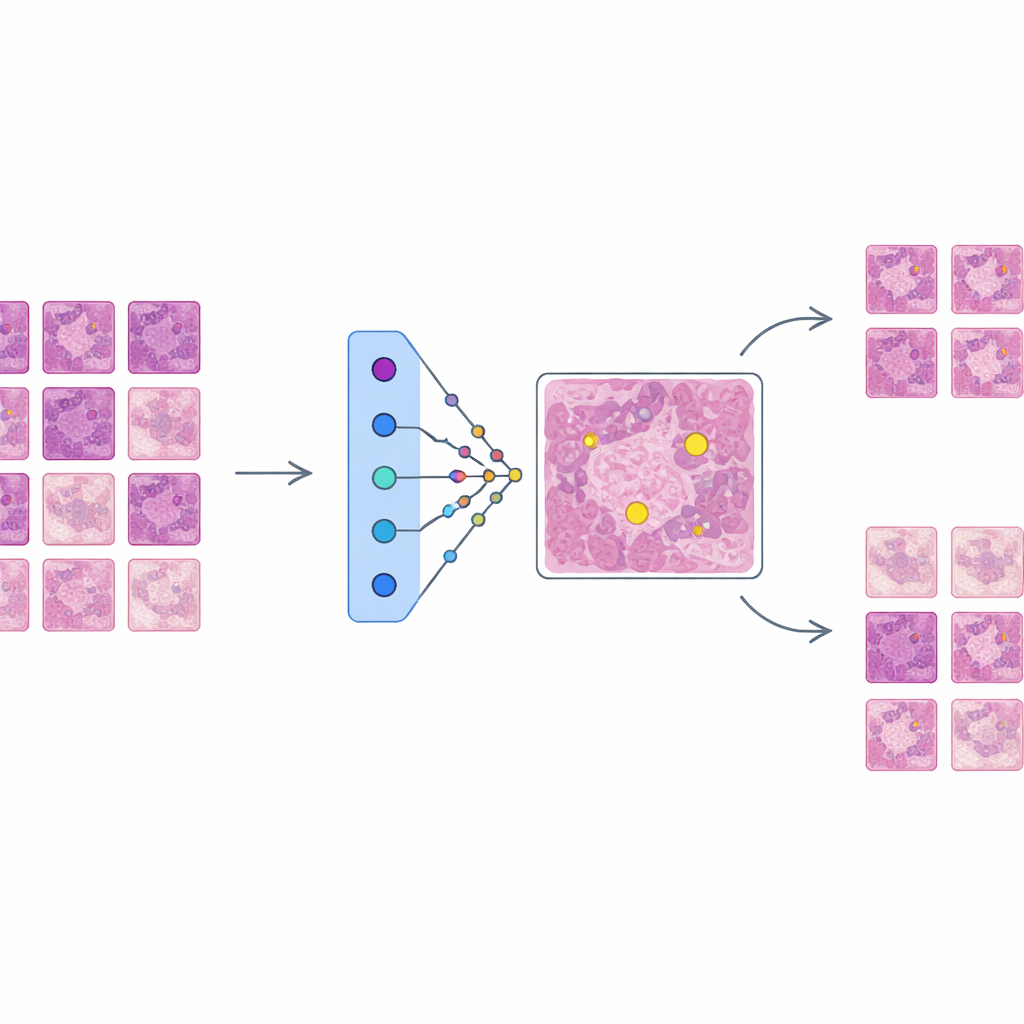
AES zit bovenop deze getrainde detector als een interpretatielaag in plaats van de werking van de detector te wijzigen. Voor elk kandidaatgebied dat de detector markeert als mogelijk mitotisch, zoekt AES in een bibliotheek van echte weefselpatches uit de trainingsdata. Uit deze bibliotheek selecteert het een kleine set "ondersteunende" voorbeelden die lijken op echte mitoses en een set "tegensprekende" voorbeelden die meer op niet-mitotische cellen lijken. Achter de schermen behandelt AES de vertrouwensscores van de detector als een glad landschap en gebruikt het een wiskundig instrument genaamd radialebasisfuncties om te benaderen hoe die vertrouwen varieert in de buurt van elk geval. Alleen prototypes die de lokale vertrouwenswaarde betekenisvol beïnvloeden worden behouden, zodat de verklaring voor een enkele beslissing doorgaans uit ongeveer tien zorgvuldig gekozen voorbeelden bestaat in plaats van honderden nauwelijks relevante voorbeelden.
Wat de voorbeelden onthullen over AI-besluiten
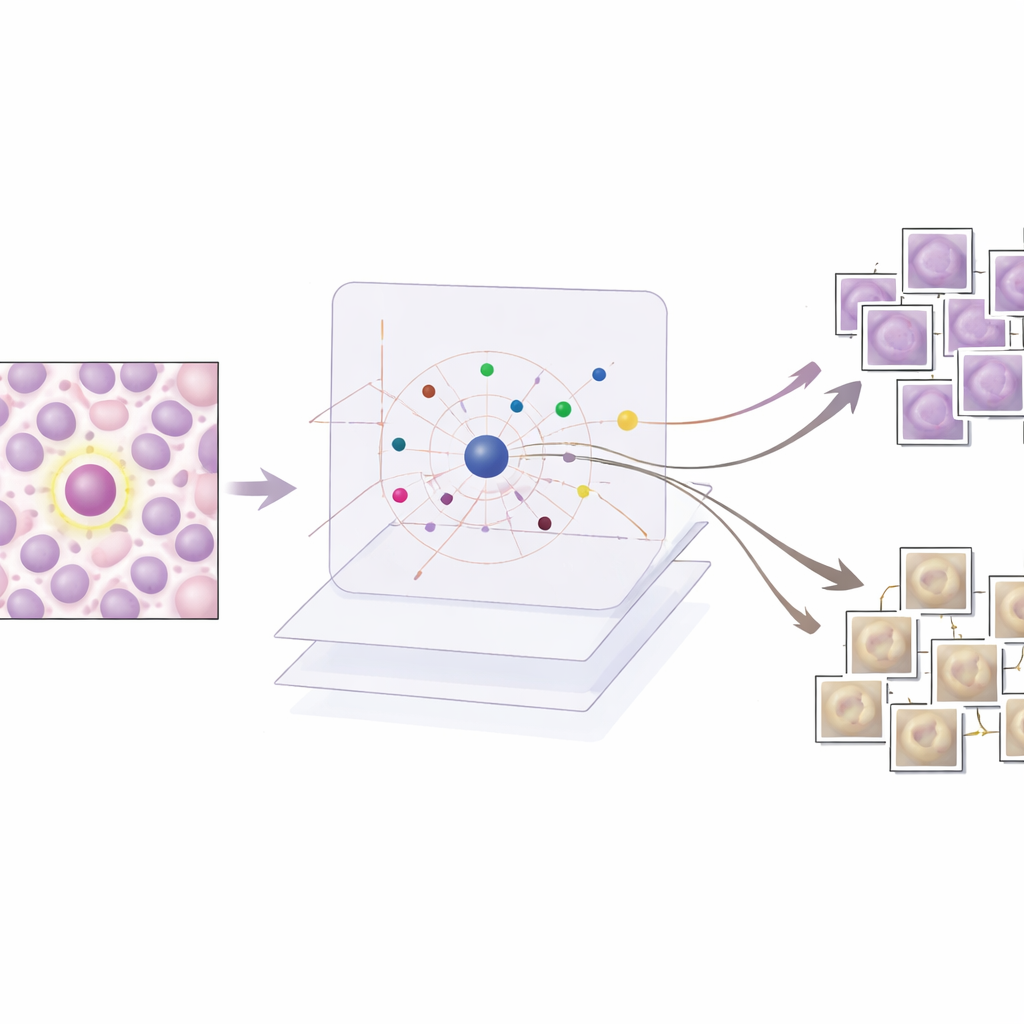
De onderzoekers evalueren AES zowel kwantitatief als kwalitatief. Kwantitatief tonen ze aan dat een compact woordenboek van ongeveer 190 prototype-afbeeldingen de vertrouwensscores van de detector met zeer hoge nauwkeurigheid kan nabootsen, terwijl het aantal getoonde voorbeelden per geval laag genoeg blijft voor een menselijke beoordeling. Kwalitatief onderzoeken ze drie veelvoorkomende scenario’s. Wanneer de detector duidelijk correct is, geeft AES alleen mitotische prototypes terug die de beslissing sterk ondersteunen, wat geruststellend is voor clinici. Bij vals alarm laat de methode mitose-achtige voorbeelden zien die verklaren waarom de detector werd misleid door vergelijkbare textuur- of chromatinepatronen, vaak naast zwakkere niet-mitotische prototypes die op onzekerheid duiden. Bij gemiste mitoses geeft AES meestal voornamelijk niet-mitotische of ambigue voorbeelden terug, wat wijst op blinde vlekken in de trainingsdata en suggereert waar nieuwe of beter gelabelde voorbeelden nodig zijn.
Van black box naar samenwerkend hulpmiddel
Door elke voorspelling te funderen op een handvol echte, gelabelde weefselpatches, laat AES een complexe AI-detector zich meer gedragen als een menselijke collega die beslissingen verantwoordt door eerdere gevallen te herinneren. Het systeem rapporteert niet alleen of een cel waarschijnlijk deelt, maar toont ook waarom en hoe zeker het is, via de samenstelling en invloed van ondersteunende en tegensprekende prototypes. Dit ontwerp stelt pathologen in staat sterke voorspellingen snel te bevestigen, de aandacht te richten op grensgevallen of verwarrende regio’s en systematische foutpatronen te identificeren die richting geven aan vervolgtraining. Hoewel ontwikkeld voor mitose-detectie kan dezelfde aanpak worden uitgebreid naar andere taken in digitale pathologie, waarmee AI verschuift van ondoorzichtige automatisering naar een uitlegbare, casusgebaseerde assistent die clinici kunnen bevragen, vertrouwen en verfijnen.
Bronvermelding: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Trefwoorden: uitlegbare AI, digitale pathologie, mitose-detectie, prototype-gebaseerde modellen, kankerdiagnostiek