Clear Sky Science · nl
Ultra-intensieve pulserende bron van ioniserende straling gebaseerd op directe laseracceleratie van elektronen voor het bestuderen van het FLASH-effect
Waarom ultra-snelle stralingspulsen ertoe doen
Radiotherapie voor kanker balanceert op een koord: genoeg straling toedienen om tumoren te doden zonder blijvende schade aan gezond weefsel. Een recent en veelbelovend idee, het zogenaamde FLASH-effect, suggereert dat het toedienen van straling in een ultra-korte, ultra-intense uitbarsting normaal weefsel kan sparen terwijl de kanker toch wordt bestreden. Deze studie presenteert een nieuw experimenteel stralingsbron gebaseerd op een krachtige laser die extreem korte pulsen hoogenergetische elektronen produceert, en gebruikt deze om te observeren hoe zuurstof in water en biologische vloeistoffen plotseling verbruikt wordt tijdens bestraling — een proces dat als centraal voor het FLASH-effect wordt gezien. 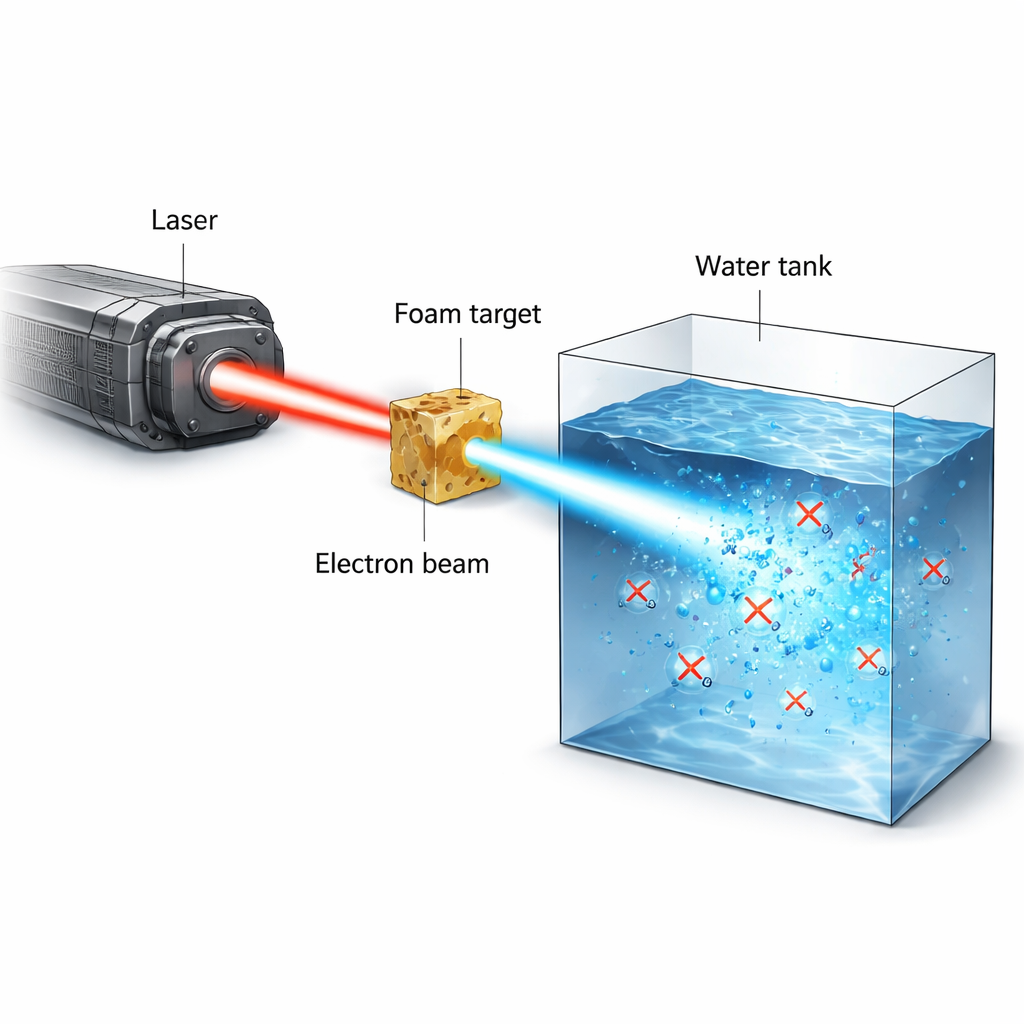
Van ziekenhuisapparaten naar laser-gedreven bundels
Conventionele radiotherapie gebruikt röntgenstraling, elektronen of protonen uit grote versnellers. Deze machines geven doorgaans dosis af over milliseconden tot seconden en, hoewel ze zeer nauwkeurig zijn, beschadigen ze toch gezond weefsel omdat straling indirect DNA breekt door watermoleculen te splitsen en reactieve zuurstofsoorten te genereren. Zuurstof in gezond, goed doorbloed weefsel vergroot deze schade juist — het zogenaamde zuurstof-effect. FLASH-radiotherapie wil dit omkeren door de volledige therapeutische dosis in een fractie van een seconde bij ultra-hoge dosissnelheden toe te dienen, wat in dierstudies lijkt te leiden tot tijdelijke bescherming van normaal weefsel zonder tumoren te beschermen. Standaard medische versnellers halen deze extreme dosissnelheden echter moeilijk, wat de zoektocht naar alternatieve bronnen zoals hogekrachtlasers aanjaagt.
Schuim en licht veranderen in een krachtige elektronenuitbarsting
De onderzoekers gebruikten de PHELIX hogekrachtlaser om smalle, hoge-stroom bundels elektronen te creëren met energieën van enkele mega-elektronvolt (MeV). De laser ioniseert eerst een laag-dichtheid polymeer schuim tot een bijna-kritisch plasma. In een tweede, ultra-korte puls van minder dan een biljoenste van een seconde duwt en vangt de laser vervolgens elektronen in een plasmakanaal en accelereert ze rechtstreeks naar hoge energieën. Dit proces, directe laseracceleratie genoemd, produceert een strak gekolimeerde bundel die tientallen nanocoulomb lading kan dragen in een piekseconde-schaal puls. Wanneer deze bundel water of waterachtig materiaal raakt, kan hij in één enkele opname 20–50 gray dosis afzetten, bij instantane dosissnelheden boven 10¹³ gray per seconde — ver boven wat conventionele machines kunnen bereiken.
Zien hoe zuurstof in één oogopslag verdwijnt
Om te onderzoeken hoe zulke intense pulsen de chemie onder weefselachtige omstandigheden beïnvloeden, bouwde het team verzegelde watertanks die in vacuüm konden werken en gevuld konden worden met zuiver water, celkweekmedium of gelizeerde cellen, allemaal vooraf volledig geoxygeneerd. De elektronenbundel werd gevormd en gefilterd zodat hoogenergetische elektronen de dosis in de tank domineerden, terwijl protonen en röntgenstraling grotendeels werden onderdrukt of zorgvuldig werden gecompenseerd met lagen afscherming en radiochromische films. Een optische sensor geplaatst aan de binnenwand van de tank monitorde opgeloste zuurstof door te meten hoe zuurstofmoleculen de luminescentie van een kleurstofvlek dempen. Na elke enkele-puls bestraling registreerde de sensor een plotselinge daling in zuurstofconcentratie die daarna langzaam herstelde terwijl zuurstof binnen het sensorgebied diffundeerde. Door filmdatagegevens, simulaties en het bekende stopvermogen van elektronen te combineren, reconstrueerden de auteurs de aan het bestraalde volume toegebrachte dosis en koppelden die direct aan de gemeten zuurstofaftak.
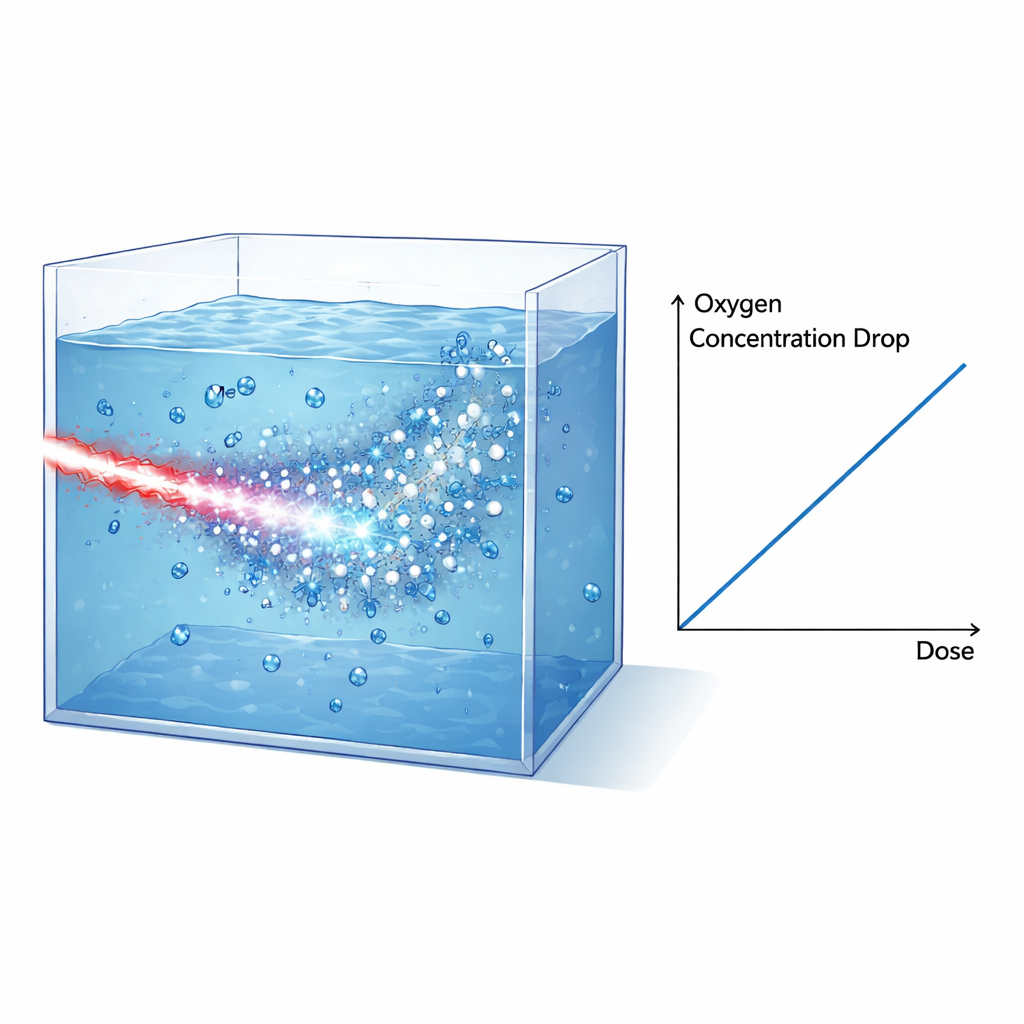
Experiment en theorie verbinden
De belangrijkste bevinding is dat de daling in opgeloste zuurstof evenredig is met de toegediende dosis voor zowel water als kweekmedium, met zeer vergelijkbare hellingen. Na correctie voor een kleine additionele dosis van röntgenstraling is de gemeten zuurstofconsumptie in water ongeveer 0,32 micromol per liter per gray. Deze waarde komt opmerkelijk goed overeen met voorspellingen uit gedetailleerde Monte Carlo track-structure simulaties (TRAX-CHEM), die de paden van elektronen in water volgen en de snelle chemie modelleren die zich binnen microseconden na bestraling ontvouwt. Cruciaal is dat in deze laser-gedreven opstelling bijna de volledige dosis binnen circa één picoseconde wordt afgegeven — veel korter dan de karakteristieke tijden van de daaropvolgende chemische reacties. Dat betekent dat het experiment nauwkeurig de ideale omstandigheden reproduceert die in deze simulaties worden verondersteld, en zo een strenge toets vormt voor de onderliggende modellen.
Een beter testplatform voor FLASH-onderzoek bouwen
Naast het valideren van theorie gebruiken de auteurs hun resultaten om een verbeterde experimentele opstelling te ontwerpen. Door de geometrie te vereenvoudigen, magneten te verwijderen en water en dosis-meetfilms symmetrisch rond de bundel te plaatsen, zouden toekomstige opstellingen de dosis binnen de tank direct kunnen meten zonder complexe reconstructie, terwijl ongewenste proton- en röntgenbijdragen verder worden onderdrukt. Simulaties tonen dat het aanpassen van het target — bijvoorbeeld het toevoegen van dunne plastic- of goudlagen — de dosis per opname kan afstemmen tussen ruwweg 40 en 80 gray, waardoor een flexibel platform ontstaat om een breed scala aan condities te verkennen die relevant zijn voor FLASH.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet-specialisten is de kernboodschap dat deze laser-gebaseerde bron extreem intense, ultra-korte elektronenpulsen creëert die de omstandigheden voor FLASH-radiotherapie nabootsen — en op sommige punten overschrijden. De studie toont aan dat deze pulsen snel opgeloste zuurstof in water en biologische media verbruiken op een manier die overeenkomt met geavanceerde theoretische voorspellingen. Aangezien zuurstofuitputting en verwante radicaalchemie leidende kandidaten zijn om te verklaren waarom FLASH gezond weefsel kan sparen, is het hebben van een controleerbare, goed begrepen bron als deze een belangrijke stap voorwaarts. Het biedt een krachtig testplatform om modellen te verfijnen en uiteindelijk het ontwerp van toekomstige klinische machines te sturen die kanker effectiever kunnen behandelen met minder bijwerkingen.
Bronvermelding: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Trefwoorden: FLASH-radiotherapie, laser-gedreven elektronen, ultra-hoge dosissnelheid, zuurstofuitputting, waterradiolyse