Clear Sky Science · nl
Selectieve klaring van monoklonale antilichamen via de mannosereceptor hangt af van glykaanparing
Waarom suikerpatronen op geneesmiddelen ertoe doen
Veel van de huidige blockbustermedicijnen zijn monoklonale antilichamen—ontworpen eiwitten die wekenlang in de bloedbaan kunnen blijven en gericht ziekten zoals kanker en auto-immuunziekten kunnen aanpakken. Maar niet alle antilichamen gedragen zich na injectie hetzelfde. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote gevolgen: hoe bepaalt het fijne “suikerpatroon” dat aan een antilichaam vastzit hoe snel het lichaam het verwijdert, en kan dit ook bijwerkingen zoals immuunreacties beïnvloeden?
Kleine suikers als verkeersborden
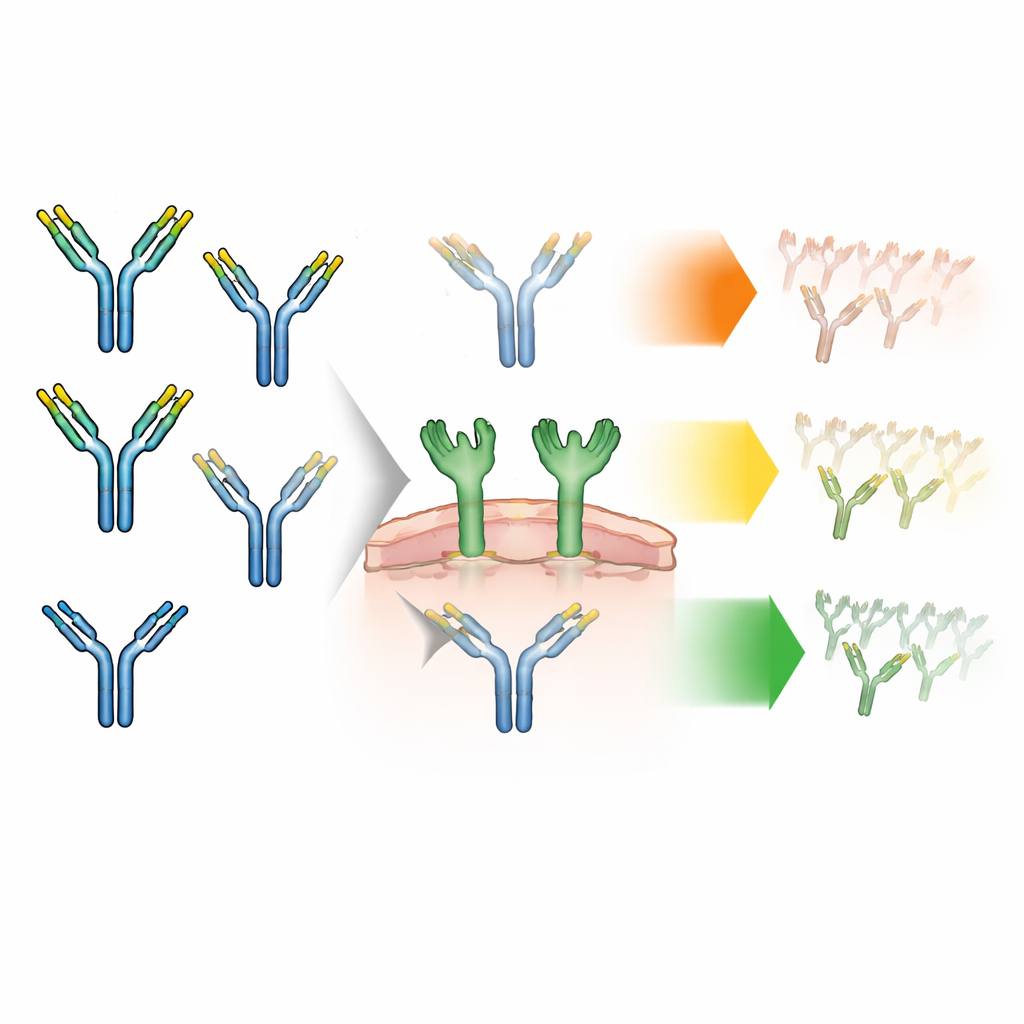
Antilichamen dragen van nature korte ketens suikers—glykanen genoemd—aan hun ruggegraat. Deze glykanen komen in verschillende varianten. De meeste hebben een “complexe” structuur, maar een minderheid is “high-mannose”, een eenvoudiger type dat in eerder werk werd gekoppeld aan snellere verwijdering uit het bloed. Elk antilichaam heeft twee suikersites die als een paar functioneren; die kunnen gelijk zijn (symmetrische paren) of verschillen (asymmetrische paren). Tot nu toe telden fabrikanten meestal enkel hoeveel van elk suikertype er in totaal aanwezig was, zonder te vragen hoe de twee suikers op hetzelfde antilichaam gepaard waren. De auteurs vermoedden dat deze paringspatronen kunnen veranderen hoe sterk antilichamen interageren met een speciaal suikersensor-eiwit op immuuncellen, de mannosereceptor—en daarmee hoe snel het lichaam het geneesmiddel klaren.
Antilichamen sorteren op hun suikerparen
Om dit te onderzoeken, maakten de onderzoekers antilichamen verrijkt in high-mannose-glykanen en scheidden die fysiek in drie hoofdgroepen: antilichamen met twee complexe suikers, met één complex en één high-mannose-suiker (asymmetrisch), of met twee high-mannose-suikers (symmetrisch). Ze verifieerden zorgvuldig dat deze groepen vrijwel identiek waren in alle andere opzichten: zelfde grootte, vorm, lading en stabiliteit, en vergelijkbare binding aan de recyclingsreceptor die antilichamen normaal beschermt tegen afbraak. Dat betekende dat eventuele verschillen die ze later in celproeven of in dieren zagen, teruggeleid konden worden naar alleen de suikerparing, niet naar verborgen schade of onzuiverheden.
Cellen zien antilichamen naar binnen trekken
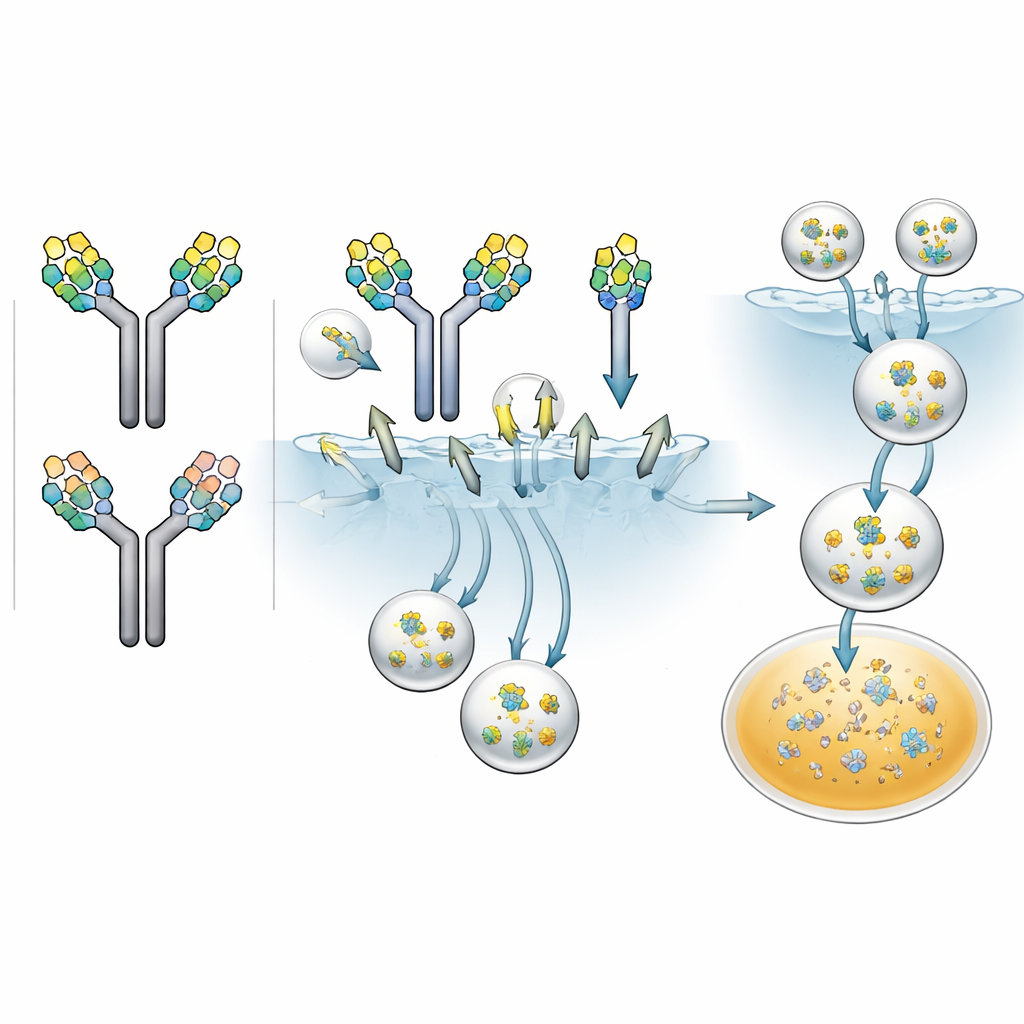
Vervolgens onderzochten de onderzoekers hoe snel elk suikerpatroon antilichamen door cellen met de mannosereceptor liet opnemen. Ze labelden de verschillende antilichaamfracties met een fluorescent label en incubeerden die met humane cellen die waren ontworpen om deze receptor te tonen. Gedurende bijna drie dagen volgden ze de gloed in de cellen als maat voor opname. Alle antilichamen werden tot op zekere hoogte opgenomen, maar de snelheden verschilden: die met twee high-mannose-suikers werden het snelst geïnternaliseerd, die met één high-mannose-suiker waren tussengesteld, en die met alleen complexe suikers het traagst. Toen het team mannan toevoegde—een natuurlijke suiker die concurreert om de mannosereceptor—viel de opname van de high-mannose-antilichamen sterk terug, wat bevestigde dat deze receptor verantwoordelijk was voor een groot deel van de snelle internalisatie.
Volgen van suikergemarkeerde antilichamen in levende dieren
De cruciale test was of deze celverschillen zich ook zouden vertalen naar echt geneesmiddelgedrag. De wetenschappers formuleerden een product met zowel symmetrische als asymmetrische high-mannose-paren, naast paren met alleen complexe suikers, en injecteerden dit in ratten. Met gevoelige massaspectrometriemethoden konden ze niet alleen het totale antilichaamgehalte over twee weken volgen, maar ook hoe elk suikerparingstype in de tijd afnam. Het patroon was opvallend: antilichamen met twee high-mannose-suikers verdwenen het snelst, met een halfwaardetijd van ongeveer 2,4 dagen; die met één high-mannose-suiker hielden langer aan, ongeveer 7,2 dagen; en die met alleen complexe suikers bleven ongeveer 17,4 dagen aanwezig. De blootstelling over tijd—de oppervlakte onder de concentratiecurve—daalde tot 38% voor het dubbele high-mannose-paar en 73% voor het gemengde paar vergeleken met het alleen-complexe paar. In wezen werkte elke extra high-mannose-suiker als een extra "ruim-me-op"-vlag voor de mannosereceptor.
Wat dit betekent voor veiligere, langer werkende geneesmiddelen
Voor patiënten verduidelijken deze resultaten waarom twee antilichaamgeneesmiddelen die op papier vergelijkbaar lijken, zich in het lichaam anders kunnen gedragen. De studie toont aan dat niet alleen de aanwezigheid maar ook de paring van high-mannose-suikers sterk bepaalt hoe snel antilichamen worden verwijderd, waarschijnlijk via mannosereceptor-gemedieerde opname en afbraak in immuuncellen. Omdat ditzelfde pad ook antigenen kan aanleveren aan de machinerie die immuunreacties activeert, kunnen deze suikerpatronen mogelijk het risico op anti-drug-antilichamen en allergische reacties beïnvloeden. De auteurs bepleiten dat fabrikanten glykaanparing—en niet alleen de totale suikercompositie—moeten monitoren en beheersen bij het ontwerpen en testen van antilichaamtherapieën. Dat kan helpen voorspelbaardere dosering, langduriger werkzaamheid en een lagere kans op ongewenste immuunreacties te waarborgen.
Bronvermelding: Baumeister, J., Meudt, M., Wei, W. et al. Selective clearance of monoclonal antibodies via the mannose receptor is dependent on glycan pairing. Sci Rep 16, 8489 (2026). https://doi.org/10.1038/s41598-026-40268-1
Trefwoorden: monoklonale antilichamen, glycosylering, mannosereceptor, farmacokinetiek, immunogeniciteit