Clear Sky Science · nl
Een geautomatiseerde beeldanalysepijplijn voor wijdveld optische redoxbeeldvorming van patiënt-afgeleide kankorganoïden
Waarom deze kankerbeeldvormingsstudie ertoe doet
Het vinden van het juiste geneesmiddel voor iemands kanker is nog steeds een traag, op toeval berustend proces. Deze studie pakt dat probleem aan door minuscule, in het laboratorium gekweekte tumoren van patiënten — zogenaamde organoïden — te combineren met een snelle, camera‑gebaseerde methode om te volgen hoe hun energiegebruik verandert wanneer geneesmiddelen worden toegediend. De auteurs tonen aan hoe een nieuwe geautomatiseerde computerpijplijn grote stapels microscoopbeelden kan doorzoeken, honderden organoïden dagenlang kan volgen en kan laten zien welke behandelingen werken, alles veel sneller en betrouwbaarder dan handmatig mogelijk zou zijn.
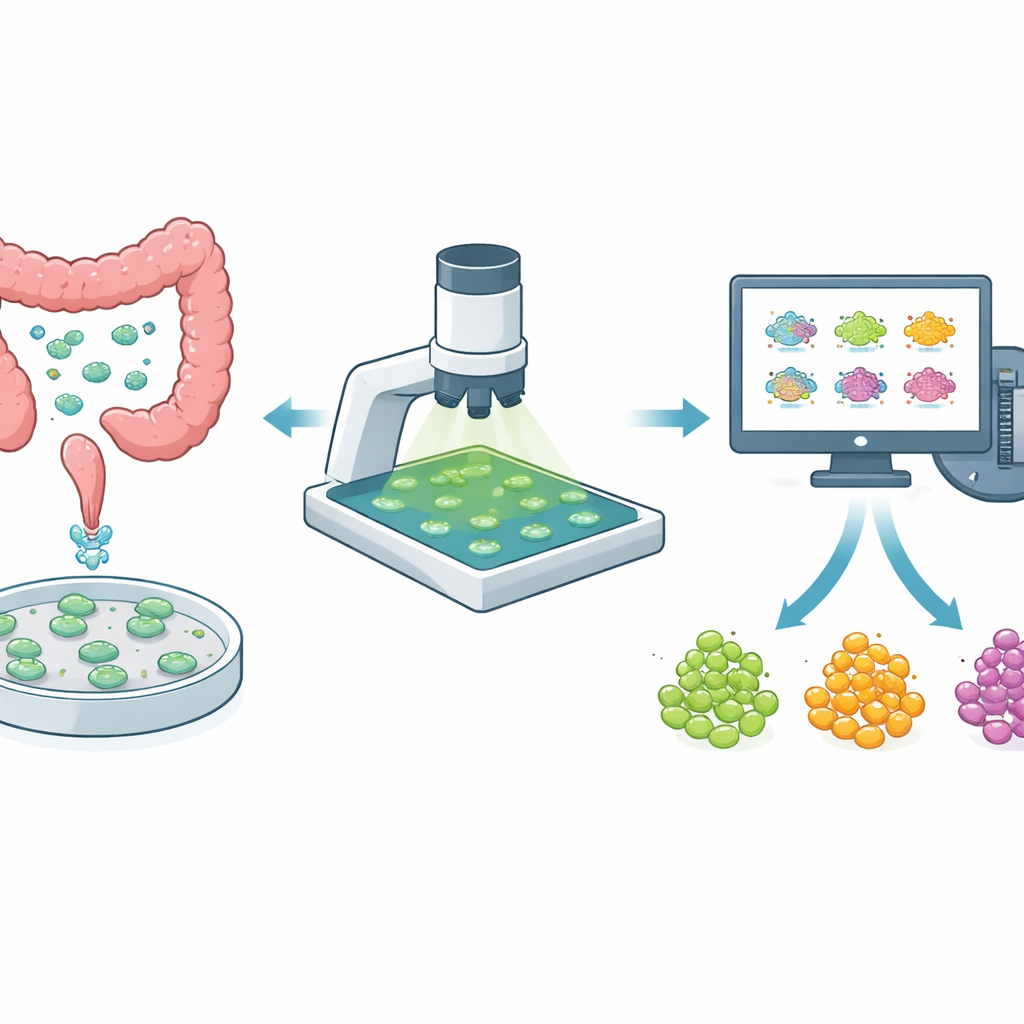
Mini‑tumoren in een schaaltje als testplatform
In plaats van alleen te vertrouwen op kankercellen die in platte lagen worden gekweekt, gebruiken onderzoekers nu vaak driedimensionale organoïden die direct uit een patiëntentumor zijn gemaakt. Deze mini‑tumoren behouden beter de mengeling van celtypen en de verborgen pockets van medicijnresistente cellen die in het lichaam aanwezig zijn. Bij dikkedarmkanker, waar tumoren sterk variëren tussen patiënten en zelfs binnen dezelfde patiënt, zijn organoïden een krachtig middel om te testen hoe goed nieuwe en bestaande geneesmiddelen werken. Maar om nuttig te zijn voor het sturen van behandelingen, moeten orgaan‑testen zowel zacht zijn—zodat hetzelfde organoïde in de tijd gevolgd kan worden—als snel genoeg om veel geneesmiddelen en doseringen te screenen.
Het ‘brandstofgebruik’ van tumoren zichtbaar maken met licht
Het team gebruikt een techniek die optische redoxbeeldvorming heet, gebaseerd op het zwakke, natuurlijke gloedje van moleculen in cellen die betrokken zijn bij energieproductie. Door specifieke kleuren licht te laten schijnen en de uitgestraalde gloed op te vangen, kan een eenvoudige wijdveldmicroscoop een kaart maken van hoe “geoxideerd” of “gereduceerd” elk organoïde is—een momentopname van zijn metabolische toestand. In tegenstelling tot complexere high‑end microscopen gebruikt deze opstelling standaardcomponenten die veel laboratoria al bezitten, waardoor de methode relatief makkelijk te adopteren is. Veranderingen in dit redoxsignaal verschijnen vaak eerder dan veranderingen in orgaan‑grootte of celdood, waardoor het een vroeg waarschuwingssignaal wordt of een geneesmiddel helpt of faalt.
Ruwe beelden omzetten in betrouwbare cijfers
Tot nu toe betekende het analyseren van deze beelden dat iemand met de hand omtrekken van elk organoïde moest tekenen, achtergrondgebieden met het blote oog moest kiezen en vervolgens moest proberen elk organoïde door meerdere dagen heen te volgen. Die trage, foutgevoelige aanpak is niet geschikt voor grootschalige geneesmiddelschermen. De auteurs ontwikkelden een end‑to‑end geautomatiseerde pijplijn die drie lastige taken uitvoert: elk organoïde nauwkeurig scheiden van de omgeving, elk exemplaar een consistente identiteit geven over meerdere dagen heen, en het achtergrondsignaal inschatten op een manier die menselijke vooringenomenheid vermijdt. Ze hebben een bestaand kunstmatig‑intelligentietool (Cellpose) fijn afgestemd om organoïden te herkennen, zelfs wanneer deze in vorm, grootte en scherpte variëren, en bouwden vervolgens een volgalgoritme dat beelden van verschillende dagen op elkaar afstemt en organoïden matcht op basis van overlap in vorm en positie.
Inzoomen op de meest actieve rand
Organoïden hebben onderscheidende zones: een dode of stervende kern, een rustige middensectie en een levendige buitenrand waar cellen actief groeien en vaak het meest gevoelig zijn voor behandeling. De pijplijn snijdt automatisch deze dunne buitenring — de zogenaamde voortschrijdende rand — uit voor elk organoïde en berekent daar de redoxwaarde van. Door diezelfde voortschrijdende rand van een organoïde drie dagen lang te volgen tijdens behandeling met verschillende doseringen van het geneesmiddel romidepsine, kan de software subtiele verschuivingen in het metabolisme detecteren. De auteurs tonen aan dat deze organoïde‑per‑organoïde opvolging de variatie vermindert vergeleken met het samenvoegen van alle organoïden, waardoor de statistische kracht om geneesmiddel‑effecten te zien toeneemt, zelfs wanneer reacties per mini‑tumor verschillen.
Snellere, robuustere inzichten in medicijnrespons
De onderzoekers hebben hun pijplijn getest op beelden van twee verschillende microscopen en vonden dat de geautomatiseerde omtrekken nauw overeenkwamen met door experts getekende omtrekken, en dat het volgen overeenkwam met handmatig volgen in meer dan 94 procent van de gevallen. Wanneer ze de algemene maatstaven voor medicijnrespons vergeleken, matchte de geautomatiseerde methode de gevoeligheid van de manuele benadering, terwijl de analysetijd met meer dan honderdvoud werd teruggebracht—van vele uren menselijke inspanning tot slechts een paar minuten computerverwerking. Voor laboratoria die met patiënt‑afgeleide organoïden werken betekent dit dat ze realistisch grote beeldcollecties kunnen analyseren en kunnen ontdekken hoe elk mini‑tumor op behandeling reageert. Op de lange termijn kan zulke geautomatiseerde analyse helpen om organoïde‑gebaseerde medicijntests dichter bij de kliniek te brengen, en zo meer gepersonaliseerde en effectieve kankerzorg ondersteunen.
Bronvermelding: Hsu, A., Samimi, K., Gillette, A.A. et al. An automated image analysis pipeline for wide-field optical redox imaging of patient-derived cancer organoids. Sci Rep 16, 9757 (2026). https://doi.org/10.1038/s41598-026-40249-4
Trefwoorden: dikkedarmkanker, patiënt-afgeleide organoïden, optische redoxbeeldvorming, geautomatiseerde beeldanalyse, medicijnrespons