Clear Sky Science · nl
β-adrenerge receptoren moduleren CA1-populatiecodering en synaptische plasticiteit tijdens cumulatieve ruimtememorievorming en -bijwerking
Waarom deze hersenstudie ertoe doet
Herinneren waar je je auto hebt geparkeerd of welke keukenkastje de schaar bevat, hangt af van het vermogen van de hersenen om “wat” en “waar” met elkaar te verbinden over herhaalde ervaringen. Deze studie kijkt in een belangrijk geheugenknooppunt in de hersenen, de hippocampus, om te zien hoe groepen zenuwcellen deze ruimtememorieën in de loop van de tijd opbouwen en bijwerken — en hoe een veelvoorkomend stressgerelateerd chemisch signaal, werkend via zogenoemde bèta-receptoren, helpt die herinneringen flexibel en nauwkeurig te houden.
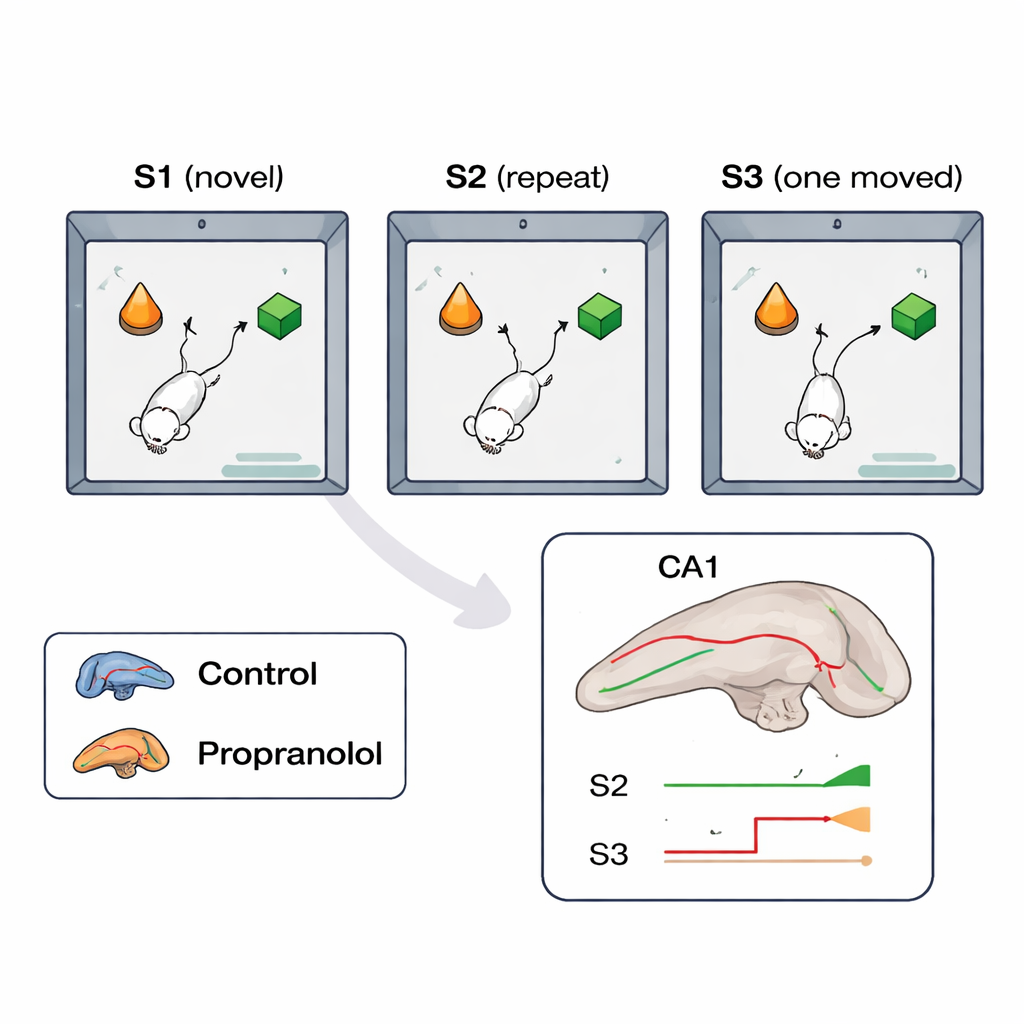
Een kleine wereld verkennen om geheugen te bestuderen
De onderzoekers trainden muizen in een eenvoudige taak: verken twee objecten die in een klein vierkant arena zijn geplaatst. In de eerste sessie waren de objecten en hun locaties nieuw. Een uur later keerden de muizen terug naar precies dezelfde opstelling. Na nog een uur werd één object ongemerkt naar een nieuwe plek verplaatst. Normaal gesproken besteden muizen meer tijd aan het onderzoeken van een verplaatst object, wat aangeeft dat ze de verandering opmerkten en zich de oorspronkelijke indeling herinneren. Tegelijkertijd registreerde het team de hersenactiviteit van honderden cellen in een hippocampale regio genaamd CA1 met een op het hoofd gemonteerde microscoop, en in een aparte groep dieren maten ze elektrische signalen die onthullen hoe sterk zenuwverbindingen worden versterkt of verzwakt.
Blokkeren van een sleutelchemisch signaal belemmert leren
Om de rol van bèta-adrenerge receptoren — doelwitten van de neurotransmitter noradrenaline — te testen, gaven de wetenschappers sommige muizen propranolol, een middel dat deze receptoren blokkeert, kort voor de eerste leersessie. Controlemuizen gedroegen zich zoals verwacht: ze verkenden minder bij het tweede bezoek, wat suggereert dat de scène nu vertrouwd was, en in de derde sessie gaven ze duidelijk de voorkeur aan het verplaatste object, wat wijst op succesvolle geheugenvorming en bijwerking. Daarentegen toonden propranolol-behandelde muizen geen sterke voorkeur voor het verplaatste object, wat impliceert dat hun vermogen om de object–locatiegeheugen te vormen en bij te werken verstoord was. In de hippocampus van onbehandelde muizen leidden nieuwe en gewijzigde objectindelingen tot een blijvende verzwakking van bepaalde synapsen, een vorm van plasticiteit die langetermijndepressie wordt genoemd; deze synaptische aanpassing trad niet goed op wanneer bèta-receptoren werden geblokkeerd.
Hoe cellengroepen “wat waar was” coderen
Bij het kijken naar individuele cellen en celgroepen vonden de auteurs dat bij normale muizen CA1-neuronen op een georganiseerde manier werden gerekruteerd over de drie sessies. Veel van dezelfde cellen gingen weer aan toen de dieren het ongewijzigde arena opnieuw betraden, wat consistent is met het reactiveren van een bestaande herinnering. Toen één object werd verplaatst, verschoof echter het patroon van actieve cellen, alsof het netwerk zijn interne kaart bijwerkte. Cellen waarvan de activiteit specifieke locaties bijhield — “plaatscelachtige” neuronen — werden met ervaring preciezer en coherenter, en meer van hen concentreerden hun activiteit rond de objecten, vooral nadat de indeling veranderde. Wanneer bèta-receptoren werden geblokkeerd, sloten zich minder neuronen vroeg aan bij het ensemble, waren hun reactiveringspatronen veranderd, en werd ruimtelijke afstemming minder coherent en minder verbonden met de objecten, wat wijst op een vager en minder aanpasbaar intern kaartbeeld.
Hersenritmes en netwerken onder chemische controle
Men denkt dat herinneringen worden versterkt door korte, sterk gesynchroniseerde uitbarstingen van activiteit waarbij veel neuronen tegelijk betrokken zijn. Bij controledieren waren dergelijke populatie-uitbarstingen in CA1 frequent tijdens leren en herinneren, consistent met actieve consolidatie van het ruimtememoriseren. Propranolol verminderde zowel het aantal als de sterkte van deze uitbarstingen, wat suggereert dat het middel het gecoördineerde vuren dat nodig is om herinneringen te stabiliseren verzwakt. Netwerkanalyses die de geregistreerde cellen als een verbonden graaf behandelden, toonden aan dat het CA1-circuit bij normale dieren evolueerde van een schaars, efficiënt patroon naar een dichter, meer modulair organisatiepatroon naarmate leren en bijwerking zich ontvouwden — een architectuur die goed geschikt is om nieuwe informatie te integreren terwijl het oude behouden blijft. Onder blokkade van bèta-receptoren werd deze evolutie verstoord: verbindingen werden ofwel overdreven redundant of te diffuus, en het netwerk slaagde er niet in te reorganiseren op een manier die oude en nieuwe ruimtelijke informatie duidelijk scheidt.
Wat dit betekent voor geheugen en geest
Samengevat laten de resultaten zien dat bèta-adrenerge receptoren helpen het geheugen te orkestreren door zowel de sterkte van individuele verbindingen als de collectieve dynamiek van hippocampale circuits te verfijnen. Wanneer deze receptoren actief zijn, vormen CA1-neuronen precieze, aan objecten gekoppelde kaarten, hergebruiken ze geschikte ensembles wanneer de wereld vertrouwd is, en rekruteren ze flexibel nieuwe patronen wanneer er iets verandert. Het blokkeren van de receptoren dooft dit proces, wat leidt tot zwakkere synaptische aanpassingen, minder gecoördineerde uitbarstingen en netwerktoestanden die minder goed onderscheid maken tussen nieuwe en vertrouwde situaties. Voor niet-specialistische lezers benadrukt dit werk hoe één chemisch signaleringssysteem niet alleen beïnvloedt of we herinneringen vormen, maar ook hoe soepel we ze kunnen bijwerken naarmate onze omgeving verandert.
Bronvermelding: Shendye, N., Haubrich, J., Weber, J.P. et al. β-adrenergic receptors modulate CA1 population coding and synaptic plasticity during cumulative spatial memory formation and updating. Sci Rep 16, 7390 (2026). https://doi.org/10.1038/s41598-026-40218-x
Trefwoorden: ruimtememorie, hippocampus, noradrenaline, synaptische plasticiteit, neurale ensembles