Clear Sky Science · nl
Multimodale karakterisering van door stroming veroorzaakte trombusinitiatie en -groei in extracorporele membraanoxygenatie
Waarom bloedstolsels in levensondersteunende machines ertoe doen
Extracorporele membraanoxygenatie, of ECMO, is een vorm van hart‑longbypass die kritisch zieke patiënten in leven kan houden terwijl hun organen herstellen. Maar bloed door pompen en kunststof buizen laten lopen stelt het bloot aan sterke mechanische krachten waarvoor ons lichaam niet ontworpen is. Deze krachten kunnen gevaarlijke bloedstolsels in het circuit uitlokken, wat het risico op beroerte, orgaanschade of uitval van het apparaat verhoogt. Deze studie had tot doel te achterhalen hoe precies de bloedstroom door een ECMO‑pomp de vorming en groei van zulke stolsels beïnvloedt, met het lange termijn‑doel ECMO veiliger en effectiever te maken.
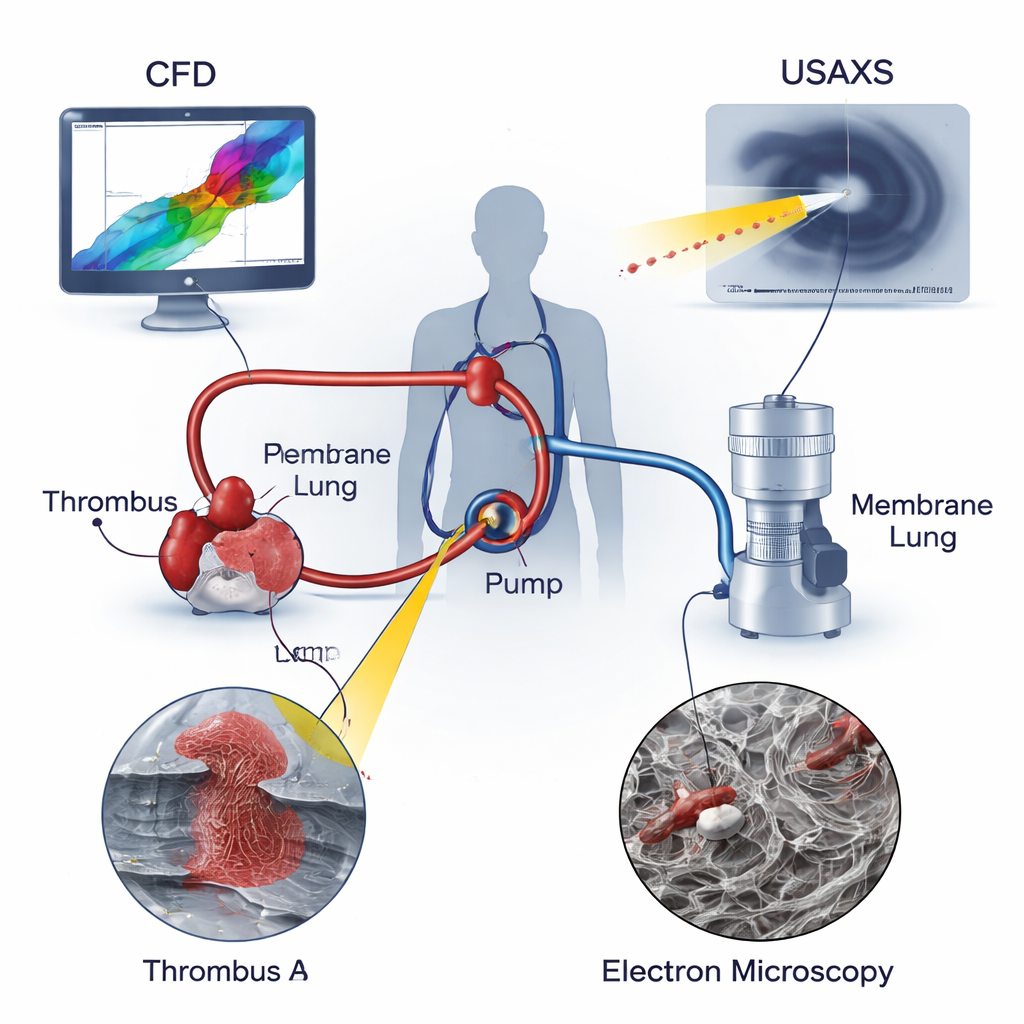
Hoe ECMO patiënten in leven houdt
Bij ECMO wordt bloed uit een grote ader of slagader weggezogen, door een centrifugaalpomp geduwd via een “membraanlong” die zuurstof toevoegt en kooldioxide verwijdert, en vervolgens teruggevoerd naar de patiënt. In tegenstelling tot bloed dat soepel door natuurlijke vaten stroomt, kent de stroming in een ECMO‑circuit extreme omstandigheden: zeer snelle stromen, scherpe richtingsveranderingen en bijna stilstaande zones waar bloed blijft hangen. Deze omgevingen beschadigen bloedcellen en stimuleren stolling. Klassieke medische modellen richten zich op langzame of geblokkeerde stroming in bloedvaten, maar houden geen volledige rekening met de intense schuif‑ en rekspanningen die bloed in een draaiende pomp ondervindt. De auteurs betogen dat om het stolrisico in ECMO echt te begrijpen, zowel de mechanische krachten in het apparaat als de microscopische structuur van de gevormde stolsels bestudeerd moeten worden.
Stolsels vanuit drie invalshoeken bekeken
De onderzoekers combineerden drie krachtige instrumenten om twee echte stolsels afkomstig uit ECMO‑circuits bij kinderen te analyseren: één stolsel bij de pomp‑inlaat (Trombus A) en een ander in de buisvoering net stroomafwaarts van de pomp (Trombus B). Computational fluid dynamics (CFD) simuleerde hoe het bloed door de pomp bewoog, waarbij regio’s met recirculerende en draaiende stroming zichtbaar werden en plaatsen waar schuif‑ en rekspanningen piekten werden gelokaliseerd. Ultra-small-angle X-ray scattering (USAXS) drong diep door in elk stolsel en mat hoe dicht de fibrinestructuur—het eiwitgaas dat stolsels bijeenhoudt—ingepakt was en in welke mate de vezels richtinggeoriënteerd waren door het monster heen. Scanning electron microscopy (SEM) leverde sterk vergrote beelden van de stolseloppervlakken, waarin de vormen van rode en witte bloedcellen, bloedplaatjes en de omringende fibrinedraden zichtbaar werden. Door deze drie aanzichten te combineren, kon het team lokale stromingscondities koppelen aan de interne architectuur van elk stolsel.
Een recirculatiezone vormt een stijv, uitgelijnd stolsel
CFD toonde dat het gebied nabij de pomp‑inlaat, waar Trombus A zich vormde, een recirculatiezone bevatte: bloed werd terug en omhoog langs de behuizing geduwd voordat het weer bij de hoofdstroom aansloot. Deze regio liet bloedbestanddelen langer verblijven en kende scherpe snelheidsonderscheidingen aan de grens tussen recirculerende en binnenkomende stroming. Binnen Trombus A toonde USAXS een hoog fibrinegehalte—ten minste 70 procent—en een sterke algehele uitlijning van vezels in een voorkeursrichting, wat duidt op een dicht, stijv geraamte. SEM‑beelden bevestigden een dicht geweven netwerk van fibrine, doorspekt met abnormaal gevormde rode bloedcellen en fragmenten van bloedplaatjes. De auteurs stellen dat de combinatie van lange verblijftijden en sterke lokale schuifkrachten de groei van een compact, sterk georganiseerd stolsel bevorderde dat bestand is tegen de mechanische belastingen van de pomp.
Draaierige uitstroming vormt een lossere, gedraaide stolsel
In contrast daarmee groeide Trombus B, genomen uit buiswerk na de pomp, in een regio gedomineerd door draaiende uitstroming. CFD onthulde roterende, spiraalachtige stromingsstructuren die uit het pompuitlaatgebied voortkwamen, en de USAXS‑gegevens lieten een fibrinenetwerk zien dat weliswaar dominant bleef maar minder dicht en minder sterk uitgelijnd was. De hoofdrichting van fibrineoriëntatie verschuift geleidelijk door het stolsel, van de ene hellingshoek naar de andere, wat het gekruiste stromingspatroon weerspiegelt. SEM‑beelden toonden fibrinedraden van wisselende dikte en talrijke gevangen rode en witte bloedcellen, inclusief aanwijzingen voor celschade en ontsteking. Belangrijk is dat de simulaties ook kleine maar significante delen van het pompvolume identificeerden waar rekspanningen hoog genoeg waren om von Willebrand‑factor te ontvouwen, een sleuteleiwit dat onder spanning plakkerig wordt en snel bloedplaatjes kan aantrekken. Deze zones concentreerden zich nabij de schoepen van de impulsgever en de uitlaat, waardoor ze waarschijnlijke locaties zijn voor de initiële activatiegebeurtenissen die leidden tot Trombus B.
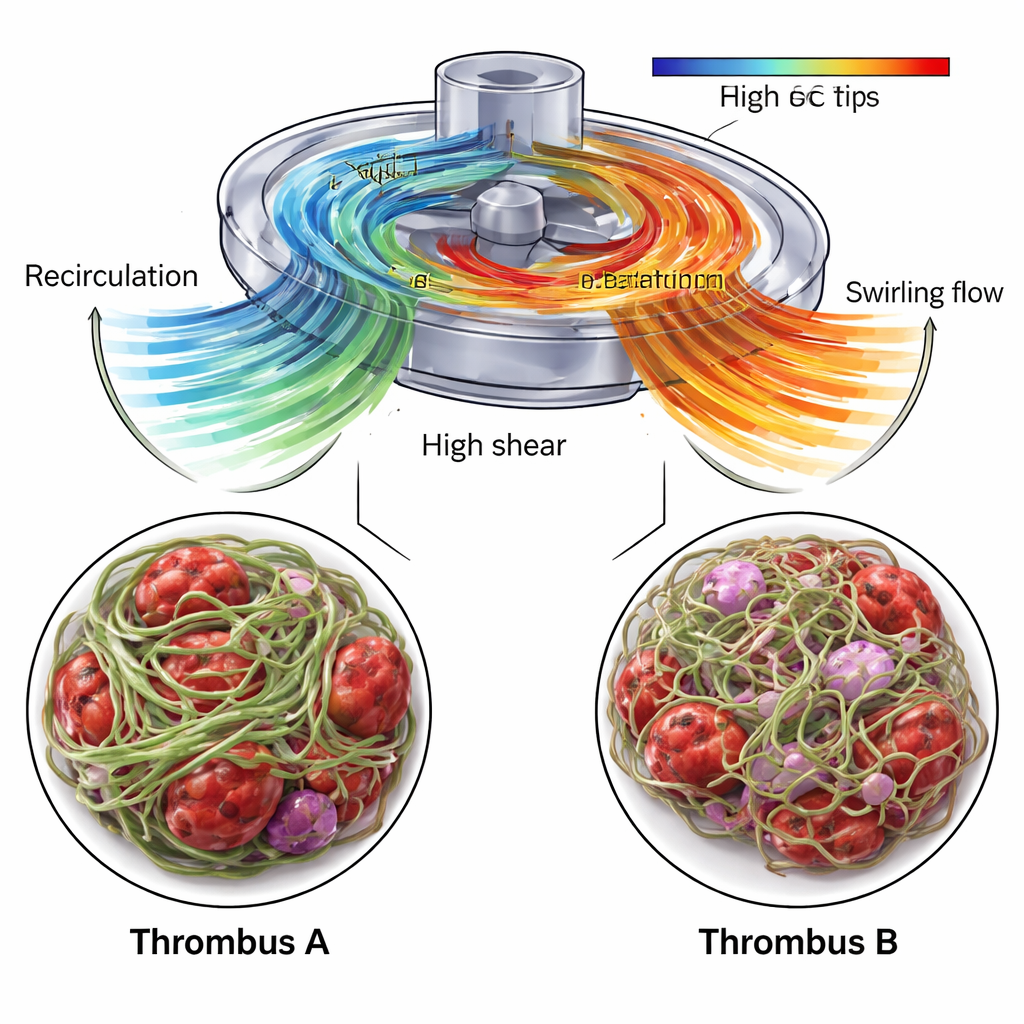
Op weg naar veiligere levensondersteunende machines
Door gedetailleerde stromingssimulaties van bloed te combineren met röntgen‑ en elektronenmicroscoopmetingen van echte ECMO‑stolsels, laat dit werk zien dat de interne “structuur” en dichtheid van een stolsel de mechanische omgeving weerspiegelt waarin het gevormd is. Recirculerende stroming nabij de pomp‑inlaat werd gekoppeld aan een dicht, sterk uitgelijnd fibrineraamwerk, terwijl draaiende uitstroming geassocieerd was met een meer gedraaid, open netwerk dat toch veel bloed‑ en immuuncellen vasthield. Deze inzichten wijzen op specifieke regio’s in ECMO‑pompen en buiswerk waar ontwerpswijzigingen of gerichte aanpassingen van anticoagulatie het stolrisico het meest effectief zouden kunnen verminderen. Op de lange termijn kan dergelijke multiscale‑kaarten—van pompprofiel en stromingspatronen tot eiwitrangschikking—leidraad zijn voor veiligere apparaatsontwerpen en hulp bieden aan clinici om het delicate evenwicht tussen bloedingsrisico en trombose tijdens levensreddende ECMO‑ondersteuning beter te beheren.
Bronvermelding: Nilsson, F., Sochor, B., Henriksson, S. et al. Multimodal characterization of flow-induced thrombus initiation and growth in extracorporeal membrane oxygenation. Sci Rep 16, 7166 (2026). https://doi.org/10.1038/s41598-026-40177-3
Trefwoorden: ECMO, bloedstolling, schuifspanning, centrifugaalpomp voor bloed, fibrinestructuur