Clear Sky Science · nl
Machine-learning–geïnspireerde transcriptomische integratie identificeert GFM1 als een lactylatie-gerelateerd kandidaat-biomarker bij aortadissectie
Waarom deze verborgen bedreiging in de aorta ertoe doet
Aortadissectie is een medische noodsituatie waarbij een scheur in de wand van de grote lichaamsslagader binnen enkele uren levensbedreigende inwendige bloedingen kan veroorzaken. Artsen kunnen patiënten vaak redden met spoedchirurgie, maar er bestaan nog geen betrouwbare bloedtesten die vroegtijdig waarschuwen of geneesmiddelen die de ziekte zelf remmen. Deze studie onderzoekt of subtiele verschuivingen in hoe arteriële cellen energie en chemische signalen verwerken, nieuwe waarschuwingssignalen kunnen onthullen. De focus ligt op een weinig bekend gen genaamd GFM1, dat mogelijk een link vormt tussen celmetabolisme en verzwakking van de aortawand.
De code van een gevaarlijke scheur kraken
Bij aortadissectie dringt bloed de wand van de aorta binnen en splitst deze lagen van elkaar. Waarom de aorta van sommige mensen op deze manier faalt, is nog niet volledig begrepen. De auteurs onderzochten patronen van genexpressie in monsters van mensen met aortadissectie en van individuen met gezonde aortas. Ze besteedden speciale aandacht aan genen die verband houden met “lactylatie,” een recent ontdekte manier waarop cellen lactaat — beter bekend als de stof die zich ophoopt in spieren tijdens zware inspanning — gebruiken om eiwitten en genregulatie fijn af te stemmen. Omdat lactylatie in verband is gebracht met ontsteking en weefselremodellering, vermoedde het team dat lactaat-gerelateerde genen ook een rol kunnen spelen bij het beschadigen van de aortawand.
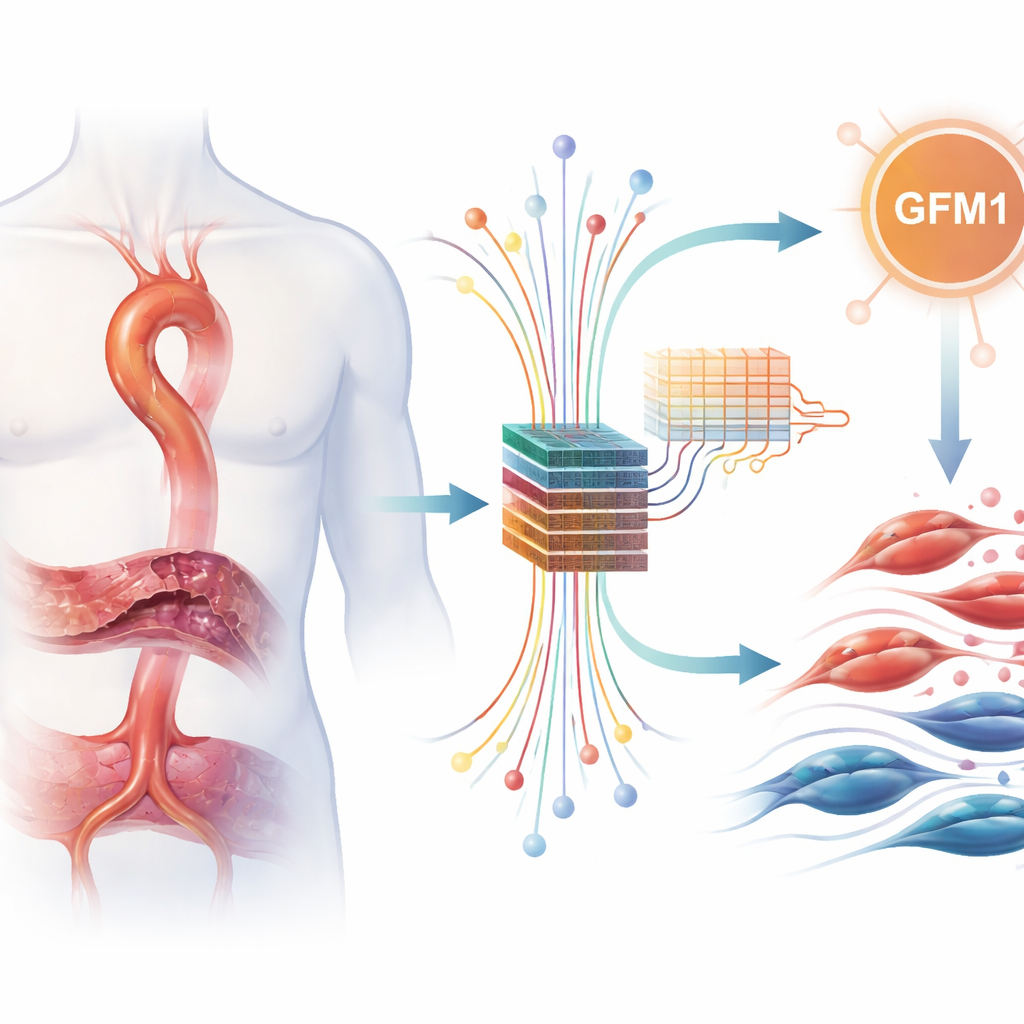
Grote datasets delven met slimme algoritmen
Om dit idee te toetsen, bundelden de onderzoekers verschillende openbaar beschikbare datasets die vastleggen welke genen in aortaweefsel aan- of uitstaan. Ze corrigeerden zorgvuldig voor technische verschillen tussen studies en zochten vervolgens naar genen waarvan de activiteit consequent verschilde tussen zieke en gezonde monsters. Uit duizenden genen vonden ze 217 met duidelijke veranderingen, waarvan vele wezen op immuunreacties en remodellering van het weefselraamwerk dat de aorta ondersteunt. Vervolgens richtten ze zich op een samengestelde lijst van genen die verband houden met lactaatverwerking en lactylatie en identificeerden 11 genen die zowel veranderd waren bij aortadissectie als deel uitmaakten van deze lactaat-gerelateerde programma’s.
Machines laten stemmen over een belangrijke verdachte
Elf interessante genen waren nog steeds te veel om diepgaand in het lab te bestuderen, dus wendde het team zich tot machine-learningmethoden als een objectief “votesysteem.” Ze voerden de gegevens voor deze genen in drie verschillende modellen — LASSO, Random Forest en XGBoost — die vaak worden gebruikt om patronen te selecteren die patiënten het beste van controles onderscheiden. Elke methode belichtte haar eigen favorieten, maar slechts één gen, GFM1, werd sterk en consistent gekozen door alle drie. Deze kruiscontrole maakte GFM1 onderscheidend als een bijzonder robuuste kandidaat-marker, ook al werden de modellen gebruikt voor rangschikking en niet voor het bouwen van een kant-en-klare diagnostische test.
Inzoomen op spiercellen van de arterie
GFM1 helpt regelen hoe mitochondriën, de energiecentrales in cellen, hun eigen eiwitten opbouwen. Omdat energiebalans cruciaal is voor het gedrag van cellen in de aortawand, onderzochten de auteurs GFM1 nader. Ze bevestigden dat GFM1-niveaus hoger waren in weefsel van patiënten met aortadissectie dan in niet-zieke aortas. Daarna gingen ze over naar een gecontroleerd celkweekmodel met muizen vasculaire gladde spiercellen — de spierachtige cellen die de aorta zijn stevigheid geven. Wanneer deze cellen werden gestimuleerd met angiotensine II, een hormoon dat verband houdt met hoge bloeddruk en vaatstress, gingen ze makkelijker delen en migreren, wat schadelijke veranderingen nabootst die in zieke arteriën worden gezien. Toen de onderzoekers met kleine interfererende RNA’s (siRNA) GFM1 in deze cellen verlaagden, werd de door angiotensine aangedreven groei en migratie merkbaar verminderd, wat suggereert dat GFM1 deze risicovolle gedragingen bevordert.
Wat dit betekent en wat het nog niet bewijst
Samen suggereren de bevindingen dat GFM1 mogelijk fungeert als een brug tussen veranderd celmetabolisme en het agressieve gedrag van cellen in de aortawand bij aortadissectie. In eenvoudige termen lijkt hogere GFM1-activiteit samen te gaan met een instabielere, schadegevoelige aorta, en het omlaag brengen ervan in kweekcellen maakt ze minder geneigd tot overgroei en migratie. De auteurs benadrukken echter dat dit werk nog in een vroeg, hypothesevormend stadium verkeert. Ze maten lactylatie niet direct in weefsels en bewezen niet dat GFM1 zelf chemisch op deze manier is gewijzigd, en de voorspellende kracht van de modellen is niet getest in onafhankelijke patiëntengroepen. Toekomstig onderzoek zal deze resultaten in grotere cohorten moeten bevestigen en precies moeten uitzoeken hoe GFM1 en verwante metabole veranderingen de aortawand verzwakken. Als die inspanningen slagen, zouden GFM1 of gerelateerde paden uiteindelijk doelwitten kunnen worden voor nieuwe bloedtesten of behandelingen die gericht zijn op het voorkomen van deze vaak fatale scheur voordat die optreedt.
Bronvermelding: Chen, J., Jiang, N., Guo, Z. et al. Machine-learning–guided transcriptomic integration identifies GFM1 as a lactylation-related candidate biomarker in aortic dissection. Sci Rep 16, 9033 (2026). https://doi.org/10.1038/s41598-026-40139-9
Trefwoorden: aortadissectie, vasculaire gladde spiercellen, lactaatmetabolisme, mitochondriale functie, biomarkerontdekking