Clear Sky Science · nl
Evaluatie van de werkzaamheid van bacteriofagen tegen Pseudomonas aeruginosa in ex vivo en in vitro hondelijke huidsystemen
Waarom huidinfecties nieuwe oplossingen nodig hebben
Hardnekkige huidinfecties zijn niet alleen een bron van ergernis voor huisdieren en hun eigenaren—they kunnen uitgroeien tot langdurige, pijnlijke problemen die standaardanibiotica weerstaan. Een veelvoorkomende veroorzaker is Pseudomonas aeruginosa, een moeilijk te doden bacterie die goed gedijt in slijmerige biofilms op wonden. Deze studie onderzoekt of virussen die bacteriën infecteren, bacteriofagen of kortweg fagen genoemd, deze infecties veilig kunnen opruimen in hondlijke huidmodellen, wat wijst op nieuwe opties die op termijn zowel dieren als mensen kunnen helpen.
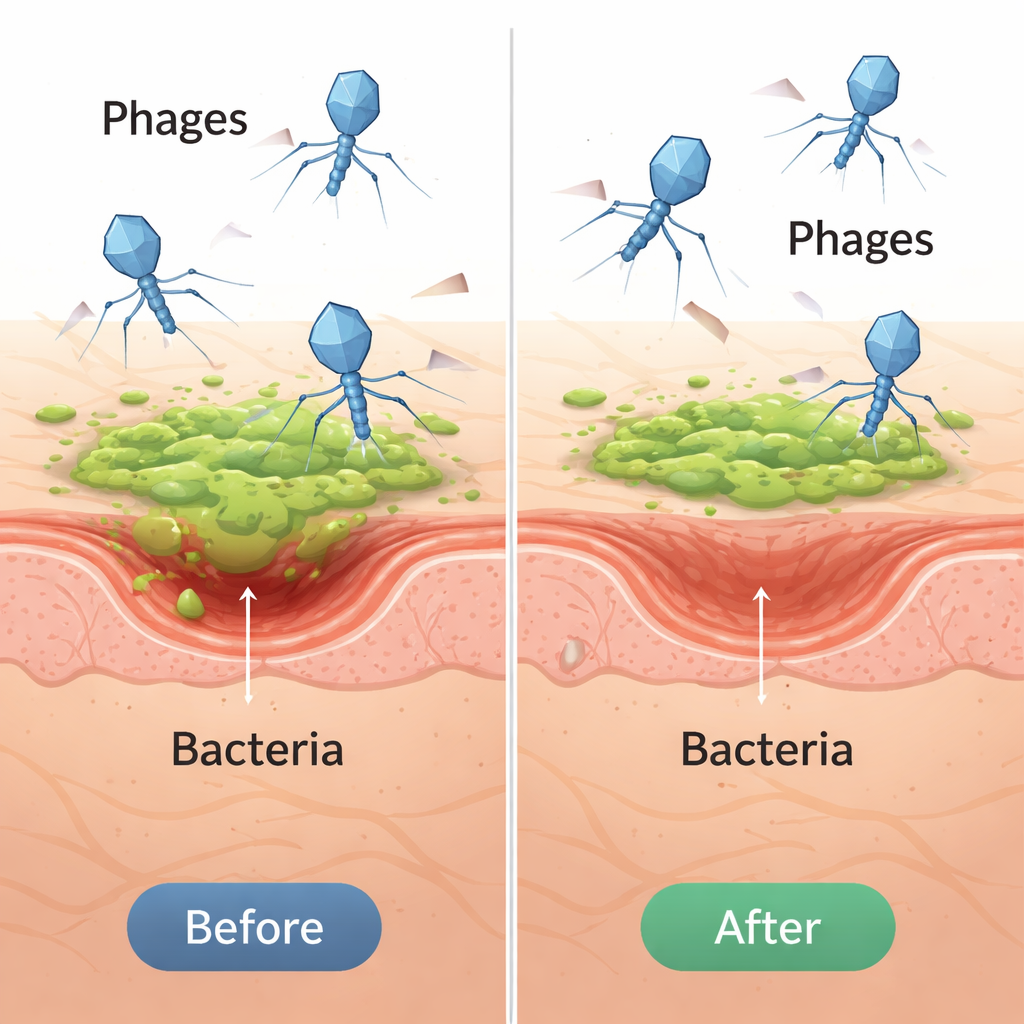
Een taaie kiem die van slijm houdt
Pseudomonas aeruginosa is een opportunistische kiem die toeslaat wanneer de afweer verzwakt is en ernstige long-, bloed- en wondinfecties veroorzaakt in ziekenhuizen en veterinaire klinieken. Deze bacterie groeit vaak in biofilms—dunne, kleverige lagen bacteriën die aan elkaar zijn gekleefd door een beschermend matrix. Binnen deze films zijn de microben veel moeilijker te bereiken met antibiotica en kunnen ze het immuunsysteem beter ontwijken, waardoor behandelbare infecties chronisch kunnen worden. Omdat multiresistente Pseudomonas nu op de lijst met hoge prioriteit van de Wereldgezondheidsorganisatie staat, zoeken onderzoekers dringend naar alternatieven voor traditionele medicijnen.
Virussen die jagen op bacteriën
Bacteriofagen zijn van nature voorkomende virussen die bacteriën infecteren en doden, terwijl dierlijke en menselijke cellen onaangetast blijven. Het team richtte zich op twee goed gekarakteriseerde fagen, JG003 en PTLAW1, gekozen omdat ze sterk lytisch zijn en genen dragen die mogelijk helpen biofilms af te breken. Eerst testten de onderzoekers deze fagen op in het laboratorium gekweekte Pseudomonas-biofilms die op plastic platen waren gevormd. Met behulp van fluorescerende kleurstoffen en 3D-confocale microscopie lieten ze zien dat elke faag op zichzelf—en vooral het paar samen—de totale biofilmvolume aanzienlijk verminderde en het aandeel bacteriën met beschadigde membranen verhoogde, wat wijst op een effectieve aanval op de bacteriegemeenschap.
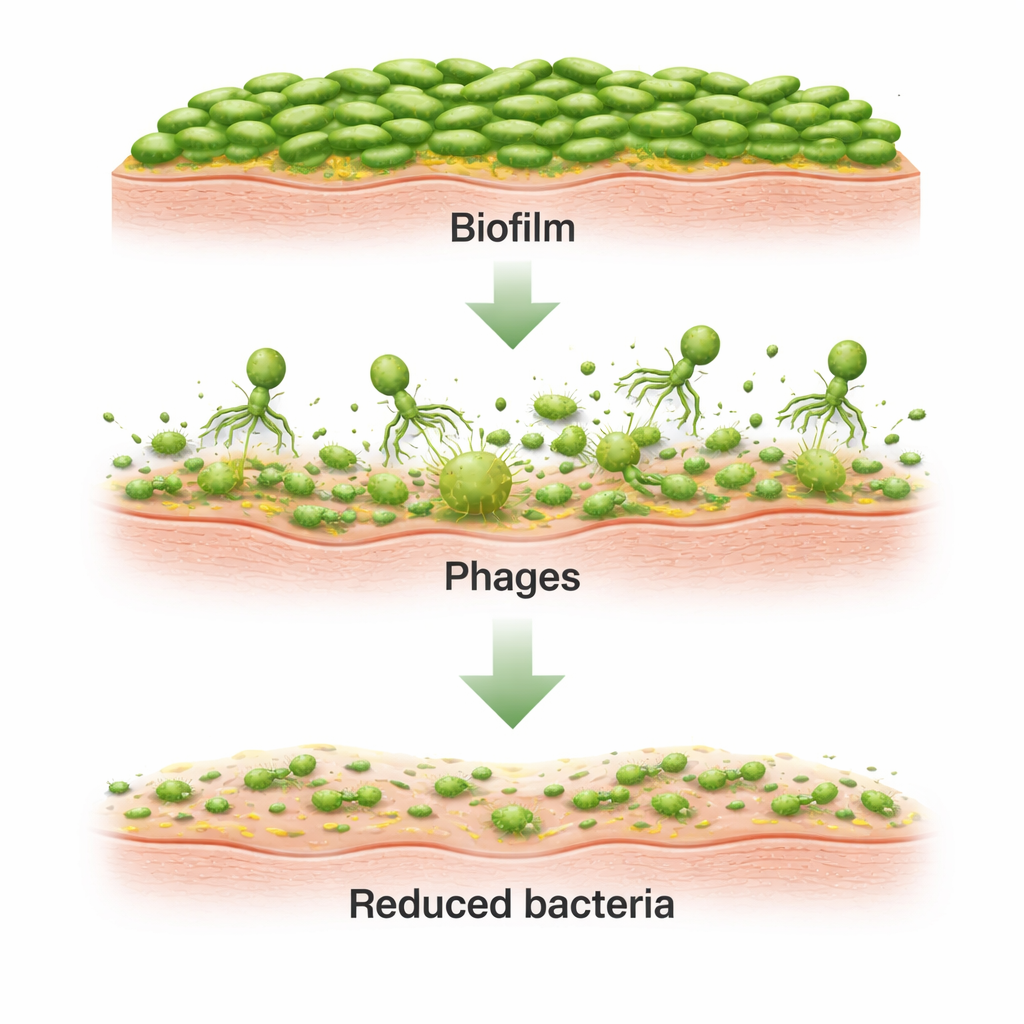
Fagen toepassen op echte hondenhuid
Biofilms op plastic zijn veel eenvoudiger dan echte huid, die lagen, haarzakjes, klieren en een stevige buitenbarrière heeft. Om meer realistische omstandigheden na te bootsen, gebruikten de onderzoekers twee canine huidsystemen. In een ex vivo-opstelling werden dunne schijfjes hondenhuid gemonteerd in Franz‑type diffusiecellen—glazen apparaten met een donor‑kamer boven en een receptor‑kamer onder de huid. Nadat het oppervlak gedurende 16 uur was geïnfecteerd met Pseudomonas, brachten ze een cocktail van de twee fagen aan. In de daaropvolgende acht uur daalden de bacterietellingen in de huid met ongeveer vier logorders vergeleken met onbehandelde monsters. Microscopie bevestigde dat dicht opeengepakte clusters bacteriën en biofilmmatrix op het huidoppervlak grotendeels waren afgebroken na blootstelling aan fagen, terwijl de fagen zelf actief bleven maar niet doorgingen naar de onderste kamer.
Een levend huidmodel dat ontsteking kan voelen
Vervolgens teelden de wetenschappers een levend “epidermaal equivalent” uit hondecellen op permeabele insertjes, waarmee de buitenste huidlagen inclusief een juiste verhoornde oppervlakte werden nagebootst. Dit stelde hen niet alleen in staat bacteriële overleving te meten maar ook ontstekingssignalen te volgen. Toen deze huidequivalenten werden geïnfecteerd met een klein aantal Pseudomonas‑cellen en drie uur later werden behandeld met de faagcocktail, kelderden de bacterieniveaus—in de meeste behandelde monsters waren geen bacteriën meer detecteerbaar. Tegelijkertijd daalden de niveaus van de pro‑inflammatoire boodschapper CXCL8, die sterk stijgt tijdens infectie, zowel op gen- als eiwitniveau weer richting normaal. Belangrijk is dat blootstelling aan fagen alleen de huidcellen of de barrièrestructuur niet beschadigde.
Wat dit betekent voor toekomstige wondzorg
Gezamenlijk tonen deze experimenten aan dat zorgvuldig geselecteerde fagen Pseudomonas‑biofilms doelgericht kunnen aantasten, bacteriële ladingen kunnen verlagen en vroege ontsteking kunnen kalmeren in realistische hondelijke huidmodellen, zonder duidelijke bijwerkingen. Hoewel de behandelingen zwaar geïnfecteerde huid niet volledig steriliseren en vooral op vroege biofilms werden getest, biedt het werk een reproduceerbaar preklinisch kader om faagdoses, timing en combinaties te verfijnen—mogelijk naast antibiotica. Voor dierenartsen die moeilijke hondenwonden behandelen, en voor artsen die met vergelijkbare infecties bij mensen te maken hebben, kunnen faaggebaseerde sprays of crèmes uiteindelijk een gerichte manier bieden om biofilmgedreven infecties aan te pakken die niet langer op standaardmedicijnen reageren.
Bronvermelding: Dalponte, A., Filor, V., Nerlich, A. et al. Evaluation of bacteriophage efficacy against Pseudomonas aeruginosa in ex vivo and in vitro canine skin systems. Sci Rep 16, 7167 (2026). https://doi.org/10.1038/s41598-026-40091-8
Trefwoorden: bacteriofaagtherapie, Pseudomonas huidinfectie, biofilm, model voor hondenwonden, antibioticaresistentie