Clear Sky Science · nl
Het antitumormechanisme van oclacitinib bij hondenlymfoom
Waarom dit belangrijk is voor honden en hun gezinnen
Lymfoom is een van de meest voorkomende kankers bij gezelschapshonden; chemotherapie helpt veel patiënten, maar werkt niet altijd en kan aanzienlijke bijwerkingen geven. Oclacitinib, een tablet die al veel wordt voorgeschreven aan jeukende honden met allergische huidaandoeningen, heeft recent verrassende voordelen laten zien bij sommige honden met huidlymfoom. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe kan dit alledaagse allergiemedicijn precies tegen kankercellen werken, en kunnen we voorspellen welke honden het meest waarschijnlijk baat hebben?
Van allergiemedicijn naar kankerbestrijder
Oclacitinib is ontwikkeld om overactieve immuunsignalen die atopische dermatitis aandrijven te dempen. Het doet dit door een familie van moleculaire schakelaars genaamd JAKs te blokkeren, met name JAK1, die berichten van ontstekingsmoleculen op het celoppervlak naar de kern doorgeven. Dierenartsen merkten dat sommige honden met een vorm van huidlymfoom verbeterden bij toediening van oclacitinib, maar de redenen waren onduidelijk en de reacties wisselden. De onderzoekers wilden dit gecontroleerd bestuderen, met behulp van in het laboratorium gekweekte lymfoomcellen van honden en monsters van echte patiënten, om te zien wanneer en hoe oclacitinib daadwerkelijk kankercellen kan doden in plaats van alleen de huid te verzachten. 
Het testen van lymfoomcellen in het laboratorium
Het team onderzocht één canine cutane (huid) lymfoomcelijn en acht aanvullende hooggradige lymfoomcelijnen die zowel T-cel- als B-celkankers vertegenwoordigden. Bij blootstelling van deze cellen aan oclacitinib in concentraties vergelijkbaar met die bij behandelde honden, liet ongeveer de helft van de celijnen duidelijke groeivertraging zien en gingen meerdere cellijnen in celdood over. Gevoelige cellen stapelden zich op in een rustfase van de celcyclus en vertoonden kenmerken van geprogrammeerde celdood, waaronder activatie van een uitvoerend eiwit genaamd caspase-3. Andere lymfoomlijnen reageerden daarentegen nauwelijks binnen hetzelfde concentratiebereik, wat benadrukt dat lymfoom bij honden geen enkele ziekte is maar een verzameling biologisch verschillende kankers.
Inzoomen op een kwetsbare signaleringsroute
Om te achterhalen wat gevoelige tumorcellen scheidde van resistente, richtten de wetenschappers zich op de JAK/STAT-signaleringsroute, een veelgebruikte overlevingsweg in veel bloedkankers. Ze ontdekten dat alleen de lymfoomcelijnen die op oclacitinib reageerden, sterke basale activatie van twee sleutelspelers toonden: JAK1 en STAT5. Wanneer deze gevoelige cellen met oclacitinib werden behandeld, daalde de activiteit van STAT5 scherp, terwijl de totale eiwitniveaus gelijk bleven. Een tweede JAK1-remmer uit de humane geneeskunde, filgotinib, gaf een vergelijkbaar patroon van groeiremming en uitschakeling van STAT5. Diepe genactiveringsprofilering liet zien dat oclacitinib sets genen dempte die gekoppeld zijn aan JAK/STAT-signalen en de expressie van c-Myc verminderd — een hoofdregelaar van groei die vaak in kankers wordt gekaapt — wat helpt verklaren waarom cellen in de celcyclus arresteren en afsterven. 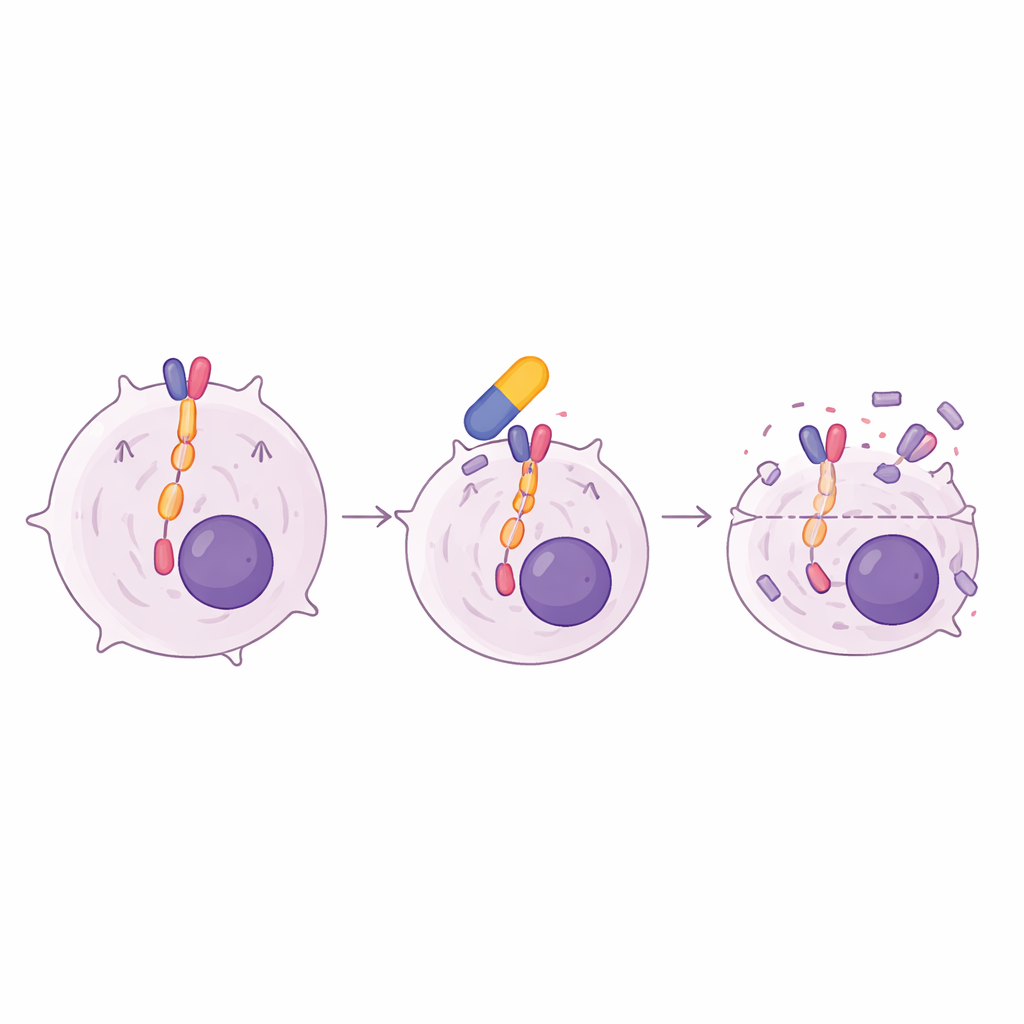
De koppeling tussen laboratoriumbevindingen en echte hondenpatiënten
Vervolgens richtten de onderzoekers zich op biopsiemonsters van honden met cutaan lymfoom die in klinieken met oclacitinib waren behandeld. Met kleuringstechnieken die geactiveerde eiwitten aantonen, vonden ze dat honden waarvan de tumoren geactiveerde JAK1 en STAT5 vertoonden, vaker partiële of volledige responsen op het middel hadden. Sommige niet-responders vertoonden nog steeds deze signalen, wat suggereert dat aanvullende ontsnappingsroutes bepaalde tumoren in stand kunnen houden, maar het algemene patroon wees op een sterke associatie. Belangrijk is dat veel monsters van lymfeklier- en darmlymfomen van andere honden hetzelfde JAK1/STAT5-activeringspatroon lieten zien, wat de mogelijkheid oproept dat de voordelen van oclacitinib zich kunnen uitstrekken voorbij huidlymfoom naar een bredere groep agressieve canine lymfomen.
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar laat het werk zien dat oclacitinib bepaalde canine lymfoomcellen rechtstreeks kan remmen en soms doden door een sleuteloverlevingsroute rond JAK1 en STAT5 uit te schakelen en de activiteit van groeibevorderende genen zoals c-Myc te verlagen. Normale lymfocyten van gezonde honden werden bij klinisch relevante doses veel minder beïnvloed, hoewel hoge concentraties de uitbreiding van geactiveerde immuuncellen wel vertraagden, wat het belang onderstreept van het afwegen van anti-kankereffecten tegen mogelijke immuunsuppressie. De studie suggereert dat het testen van tumoren op geactiveerde JAK1 en STAT5 dierenartsen kan helpen de honden te identificeren die het meest waarschijnlijk voordeel hebben van oclacitinib en soortgelijke middelen. Hoewel meer klinische proeven nodig zijn, kan dit algemeen beschikbare allergiemedicijn onderdeel worden van een doelgerichte behandelingsarsenaal voor hondenlymfoom, gestuurd door eenvoudige moleculaire markers.
Bronvermelding: Harada, M., Inanaga, S., Sakurai, M. et al. The antitumor mechanism of oclacitinib in canine lymphoma. Sci Rep 16, 8427 (2026). https://doi.org/10.1038/s41598-026-40066-9
Trefwoorden: hondenlymfoom, oclacitinib, JAK1 STAT5-route, gerichte kankertherapie, veterinaire oncologie