Clear Sky Science · nl
Tribolium castaneum met langere duur van tonische immobiliteit vertoont meer variaties die overeenkomen met het menselijke Parkinson-genoomgebied
Waarom een klein kevertje belangrijk is voor hersenziekten
De ziekte van Parkinson staat vooral bekend om tremoren en bewegingsproblemen, maar in wezen gaat het om uitval van hersencellen die de boodschapperstof dopamine gebruiken. Deze studie laat zien dat een veelvoorkomende voorraadkastplaag, de rode meelkever, Parkinson-achtige eigenschappen kan ontwikkelen na generaties selectie op een ongewone verdedigingsstrategie: doodspelen. Door dit theatrale gedrag te koppelen aan specifieke genetische veranderingen die lijken op veranderingen nabij menselijke Parkinson-genen, suggereert het werk dat zelfs een klein kevertje ons kan helpen een grote menselijke hersenaandoening beter te begrijpen.
Een kever die de dood voorwendt door stil te blijven staan
Bij aanvallen van roofdieren laten sommige rode meelkevers zich roerloos vallen en “spelen dood” in een toestand die tonische immobiliteit wordt genoemd. De onderzoekers kweekten eerder twee stammen: een die lange tijd roerloos blijft (de L-stam) en een die er snel uit komt (de S-stam). Eerder werk toonde aan dat de langdoende kevers langzamer bewegen, afwijkende looppatronen hebben en lagere dopaminegehalten in hun hersenen dragen. Toediening van dopamine, of zelfs cafeïne, verkort hun doodspelbeurten. In de natuur overleven de langzaam bewegende, lang-doodspelende kevers juist beter tegen bepaalde spinnen en sluipwespen, omdat stil blijven ze moeilijker te pakken maakt. Zo produceert een overlevingsstrategie in het wild kevers die in het laboratorium opvallend veel overeenkomsten vertonen met Parkinsonpatiënten in hun bewegingen.
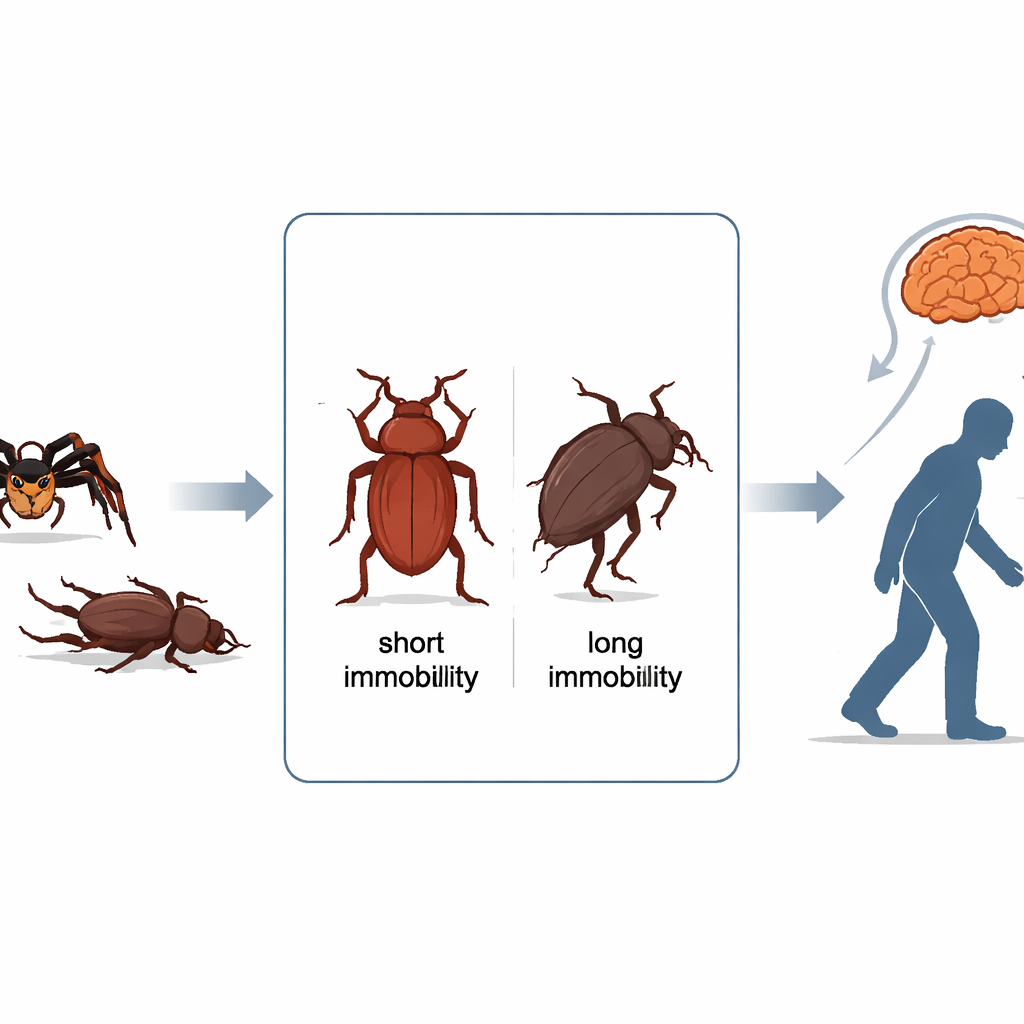
Beetle-DNA scannen op echo’s van Parkinson
Om te onderzoeken of deze Parkinson-achtige eigenschappen samenhingen met genetische veranderingen vergelijkbaar met die bij mensen, vergeleek het team de volledige DNA-sequenties van de lang- en kort-doende stammen. Ze zochten naar kleine veranderingen in de genetische code, grotere inserties en deleties, en variaties in het aantal kopieën van genen. Vervolgens keken ze welke van deze gewijzigde kevergenen sterk overeenkomen met menselijke genen die al in verband zijn gebracht met Parkinson of met het dopaminesysteem. Het antwoord was opvallend: de lang-doende stam droeg veel meer mutaties in keverversies van menselijk Parkinson-gerelateerde genen dan de kort-doende stam. Dit omvatte genen die betrokken zijn bij stressgevoelige ‘chaperonne’-eiwitten en in de energieproducerende machines van mitochondriën, beide centrale verdachten bij menselijke Parkinson.
Van genen naar dopamine en beweging
De studie ging verder dan ruwe DNA-sequenties en onderzocht hoe sterk verschillende genen in het keverlichaam aanstaan. Met eerder RNA-sequencingmateriaal koppelden de auteurs tientallen genen die tussen stammen verschilden aan menselijke routes voor monoamine-signaleringspaden, een familie van hersenchemicaliën waartoe dopamine behoort. Bij lang-doende kevers vertoonden enzymen die het aminozuur tyrosine omzetten in dopamine gewijzigde expressie en subtiele sequentieveranderingen. Dit suggereert dat dopamine in deze dieren anders geproduceerd en verwerkt wordt. Ze vonden ook verschillen in kevergenen die gerelateerd zijn aan insuline- en suikerhuishouding, overeenkomend met menselijke en fruitvlieggenen die aan Parkinson en diabetes zijn gekoppeld — twee aandoeningen die bij mensen al bekend zijn om invloed op elkaar te hebben.
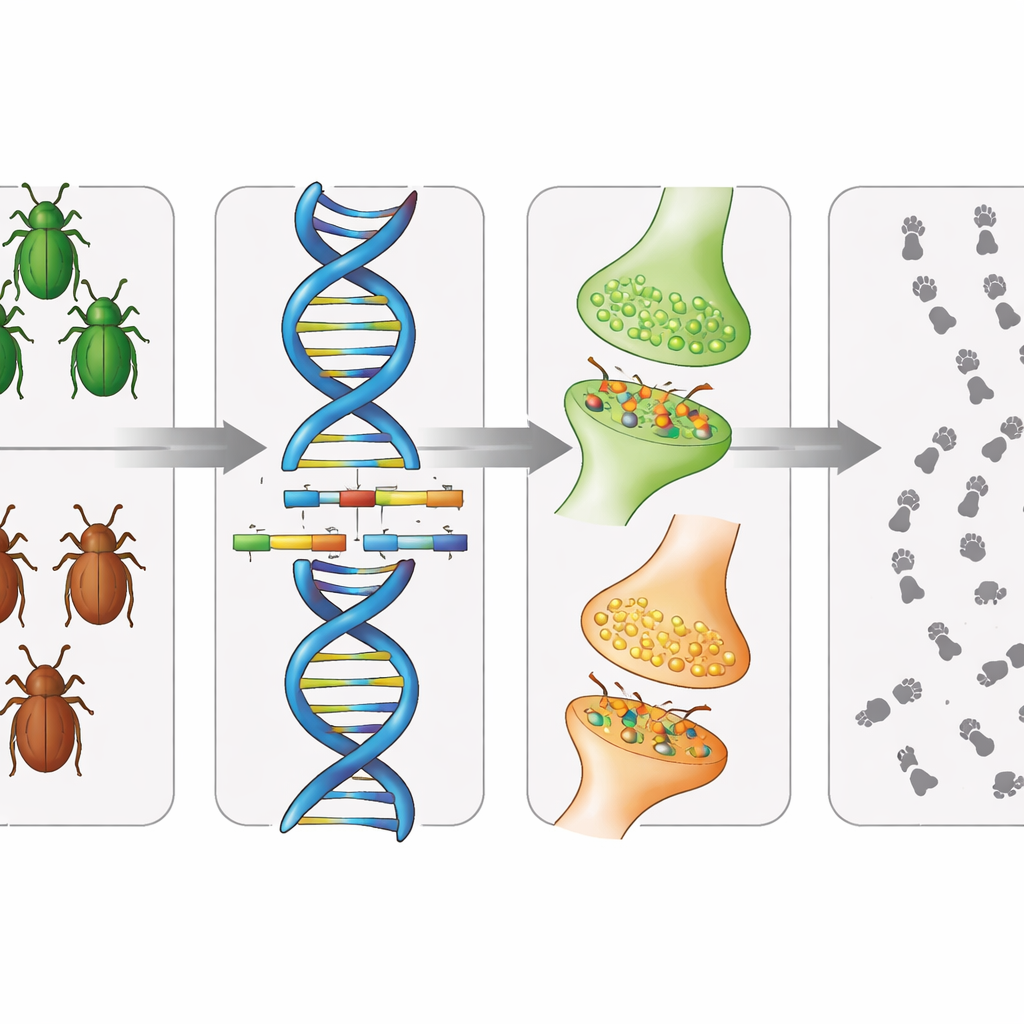
Een web van signalen, geen enkelvoudig “Parkinson-gen”
Belangrijk is dat klassieke menselijke Parkinson-genen zoals LRRK2 en PINK1 geen duidelijke mutaties lieten zien in deze kevers. In plaats daarvan lijkt de lang-doende stam een cluster van veranderingen op te hopen verspreid over vele genen die bijdragen aan dopamine-signaleringsroutes, mitochondriale gezondheid, stressresponsen en insulinepaden. Netwerkanalyses toonden dat deze kevergenen aansluiten bij menselijke routes die worden gelabeld als verschillende Parkinson-subtypen. De auteurs stellen dat dit het menselijke beeld weerspiegelt, waarin Parkinson beter wordt gezien als een syndroom dat voortkomt uit verstoorde netwerken van genen en cellulaire systemen, en niet uit één enkele defecte schakel.
Wat dit betekent voor mensen en voor roofdieren
Voor niet-specialisten is de kernboodschap dat een door evolutie gevormd gedrag om roofdieren te slim af te zijn per ongeluk kenmerken van een menselijke hersenziekte kan nabootsen. Door kevers te selecteren op hoe lang ze “doodspelen”, kregen wetenschappers dieren wiens genen en hersenchimie echo’s vertonen van belangrijke aspecten van Parkinson, waaronder lage dopamine, stijve en afwijkende beweging, en verstoringen in energie- en insulinesignalering. Hoewel deze kevers niet letterlijk “Parkinson hebben,” bieden ze een eenvoudig, genetisch goed te manipuleren model om te onderzoeken hoe veranderingen in veel paden samen bewegen verstoren. Zulke modellen kunnen onderzoekers helpen hypotheses te testen over hoe stress, metabolisme en dopamine in de menselijke hersenen op elkaar inwerken, en uiteindelijk bijdragen aan nieuwe benaderingen om Parkinson-achtige aandoeningen te voorkomen of te behandelen.
Bronvermelding: Tanaka, K., Sasaki, K., Yajima, S. et al. Tribolium castaneum with longer duration of tonic immobility have more variations corresponding to the human Parkinson’s disease genomic region. Sci Rep 16, 8840 (2026). https://doi.org/10.1038/s41598-026-40050-3
Trefwoorden: Ziekte van Parkinson, dopamine, meelkever, tonische immobiliteit, insulinesignalering