Clear Sky Science · nl
MyoFuse is een volledig AI-gebaseerde workflow voor geautomatiseerde kwantificering van fusie van skeletspiercellen in vitro
Waarom het tellen van spiercellen ertoe doet
Wanneer we sporten, herstellen van een verwonding of ziekten zoals diabetes ontwikkelen, remodelen onze skeletspieren zichzelf continu. In het laboratorium bootsen wetenschappers dit proces na door spiercellen in een schaaltje te kweken en te observeren hoe individuele cellen versmelten tot lange, meerkernige vezels. Een eenvoudige maat, de fusie‑index, geeft aan hoe goed die fusie verloopt. Vandaag de dag wordt dat getal meestal verkregen doordat mensen handmatig duizenden kleine celkernen op een scherm tellen—een traag proces dat inconsistent en foutgevoelig kan zijn. Deze studie introduceert MyoFuse, een volledig AI‑gestuurde workflow die deze teltaak automatiseert, met als doel spieronderzoek sneller, betrouwbaarder en minder bevooroordeeld te maken.
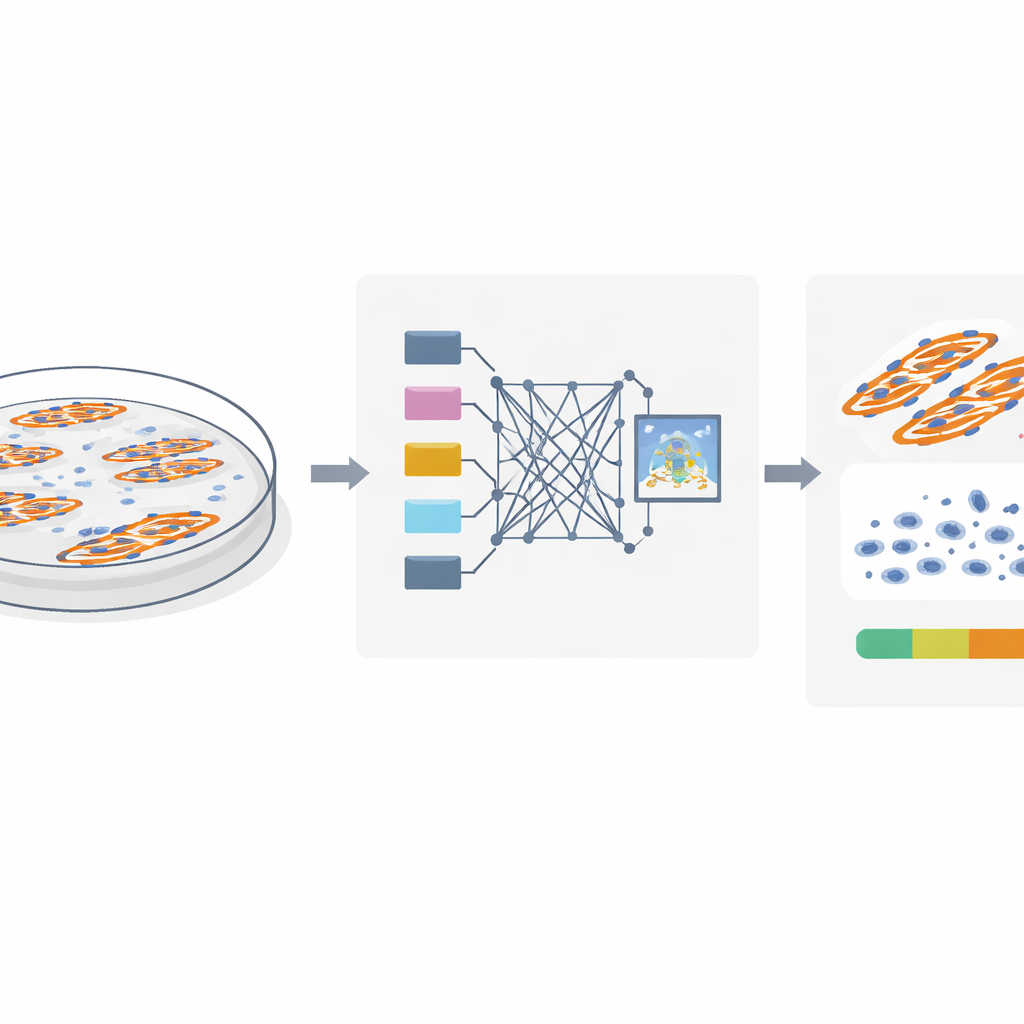
De uitdaging van zien wat er echt is
Om fusie van spiercellen te bestuderen kleuren onderzoekers celnuclei en spiervezels met fluorescente kleurstoffen en maken microscoopbeelden. De cruciale vraag is welke kernen werkelijk binnen gefuseerde spiervezels liggen en welke toebehoren aan niet‑gefuseerde cellen die er vlakbij zitten. Traditionele methoden gaan ervan uit dat als een kern in een vlak, tweedimensionaal beeld overlapt met een spiervezel, die kern zich binnen die vezel bevindt. Cellen groeien echter in drie dimensies: een kern kan makkelijk boven of onder een vezel liggen en toch overlappend lijken in het beeld. De auteurs gebruiken gedetailleerde confocale beelden van zowel muis‑ als menselijke spiercellen om te laten zien dat deze overlappingstactiek misleidend kan zijn, waardoor veel nabijgelegen kernen ten onrechte als deel van gefuseerde vezels worden geteld en de fusie‑index wordt opgeblazen.
Een slimere manier om fluorescente beelden te lezen
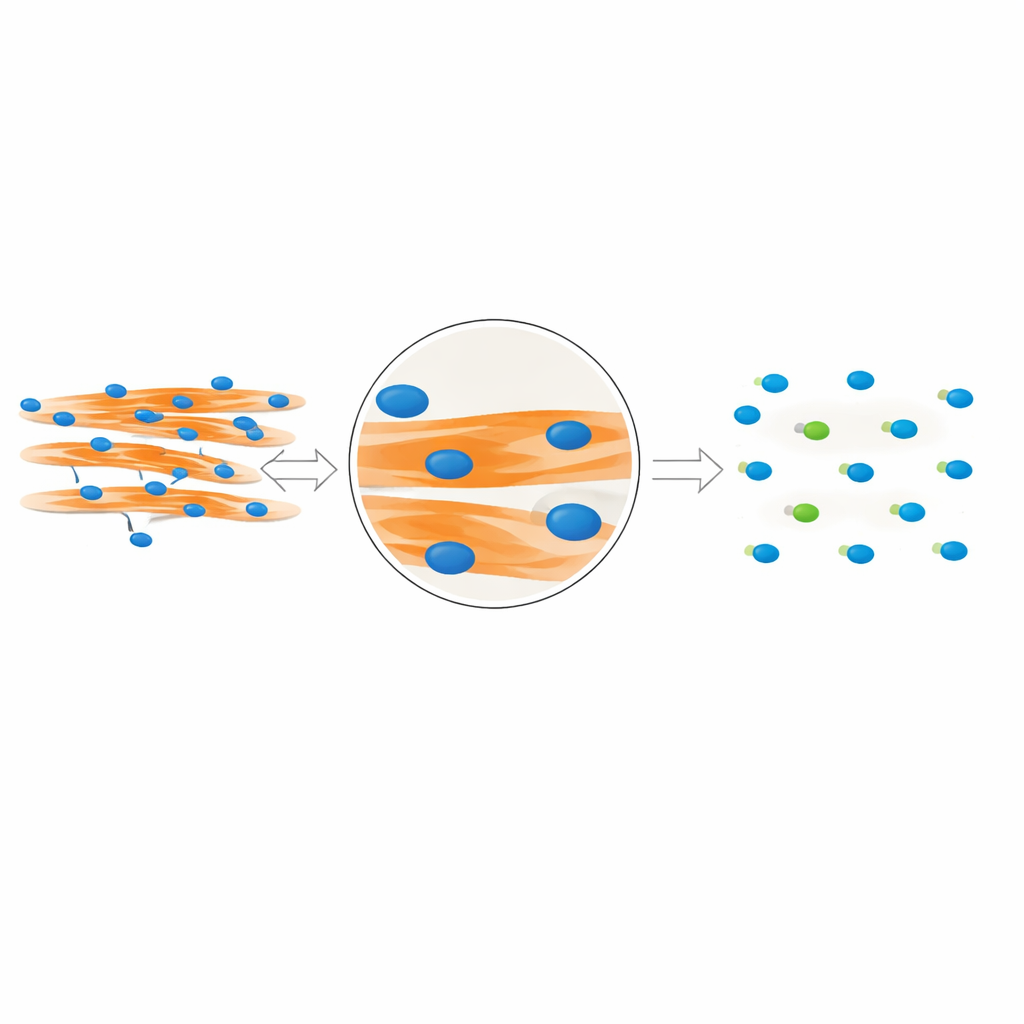
Het team ontdekte dat echte “in‑vezel” kernen een duidelijk visueel spoor achterlaten. Omdat deze kernen fysiek ruimte innemen binnen de vezel, veroorzaken ze kleine donkere onderbrekingen in het fluorescerende signaal dat het spierproteïne MyHC markeert. Kernen die boven of onder een vezel liggen verstoren dit signaal niet. Op basis van dit inzicht ontwierpen de auteurs MyoFuse, een twee‑stappen AI‑workflow. Eerst trekt een gespecialiseerd segmentatiemodel (gebaseerd op het open‑source hulpmiddel Cellpose) nauwkeurig de contouren van individuele kernen, zelfs wanneer die dicht op elkaar in clusters zitten. Vervolgens onderzoekt een lichtgewicht neuraal netwerkclassifier het omringende MyHC‑signaal voor elke kern en bepaalt of deze binnen een spiervezel ligt of erbuiten, uitsluitend op basis van dit lokale patroon in plaats van eenvoudige overlapping.
Hoe goed de AI overeenkomt met menselijke experts
De onderzoekers testten MyoFuse grondig op beelden van muizen C2C12 spiercellen en primaire menselijke spiercellen uit verschillende spieren. Voor beide soorten kwamen het totale aantal kernen en de berekende fusie‑index van de AI buitengewoon goed overeen met zorgvuldige handmatige annotaties door experts, met bijna perfecte correlaties. Op het niveau van individuele kernen onderscheidde de classifier kernen binnen versus buiten vezels in meer dan 90% van de gevallen over de datasets heen, met prestatiecijfers die het menselijk niveau benaderen. Belangrijk is dat MyoFuse ook goed presteerde op een aparte set menselijke cellen die nooit voor training was gebruikt, wat suggereert dat de aanpak kan generaliseren naar nieuwe monsters in plaats van alleen de trainingsbeelden te memoriseren.
Verborgen vooringenomenheid in gangbare methoden aan het licht brengen
Naast de nauwkeurigheid legde MyoFuse systematische problemen bloot in veelgebruikte maskergebaseerde methoden die vertrouwen op eenvoudige overlap tussen kern‑ en vezelsignalen. Toen de auteurs fusie‑indices van MyoFuse vergeleken met die van een verfijnde maskermethode toegepast op dezelfde beelden, overschatte de maskermethode consequent de fusie, vooral in gebieden waar spiervezels een groter deel van de kweekplaat bedekten. Het aanpassen van detectiedrempels veranderde de cijfers maar verwijderde deze onderliggende bias niet; ogenschijnlijke verbeteringen kwamen vaak voort uit fouten die elkaar opheffen in plaats van betere biologische detectie. Het team toonde ook aan dat fusieschattingen sterk kunnen variëren tussen verschillende regio’s van een enkel kuipje, wat benadrukt dat het analyseren van slechts een paar handgekozen velden een vertekend beeld kan geven van hoe goed cellen samenvoegen.
Wat dit betekent voor toekomstig spieronderzoek
MyoFuse biedt spierbiologen een manier om cel‑fusie te meten die zowel sneller is als trouw blijft aan wat er daadwerkelijk in het schaaltje gebeurt. Door geautomatiseerde microscopie te combineren met een AI die honderden duizenden kernen in enkele minuten kan segmenteren en classificeren, vermindert de workflow de werklast voor mensen, minimaliseert subjectieve keuzes over waar te kijken en hoe beelden te drempelen, en voorkomt het dat nabijgelegen cellen als gefuseerde spiercellen worden geteld. De auteurs erkennen dat extreme beeldomstandigheden of sterk afwijkende kleuringsprotocollen hertraining kunnen vereisen, maar de methode is openlijk beschikbaar en ontworpen om aanpasbaar te zijn. Voor laboratoria die spierontwikkeling, veroudering, regeneratie of metabole ziekten bestuderen, belooft MyoFuse robuustere fusiemetingen—en daarmee betrouwbaardere conclusies over hoe spieren groeien en veranderen.
Bronvermelding: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Trefwoorden: skeletspier, cel‑fusie, kunstmatige intelligentie, beeldanalyse, myogenese