Clear Sky Science · nl
RBP4 remt de progressie van plaveiselcelcarcinoom van de tong door het PI3K/AKT-signaleringspad te remmen en de M1-polarisatie van macrofagen te bevorderen
Waarom tongkanker nieuwe ideeën nodig heeft
Tongkanker kan mensen hun vermogen om te spreken, te eten en te proeven ontnemen, en zelfs met chirurgie, chemotherapie en bestraling zijn de langetermijnuitkomsten vaak teleurstellend. Deze studie onderzoekt een onverwachte helper in ons bloed, een vitamine A-transporteiwit genaamd RBP4, en toont aan hoe het zowel de groei van tongtumoren kan vertragen als de eigen immuunverdediging van het lichaam kan mobiliseren. Door te onthullen hoe dit molecuul werkt in kankercellen en in de omliggende immuuncellen wijst het onderzoek op nieuwe strategieën die mogelijk ooit behandelingen effectiever en minder schadelijk kunnen maken.
Een verborgen eiwit in tongtumoren
De onderzoekers begonnen met het doorzoeken van grote kanker-genendatabanken om te zien welke immuun-gerelateerde genen mogelijk kunnen voorspellen hoe patiënten met plaveiselcelcarcinoom van de tong op de lange termijn zullen functioneren. Onder honderden kandidaten bleek RBP4, een eiwit dat vooral bekend is als transporteur van vitamine A in het bloed, bijzonder interessant. Toen het team tumorstalen vergeleek met nabijgelegen gezond tongweefsel, vonden ze dat de RBP4-niveaus consequent veel lager waren in de kanker. Dit patroon werd bevestigd in meerdere onafhankelijke datasets en in weefselmonsters van 20 patiënten, wat suggereert dat verlies van RBP4 een veelvoorkomend kenmerk van deze ziekte is.
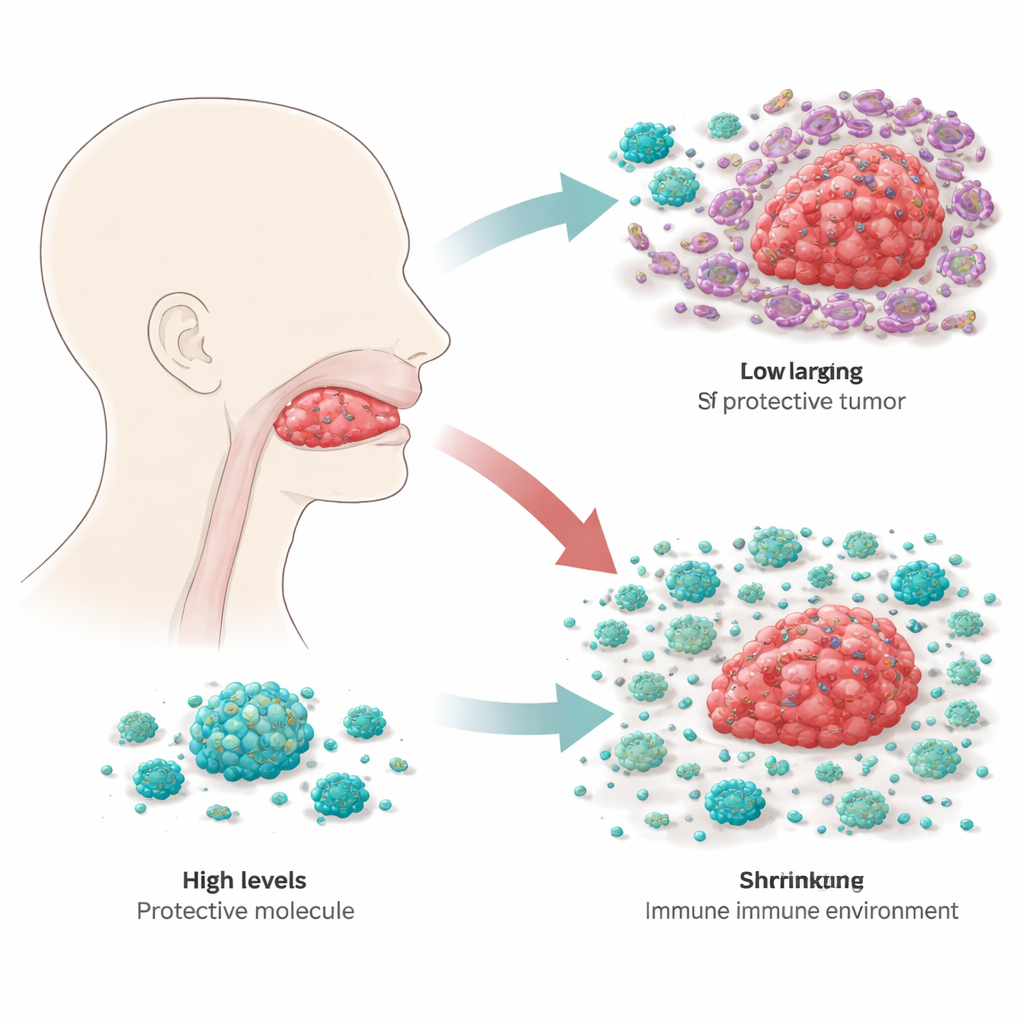
De tumorgroei van binnenuit vertragen
Om uit te zoeken wat RBP4 daadwerkelijk doet in tongkankercellen, maakten de wetenschappers tumorcellijnen die ofwel extra RBP4 produceerden of juist veel minder ervan maakten. In kweek groeiden cellen met hogere RBP4 langzamer, terwijl cellen met verlaagd RBP4 sneller vermenigvuldigden en beter waren in bewegen en binnendringen door kunstmatige membranen—gedragingen die gekoppeld zijn aan uitzaaiing en terugkeer van de ziekte. Wanneer deze gemodificeerde cellen bij muizen werden geïmplanteerd, bleven tumoren met extra RBP4 kleiner, terwijl tumoren met verlaagd RBP4 agressiever groeiden. Door sleutelregelaars van groei in de cellen te volgen, liet het team zien dat RBP4 een belangrijk groeipad, bekend als PI3K–AKT–mTOR, dempt—een intern gaspedaal waarop veel kankers vertrouwen. Met hoge RBP4 is dit pad stiller en kunnen tumorcellen minder goed die flexibele, mobiele toestand aannemen die hen helpt te migreren.
Immuuncellen veranderen in tumorbestrijders
Kanker groeit niet geïsoleerd; het leeft binnen een buurt van immuuncellen, bloedvaten en steuncellen die samen de tumormicro-omgeving vormen. Hier spelen macrofagen—grote immuuncellen die tumoren kunnen aanvallen of juist ondersteunen—een centrale rol. De onderzoekers merkten dat tumoren met meer RBP4 ook de neiging hadden meer van het “M1”-type macrofaag te bevatten, dat geassocieerd wordt met ontsteking en tumorvernietiging, in plaats van het “M2”-type dat vaak tumorgroei ondersteunt. In kweek, wanneer macrofagen werden blootgesteld aan gezuiverd RBP4 of aan tongkankercellen die meer RBP4 afscheidden, schakelden ze over naar deze M1, tumorbestrijdende toestand. Wanneer RBP4 in de kankercellen werd gereduceerd, neigden de macrofagen in plaats daarvan naar het meer tumorvriendelijke profiel.
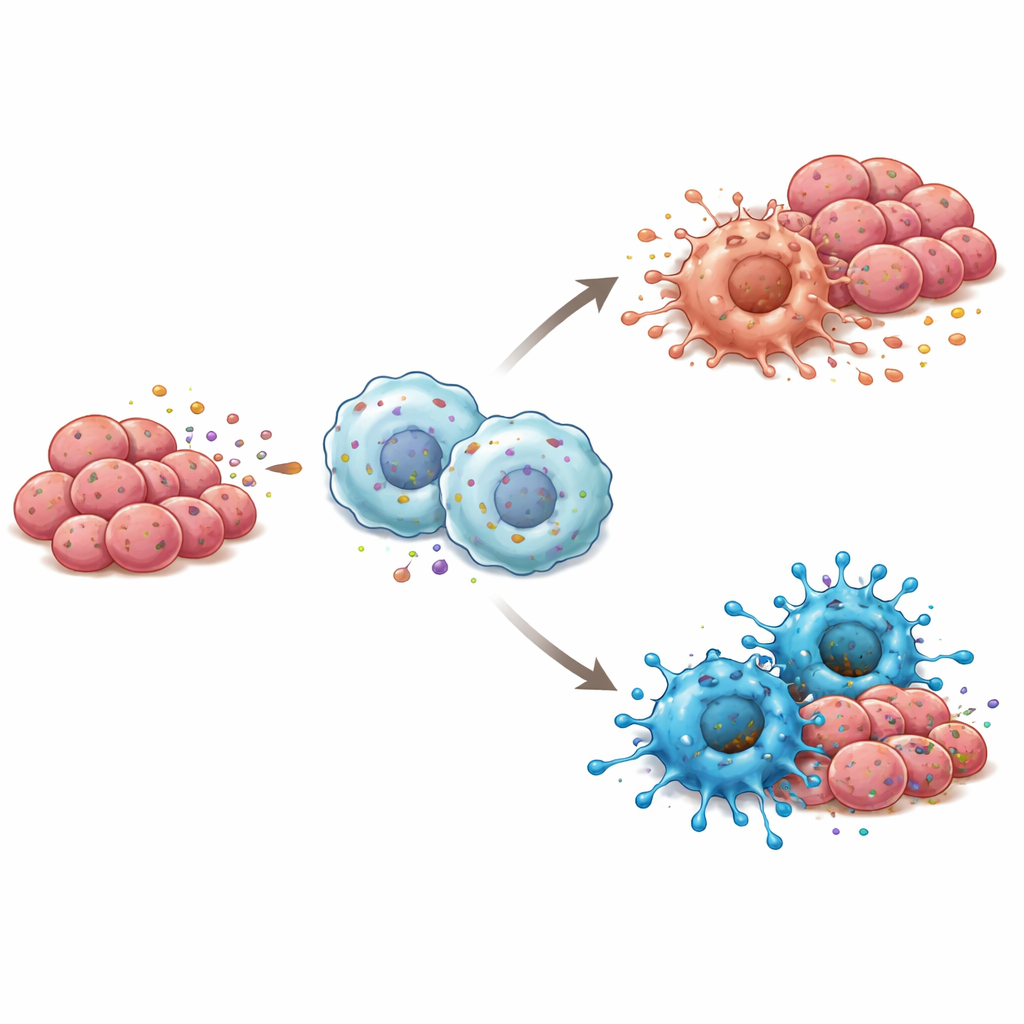
Signaalroutes achter de immuumswitch
Om te begrijpen hoe RBP4 macrofagen aanzet tot een vijandiger houding tegenover tumoren onderzochten de onderzoekers welke interne alarmsystemen in deze immuuncellen werden geactiveerd. Ze vonden dat RBP4 een sensor genaamd TLR4 op het oppervlak van de macrofaag stimuleerde en daarmee NF-κB activeerde, een hoofdregelaar die ontstekingsreacties aanstuurt. Het blokkeren van TLR4 met een chemische remmer schakelde deze ketenreactie uit en voorkwam dat macrofagen de M1-toestand aannamen, zelfs in aanwezigheid van RBP4. In muizen groeiden tumoren die waren gevormd uit tongkankercellen rijk aan RBP4 en gemengd met macrofagen langzamer en bevatten ze meer M1-type cellen, samen met sterkere TLR4- en NF-κB-activiteit, wat het idee versterkt dat dit pad cruciaal is voor de immuuneffecten van RBP4.
Wat dit zou kunnen betekenen voor toekomstige zorg
Al met al portretteert het werk RBP4 als een dubbelwerkende rem op tongkanker: binnen tumorcellen knijpt het een overactief groeicircuit af, en in de omgeving van de tumor helpt het macrofagen te veranderen in waakzamere verdedigers. Hoewel veel vragen nog onbeantwoord zijn—zoals precies hoe RBP4 met zijn doelen interageert en hoe het het beste veilig kan worden verhoogd—suggereert de studie dat het herstellen of nabootsen van RBP4’s werking zowel de tumoruitbreiding kan vertragen als de eigen immuundruk op de kanker kan versterken. Voor patiënten opent dat het vooruitzicht op toekomstige therapieën die niet alleen tumoren verwijderen, maar ook hun interne bedrading en lokale “ecosysteem” herstructureren om terugkeer te voorkomen.
Bronvermelding: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Trefwoorden: tongkanker, RBP4, tumormicro-omgeving, macrofagen, PI3K AKT-pad