Clear Sky Science · nl
Een intelligent gezondheidszorgkader voor de diagnose van hepatocellulair carcinoom gebaseerd op samengestelde learners uit biomedische gegevens met behulp van uitlegbare kunstmatige intelligentie
Waarom slimmer controleren op leverkanker ertoe doet
Leverkanker, met name een veelvoorkomend type dat hepatocellulair carcinoom heet, groeit vaak geruisloos totdat behandeling lastig wordt. Artsen verzamelen al een schat aan routinematige testresultaten van patiënten, maar al die cijfers omzetten in een vroegtijdig waarschuwingssignaal is moeilijk. Deze studie onderzoekt hoe geavanceerde computerprogramma’s door alledaagse medische gegevens kunnen zoeken om te ontdekken welke patiënten een hoog risico lopen, en daarbij ook hun redenering op een manier kunnen uitleggen die artsen vertrouwen.
Routineonderzoeken omzetten in vroegtijdige waarschuwingen
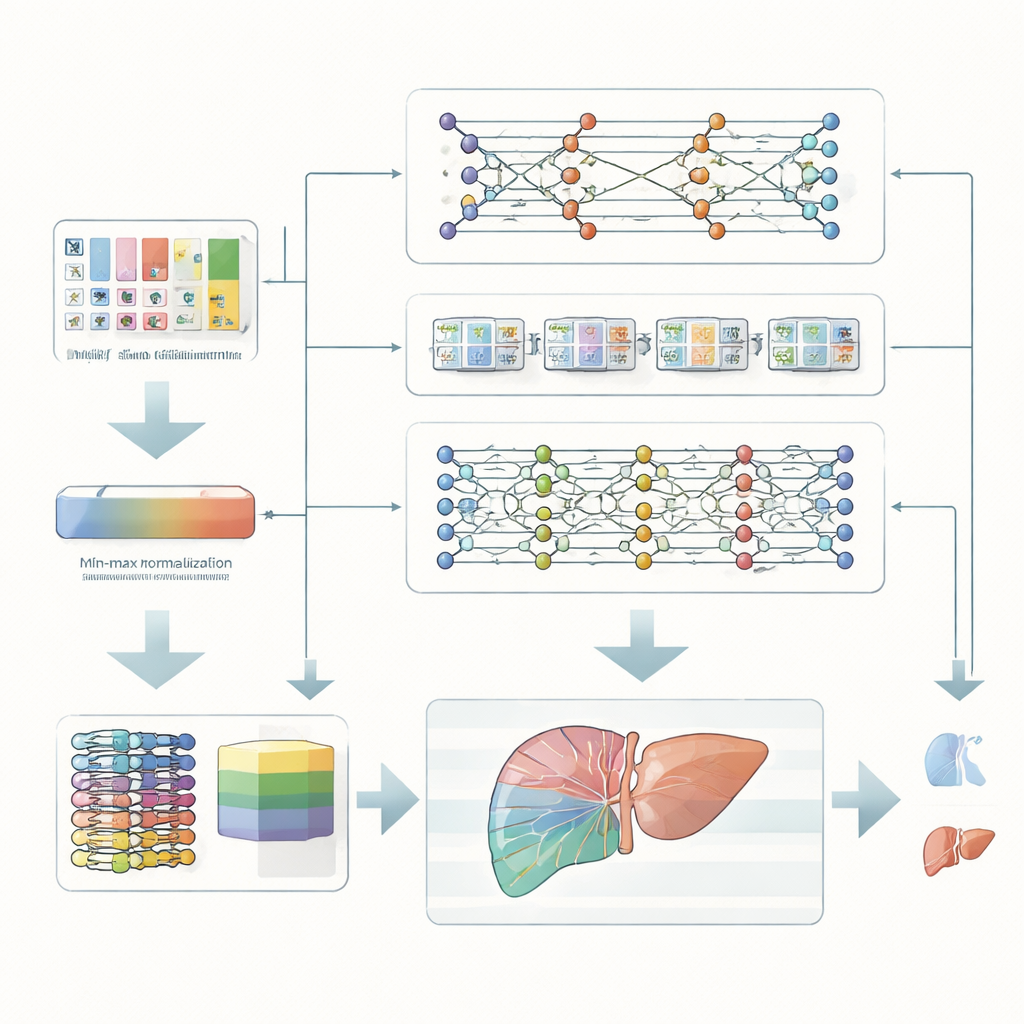
De onderzoekers richten zich op patiënten met chronische leverproblemen, die een hoger risico lopen ernstige leverkanker te ontwikkelen. In plaats van te vertrouwen op dure scans of complexe genetische tests, gebruiken ze standaard klinische metingen — zoals bloedchemie, leverenzymen en basisgezondheidsinformatie. Deze metingen worden eerst zorgvuldig herschaald zodat alle kenmerken in hetzelfde numerieke bereik vallen. Deze eenvoudige maar belangrijke opschoningsstap helpt computermodellen patronen betrouwbaarder te leren en voorkomt dat een enkele ongewoon grote waarde de voorspellingen domineert.
Veel digitale “tweede meningen” werken samen
In plaats van te leunen op één algoritme bouwen de onderzoekers een ensemble, of team, van drie verschillende deep learning‑modellen. Het ene model comprimeert de gegevens om de meest informatieve combinaties van kenmerken te ontdekken. Een tweede model is ontworpen om patronen te herkennen die zich als reeksen ontvouwen, en legt vast hoe meerdere metingen samen op risico kunnen wijzen. Een derde model stapelt meerdere eenvoudige lagen om complexe, niet‑lineaire relaties in de data vast te leggen. Elk model geeft zijn eigen oordeel of een patiënt tot een hoge‑risico- of lage‑risicogroep behoort, en een hoger niveau‑combiner weegt en verenigt deze meningen tot één uiteindelijke beslissing.
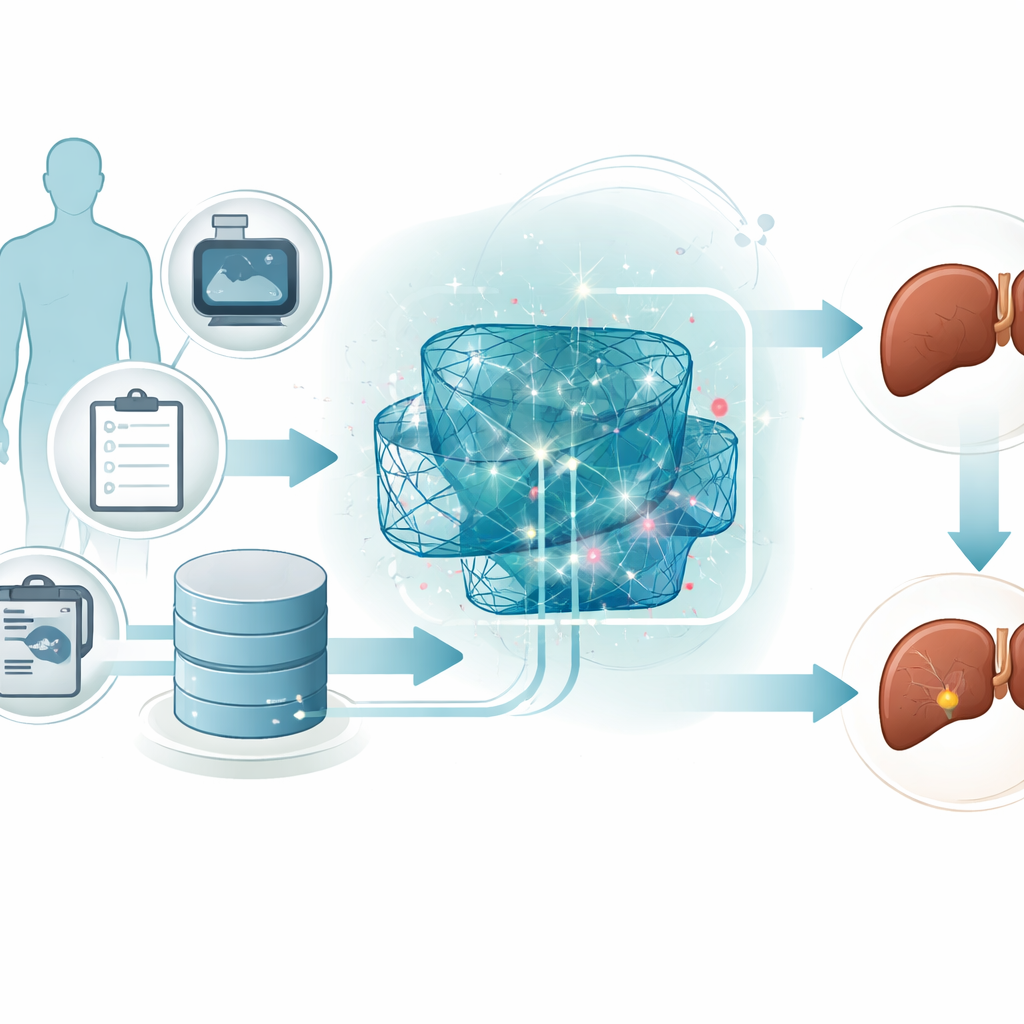
De zwarte doos openen voor artsen
Hoe krachtig ze ook zijn, deep learning‑systemen worden vaak bekritiseerd omdat ze als mysterieuze “zwarte dozen” functioneren. Om dit aan te pakken voegen de auteurs een uitlegbare artificiële intelligentielaag toe op basis van een methode bekend als SHAP. Deze techniek schat in hoeveel elke invoerkenmerk een individuele voorspelling duwt richting een veiliger of risicovoller resultaat. Bijvoorbeeld: bepaalde leverenzymniveaus, markers van leverfunctie en tekenen van uitzaaiing buiten de lever blijken bijzonder invloedrijk. Artsen kunnen niet alleen zien dat het systeem een patiënt als hoog risico markeert, maar ook welke specifieke metingen die beslissing hebben gedreven en in welke richting, wat een transparantere samenwerking tussen clinicus en machine oplevert.
Hoe goed werkt de aanpak?
Het team test zijn kader op een openbare dataset van 165 patiënten die ten minste een jaar werden gevolgd, elk gelabeld als overlevend of niet‑overlevend. Ondanks de bescheiden omvang van de dataset leert het gecombineerde model hoge‑risico van lage‑risico patiënten met opvallende nauwkeurigheid te scheiden: het classificeert in de laatste trainingsfasen ongeveer 98 van de 100 gevallen correct. In vergelijking met een reeks bestaande methoden — inclusief klassieke statistische modellen en enkele moderne neurale netwerken — evenaart of overtreft dit benadering niet alleen hun nauwkeurigheid, precisie en balans tussen gemiste en foutieve alarmen, maar doet dit ook met relatief korte rekentijd. Een ablatiedome onderzoek, waarbij de drie componentmodellen afzonderlijk worden getest, toont aan dat elk van hen waarde toevoegt, maar dat hun combinatie het beste presteert.
Wat dit kan betekenen voor patiëntenzorg
Voor de dagelijkse medische praktijk wijst dit werk op beslissingshulpmiddelen die zowel scherp als begrijpelijk zijn. Een systeem gebouwd volgens deze principes zou kunnen helpen leverpatiënten te signaleren die geruisloos in een gevarenzone dreigen te raken, lang voordat symptomen zich openbaren, met gebruik van gegevens die al in veel klinieken worden verzameld. Tegelijkertijd kunnen de verklaringen — die aangeven welke testresultaten en klinische tekenen voor een bepaald persoon het belangrijkst zijn — artsen ondersteunen bij het verfijnen van behandelplannen en het bespreken van risico’s met patiënten. Hoewel de studie nog steunt op een relatief kleine, enkelbronige dataset en beelden en genetische data weglaat, biedt zij een routekaart voor slimmere, meer transparante kankerrisicomodellen die, met grotere en diversere gegevens, op een dag routinepartners in de strijd tegen leverkanker zouden kunnen worden.
Bronvermelding: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
Trefwoorden: leverkanker, medische AI, vroege diagnose, uitlegbare AI, klinische besluitvorming