Clear Sky Science · nl
Multi-omics identificatie van sleuteltargets voor de osteogene differentiatie van humane beenmerg mesenchymale stromale cellen onder oxidatieve stress
Waarom gestresste botten ertoe doen
Naarmate we ouder worden of chronische ziekten ontwikkelen zoals diabetes en osteoporose, verliezen onze botten hun vermogen om zichzelf te herstellen. Een grote boosdoener is “oxidatieve stress” — een ophoping van reactieve moleculen die cellen beschadigen. Deze studie stelt een praktische vraag met grote gevolgen voor breuken en botimplantaten: wat gaat er precies mis in humane beenmergstamcellen wanneer ze aan oxidatieve stress worden blootgesteld, en kunnen we een moleculaire schakel vinden die hen helpt om toch nieuw bot te blijven vormen?
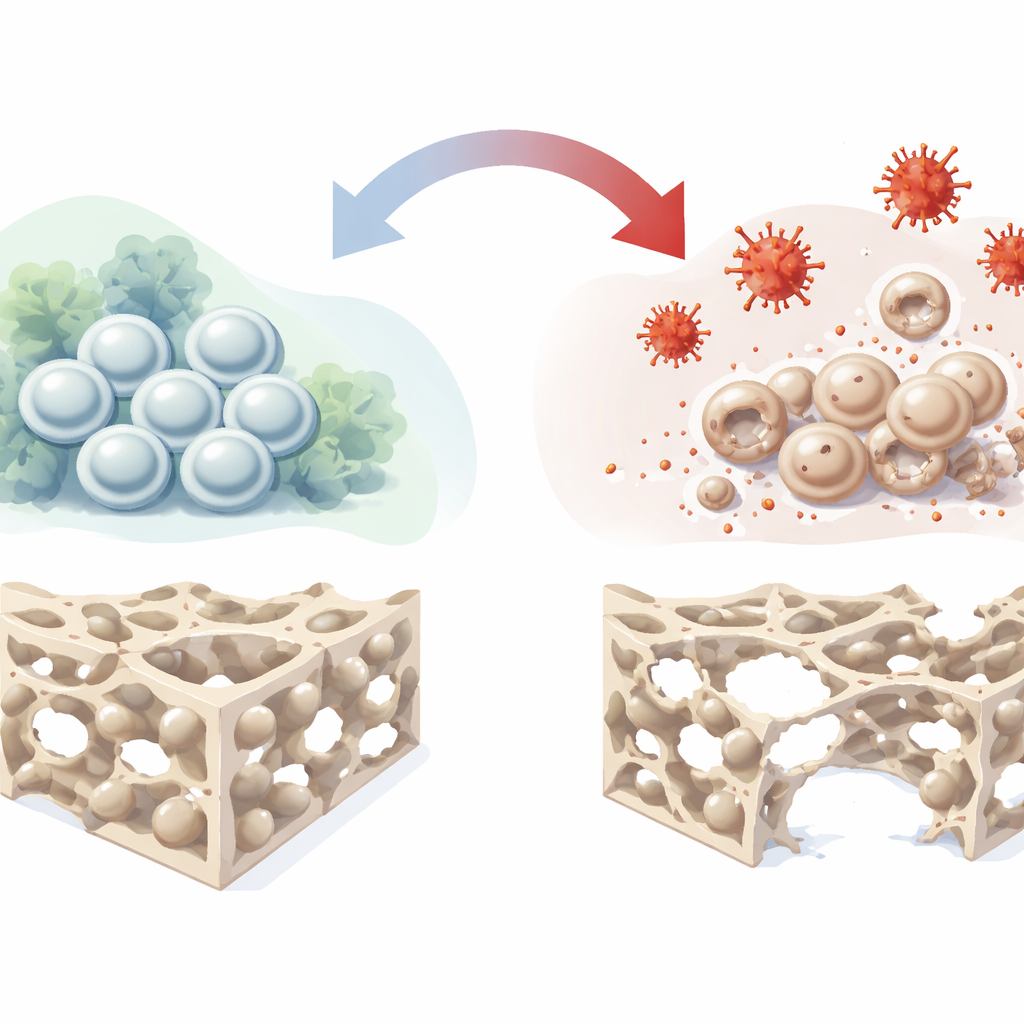
Stamcellen die bot opbouwen
Diep in ons bot bevinden zich beenmerg mesenchymale stromale cellen, een veelzijdige populatie die zichzelf kan vernieuwen en kan uitrijpen tot botvormende cellen, kraakbeencellen en vetcellen. Omdat ze van nature beschadigd weefsel helpen herstellen, zijn ze een vooraanstaande kandidaat voor volgende generatie behandelingen om botdefecten en osteonecrose te repareren. In echte patiënten bevinden deze cellen zich echter vaak in vijandige omgevingen met slechte doorbloeding, lage zuurstof, ontsteking en oxidatieve stress. In zulke omstandigheden verzwakt hun vermogen om in botcellen te veranderen, wat het succes van op stamcellen gebaseerde therapieën beperkt. De auteurs wilden deze vijandige omgeving in het laboratorium nabootsen en gedetailleerd in kaart brengen hoe dit botvorming verstoort.
Een harde omgeving nabootsen in het laboratorium
De onderzoekers gebruikten waterstofperoxide, een veelvoorkomende bron van reactieve zuurstofspecies, om oxidatieve stress op humane beenmergstamcellen in kweek toe te passen. Ze titreren de dosis zorgvuldig om een balans te vinden waarbij de cellen gestrest maar niet gedood werden. Bij of onder 400 micromolair behielden de cellen hun normale spilvorm en bleven ze levensvatbaar, hoewel hun interne biochemie duidelijk veranderde: de niveaus van reactieve zuurstof stegen, de mitochondriale functie begon te wijzigen en de balans tussen overleving- en sterftegerelateerde eiwitten kantelde richting stressadaptatie. Bij hogere doses verloren de cellen hun vorm en stierven ze in grote aantallen. Met de goed verdragen dosis van 400 micromolair zette het team vervolgens de cellen aan tot botvorming en observeerde wat er gebeurde.
Hoe stress botopbouw blokkeert
Onder oxidatieve stress nam het vermogen van de stamcellen om botcellen te worden af, zoals bleek uit meerdere aanvullende testen. Vroege botvormende activiteit, gevolgd met een enzym genaamd alkalische fosfatase, nam af naarmate de stress toenam. Later, toen de cellen minerale afzettingen zouden moeten vormen, lieten de kweekschalen minder en zwakkere calciumnoduli zien. Belangrijke botgerelateerde genen en eiwitten, zoals RUNX2 en osteopontine, werden eveneens naar beneden bijgesteld. Om dieper te kijken combineerden de wetenschappers twee krachtige “omics”-benaderingen: RNA-sequencing om te profileerden welke genen actiever of minder actief waren, en grootschalige proteïne-analyse om te zien welke eiwitten daadwerkelijk in hoeveelheid veranderden. Gezamenlijk onthulden deze datasets honderden verschuivingen in celcycluscontrole, chromatinegedrag, metabolisme en de organisatie van het extracellulaire geraamte, waarmee een beeld ontstond van stamcellen waarvan de interne timing en structurele ondersteuning verstoord zijn door oxidatieve stress.
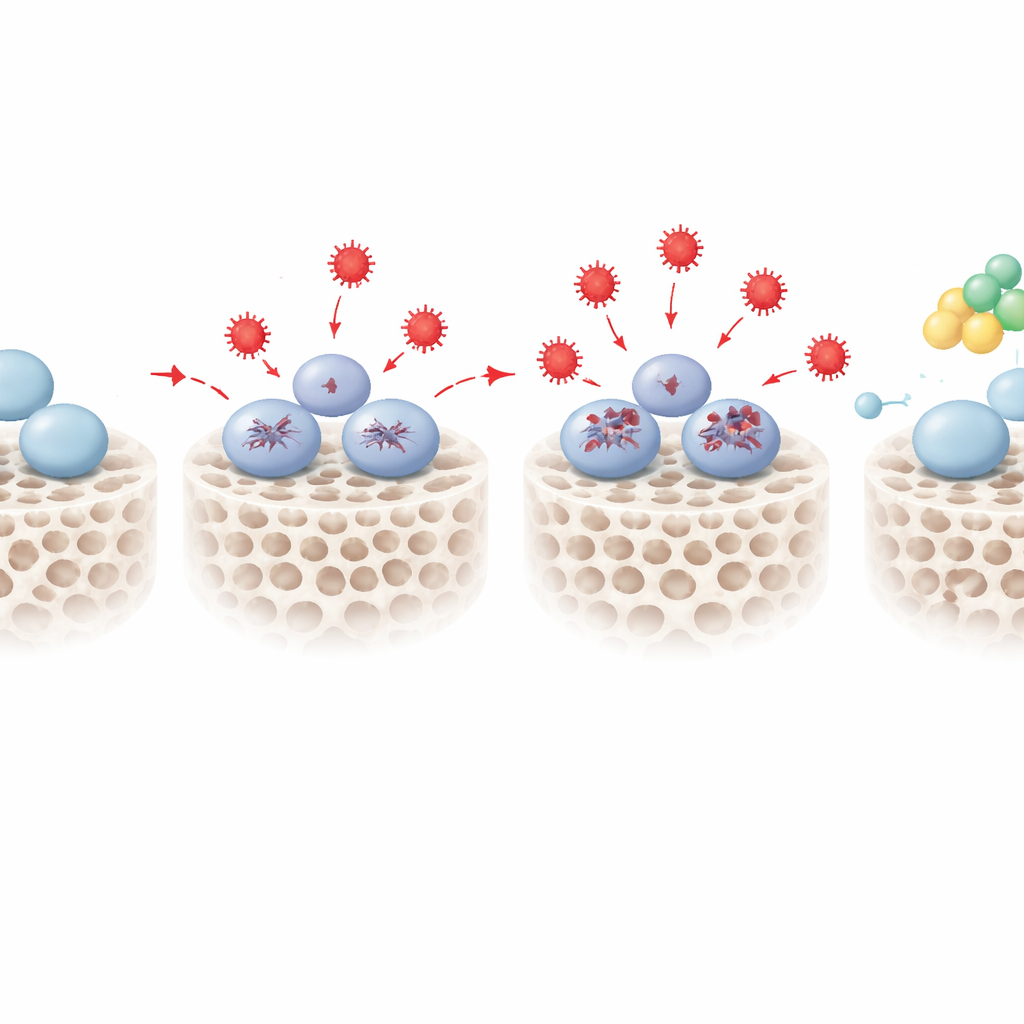
Een beschermende schakel genaamd PENK vinden
Door de RNA- en eiwitkaarten te overlappen, spitste het team het veld toe tot 18 moleculen die consequent veranderden in gestresste cellen en gekoppeld waren aan zowel stressreacties als botvorming. Eén viel op: proenkephalin, of PENK, vooral bekend als voorloper van natuurlijke opioïde peptiden. Onder oxidatieve stress stegen de PENK-niveaus op een dosisafhankelijke manier. Wanneer de wetenschappers PENK kunstmatig naar beneden brachten met genetische middelen, werden gestresste stamcellen nog minder in staat bot te vormen, met zwakkere vroege enzymactiviteit en minder minerale afzetting. Wanneer ze PENK versterkten, gebeurde het tegenovergestelde: zelfs onder dezelfde oxidatieve omstandigheden herwonnen de cellen een groot deel van hun vermogen om gemineraliseerde botmatrix te bouwen. Aanvullende padanalyses suggereerden dat PENK mogelijk werkt door bepaalde metabole routes bij te sturen, waaronder sphingolipidemetabolisme, die de redoxbalans verbinden met de beslissing of een stamcel zijn potentieel behoudt of richting een botbestemming gaat.
Wat dit betekent voor toekomstige botreparatie
Deze studie toont aan dat oxidatieve stress op zichzelf voldoende is om het botvormende vermogen van humane beenmergstamcellen te ondermijnen, en identificeert PENK als een ingebouwd beschermend factor dat hen helpt deze schade te weerstaan. Voor niet-specialisten is de boodschap duidelijk: het succes van op stamcellen gebaseerde bottherapieën hangt niet alleen af van de cellen zelf, maar ook van de gestresste omgevingen waarin ze worden geplaatst en de moleculaire schakelaars die hen helpen ermee om te gaan. Door PENK te benadrukken als een veelbelovend doelwit, wijst het werk de weg naar toekomstige geneesmiddelen of gengebaseerde benaderingen die botreparatie kunnen versterken bij patiënten wier weefsels zijn doordrenkt met oxidatieve stress, van oudere individuen tot mensen met chronische metabole of inflammatoire aandoeningen.
Bronvermelding: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Trefwoorden: botregeneratie, oxidatieve stress, mesenchymale stamcellen, osteogene differentiatie, PENK