Clear Sky Science · nl
Impact van oxidatie van G-quadruplex-RNA op zijn conformationele dynamiek en interactie met ALS-geassocieerde TDP-43
Waarom dit van belang is voor zenuwgezondheid
Amyotrofische laterale sclerose (ALS) is een dodelijke ziekte waarbij de zenuwcellen die beweging aansturen langzaam afsterven, maar de onderliggende oorzaken van deze selectieve beschadiging blijven onduidelijk. Deze studie stelt een eenvoudige maar belangrijke vraag: wanneer we ouder worden en onze cellen meer „roestachtige" chemische schade ondervinden, verstoort die slijtage van RNA—de werkende kopie van onze genen—dan vitale signalen die motorische neuronen in leven houden? Door in te zoomen op een bijzondere gevouwen RNA-vorm en een sleuteleiwit dat aan ALS gelinkt is, TDP-43, onthult het werk hoe kleine chemische littekens mogelijk het toneel voor ziekte kunnen voorbereiden. 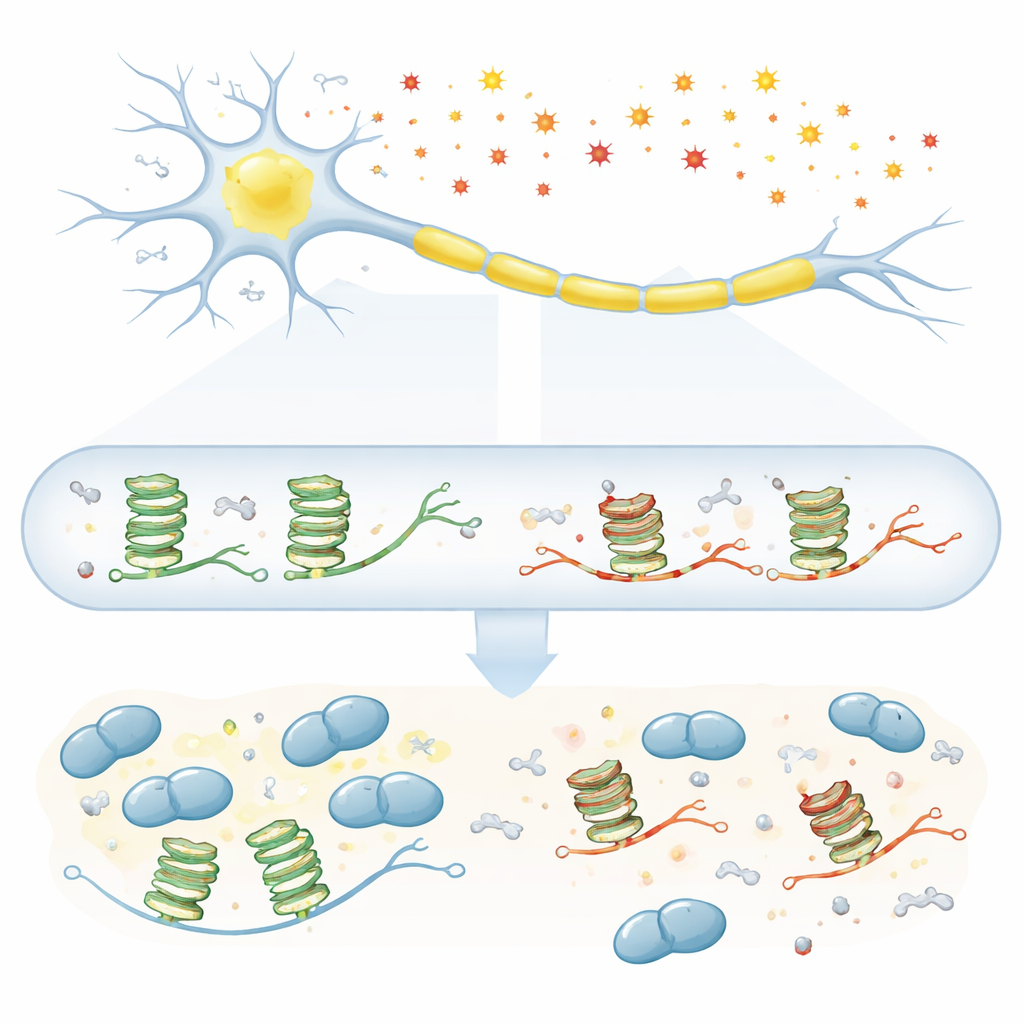
Een kwetsbare RNA-knoop in het hart van motorische neuronen
Motorische neuronen zijn afhankelijk van het lange-afstandsvervoer van RNA-boodschappen langs hun axonen zodat eiwitten ter plaatse kunnen worden gemaakt, dicht bij de verbindingen met spier. Veel van deze boodschappen dragen een speciale structurele „knoop" die G-quadruplex heet, opgebouwd uit reeksen van de base guanine. Eiwitten zoals TDP-43 herkennen deze knoop en haken het RNA vast aan transportgranules die langs het axon bewegen. Het probleem is dat guanine ook de makkelijkst te oxideren base is wanneer cellen onder stress staan door reactieve zuurstofsoorten, die met ouder worden accumuleren. Eerdere aanwijzingen suggereerden dat G-quadruplexen en TDP-43 centraal staan in ALS, maar het was onduidelijk hoe oxidatie van deze RNA-knopen precies hun samenwerking kan verstoren.
Observeren hoe oxidatieve stress RNA-vormen vervormt
De onderzoeker stelde eerst menselijke neuroblastoomcellen bloot aan waterstofperoxide, een veelvoorkomend oxidatief middel, en onderzocht vervolgens de staat van G-quadruplexstructuren. Signalen van een G-quadruplex-gevoelige probe namen af naarmate de oxidatieve stress toenam, wat aangeeft dat deze compacte RNA-knopen hun normale vorm verloren. Om de chemie vast te pinnen bouwde het team vervolgens synthetische RNA’s die G-quadruplexen vormen en voegden doelbewust verschillende hoeveelheden 8-oxoguanine toe, een bekende geoxideerde variant van guanine die wordt aangetroffen in verouderende neuronen en ALS-weefsel. Met een reeks biofysische technieken lieten ze zien dat zelfs bescheiden niveaus van deze modificatie de ordelijke stapeling van het G-quadruplex losser maken, hoewel de precieze uitkomst afhangt van de omliggende RNA-sequentie. 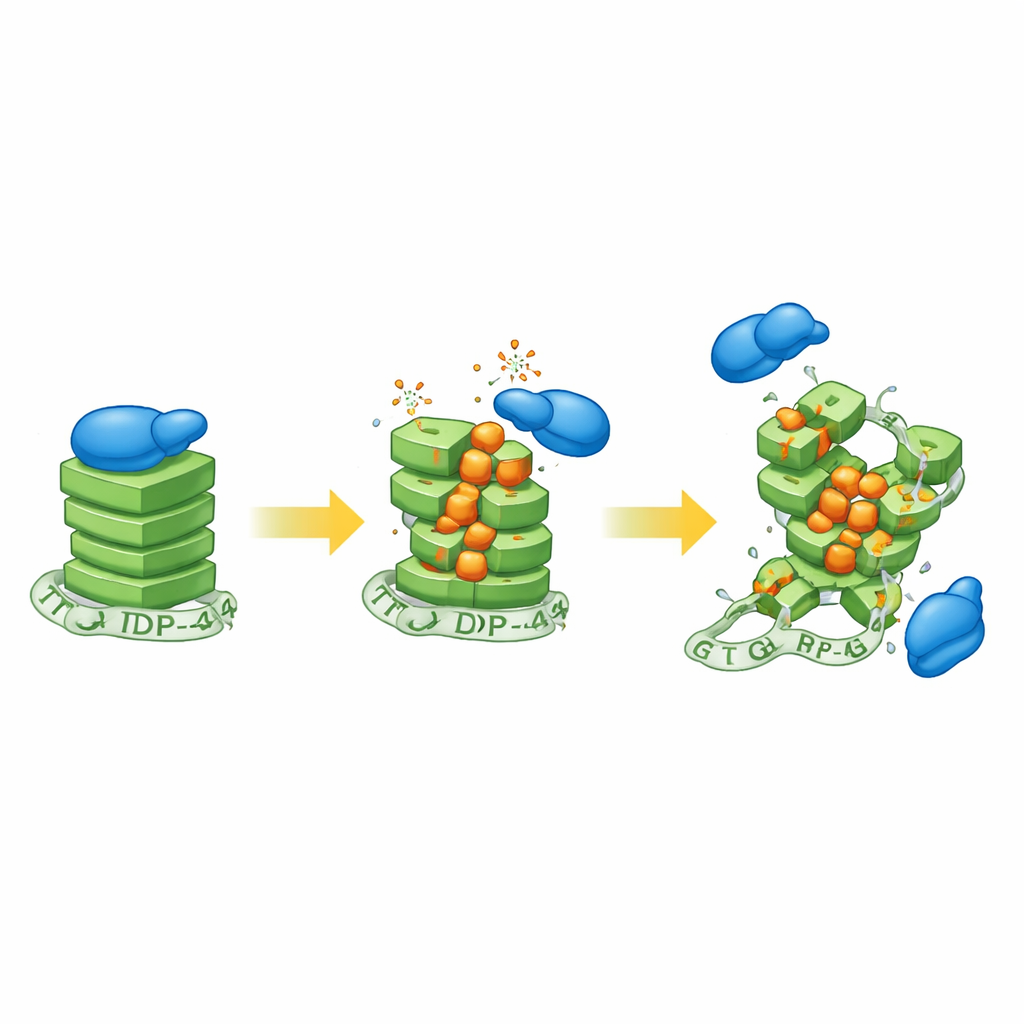
Nieuwe fouten: mismatches en fout-gekoppelde strengen
Nadere analyse bracht twee verschillende soorten structurele problemen aan het licht. In één G-quadruplex afgeleid van het PSD-95-bericht neigden geoxideerde guanines ertoe onjuist te pairen met nabijgelegen adenines, waardoor "mismatches" ontstonden die de vouwing subtiel vervormden. Deze mismatches traden het meest op bij matige oxidatieniveaus, wanneer het RNA zich nog tijdelijk kon assembleren tot een G-quadruplex dat de verkeerde partners in contact bracht. In een andere G-quadruplex afkomstig van het CaMKIIα-bericht destabiliseerde zware oxidatie de gebruikelijke intramoleculaire knoop zo sterk dat de overgebleven intacte guanines naar partners op andere RNA-strengen zochten, wat abnormale intermoleculaire G-quadruplexen bevorderde. Dergelijke verkeerd gekoppelde structuren kunnen verschillende RNA’s door elkaar raken en het normale RNA-verkeer binnen neuronen verstoren.
Wanneer beschadigd RNA zijn eiwitpartner verliest
Vervolgens onderzocht de studie hoe deze vervormde knopen interageren met TDP-43. Met behulp van gelgebaseerde bindingsassays toonde de onderzoeker aan dat TDP-43 een sterke voorkeur heeft voor intacte, parallelle G-quadruplexen en steeds minder goed bindt naarmate er meer geoxideerde basen worden geïntroduceerd. De CaMKIIα-structuur, al dicht op elkaar gepakt, bleek bijzonder gevoelig: zelfs lage oxidatie hing TDP-43-binding bijna volledig af. Een tweede eiwit, FUS—ook gekoppeld aan ALS—toonde een vergelijkbaar maar iets minder ernstig verlies van affiniteit, wat suggereert dat oxidatie de greep van G-quadruplex-bindende eiwitten in het algemeen verzwakt. Intrigerend genoeg wees het bewijs erop dat wanneer TDP-43 met licht geoxideerd RNA werd gemengd, het eiwit een onstabiele tussenvorm van het G-quadruplex leek te binden in plaats van een volledig gevouwen knoop, wat wijst op een dynamische strijd tussen stabilisatie en afbraak.
Extra kwetsbaarheid in ALS-gebonden mutant-eiwitten
Het werk onderzocht verder tien TDP-43-varianten die bij ALS-patiënten worden gevonden, waarvan de meeste veranderingen dragen in een flexibele, glycine-rijke staart die de RNA-herkenning fijn afstemt. Al deze mutanten binden normale G-quadruplexen zwakker dan het wilde-type eiwit. Wanneer geoxideerde G-quadruplex-RNA’s als concurrenten werden geïntroduceerd, waren de mutanten nog minder in staat dan het normale eiwit om de beschadigde structuren te herkennen en te binden. Sommige varianten die zich in bijzonder wanordelijke regio’s bevinden, waren het meeste aangetast. Dit suggereert een dubbele klap bij oudere individuen die dergelijke mutaties dragen: niet alleen is hun TDP-43 van zichzelf minder effectief, maar leeftijdsgerelateerde RNA-oxidatie erodeert verder het vermogen om cruciale boodschappen langs axonen van motorische neuronen te begeleiden.
Wat dit betekent voor het begrip van ALS
Kort gezegd laat deze studie zien dat door leeftijd aangedreven chemische schade fragiele RNA-knopen hervormt die het boodschappertransport in motorische neuronen sturen, en dat deze vervormde knopen niet meer goed samenwerken met TDP-43 of verwante eiwitten. Het gevolg is een vergrote kans op verkeerd geleverde of stilgevallen RNA-ladingen, precies in de lange, kwetsbare axonen die spieren onder controle houden. Voor mensen die ook TDP-43-mutaties erven, kan deze door oxidatie geïnduceerde verzwakking van RNA–eiwitinteracties reeds gestreste neuronen dichter bij uitval duwen. Door deze subtiele maar krachtige keten van gebeurtenissen te belichten—van oxidatieve stress naar veranderd RNA-architectuur naar verstoord transport—benadrukt het werk oxidatie van G-quadruplex-RNA als een veelbelovende moleculaire schakel tussen veroudering en ALS, en als een potentieel doelwit voor toekomstige beschermende therapieën.
Bronvermelding: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Trefwoorden: amyotrofische laterale sclerose, RNA-oxidatie, G-quadruplex, TDP-43, degeneratie van motorische neuronen