Clear Sky Science · nl
Identificatie van biomarkers gerelateerd aan beschadiging van de bloed-hersenbarrière bij cerebraal infarct met transcriptomische analyse
Waarom dit belangrijk is voor beroerte en hersengezondheid
Wanneer iemand een beroerte krijgt door een verstopt bloedvat in de hersenen, kunnen artsen de schade op scans zien maar hebben ze nog steeds moeite te voorspellen wie verergerde zwelling, bloedingen of blijvende beperkingen zal ontwikkelen. Een groot deel van die schade doet zich voor bij de beschermende poortwachter van de hersenen, de bloed‑hersenbarrière, die normaal voorkomt dat schadelijke stoffen uit het bloed in het kwetsbare zenuwweefsel lekken. Deze studie stelde een eenvoudige maar belangrijke vraag: bestaan er moleculaire signalen die aangeven wanneer deze barrière bezwijkt, en zouden die signalen ooit de diagnose en behandeling van beroertepatiënten kunnen verbeteren?
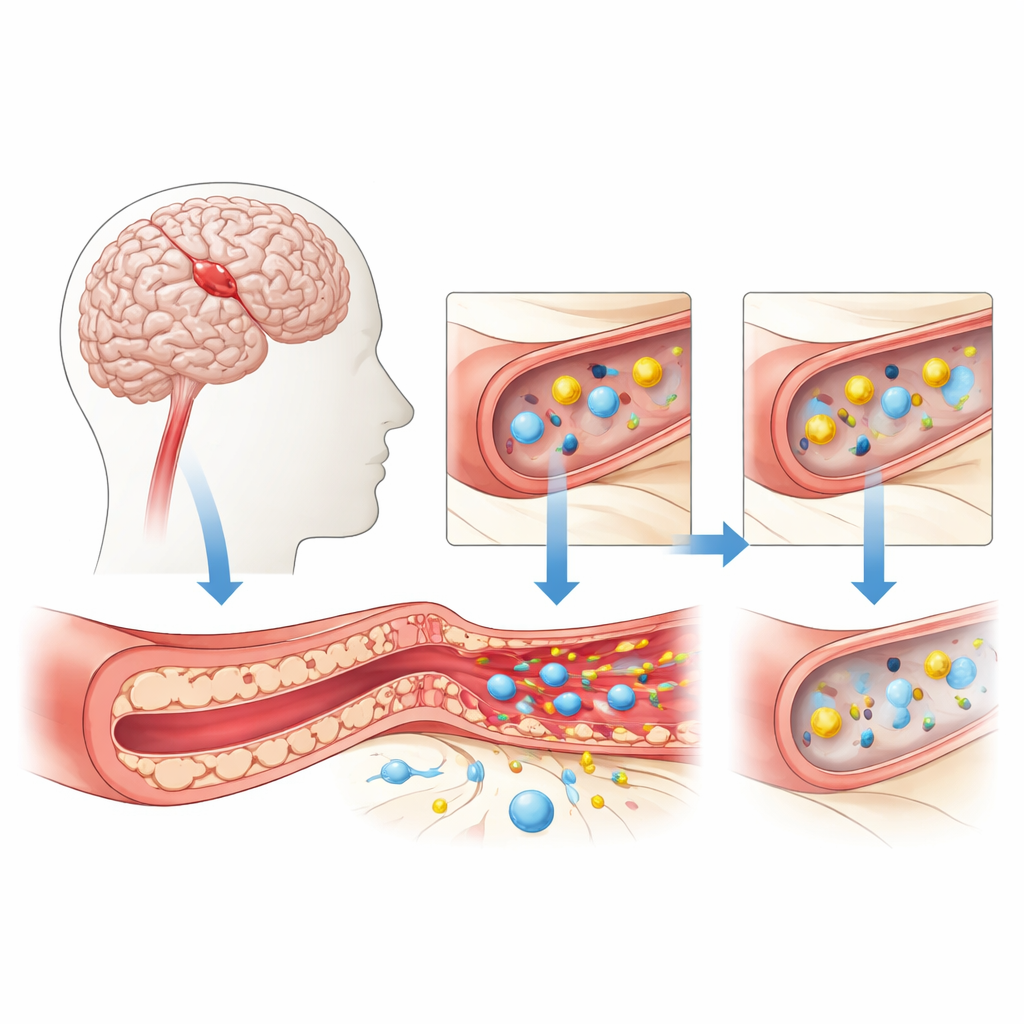
De beschermende poort van de hersenen onder stress
De bloed‑hersenbarrière wordt gevormd door dicht opeengepakte cellen die de wanden van kleine hersenbloedvaten bekleden. Deze cellen regelen zorgvuldig wat van bloed naar hersenen kan passeren: ze laten levensbelangrijke voedingsstoffen zoals zuurstof en glucose binnen en blokkeren toxines en immuuncellen die schade kunnen veroorzaken. Tijdens een cerebraal infarct, of ischemische beroerte, valt de bloedtoevoer plotseling weg. Zonder voldoende zuurstof en suiker raken deze vaatwandcellen onder stress en verliezen ze hun nauwe aansluiting. Er ontstaan openingen tussen hen, vocht sijpelt het omliggende weefsel in en ontstekingssignalen overspoelen het gebied, wat hersenzwelling en verdere schade kan verergeren.
Schade van een beroerte in het laboratorium nabootsen
Om te onderzoeken wat er in deze barrièrecellen gebeurt, gebruikten de onderzoekers een bekende menselijke cellijn die het bekledingstype van hersenvaten nabootst. Ze stelden deze cellen bloot aan een omgeving met weinig zuurstof en geen glucose — oxygen‑glucose deprivation — om de omstandigheden van een beroerte te imiteren, en herstelden daarna de normale omstandigheden om behandeling en herstel na te bootsen. Ze maten hoe goed de cellen overleefden, hoeveel van een celschade‑enzym lekte en hoeveel ontstekingsmoleculen ze afgaven. Zoals verwacht verminderde de stressvolle behandeling de cellulaire gezondheid, verhoogde ontstekingssignalen zoals IL‑1β, IL‑6 en TNF‑α, en vergrootte het lekken van een schade‑marker, LDH. Toen zuurstof en voedingsstoffen werden hersteld, verminderden veel van deze schadelijke veranderingen en herwonnen de cellen deels hun vermogen om in een groeitest nieuwe buisachtige structuren te vormen.
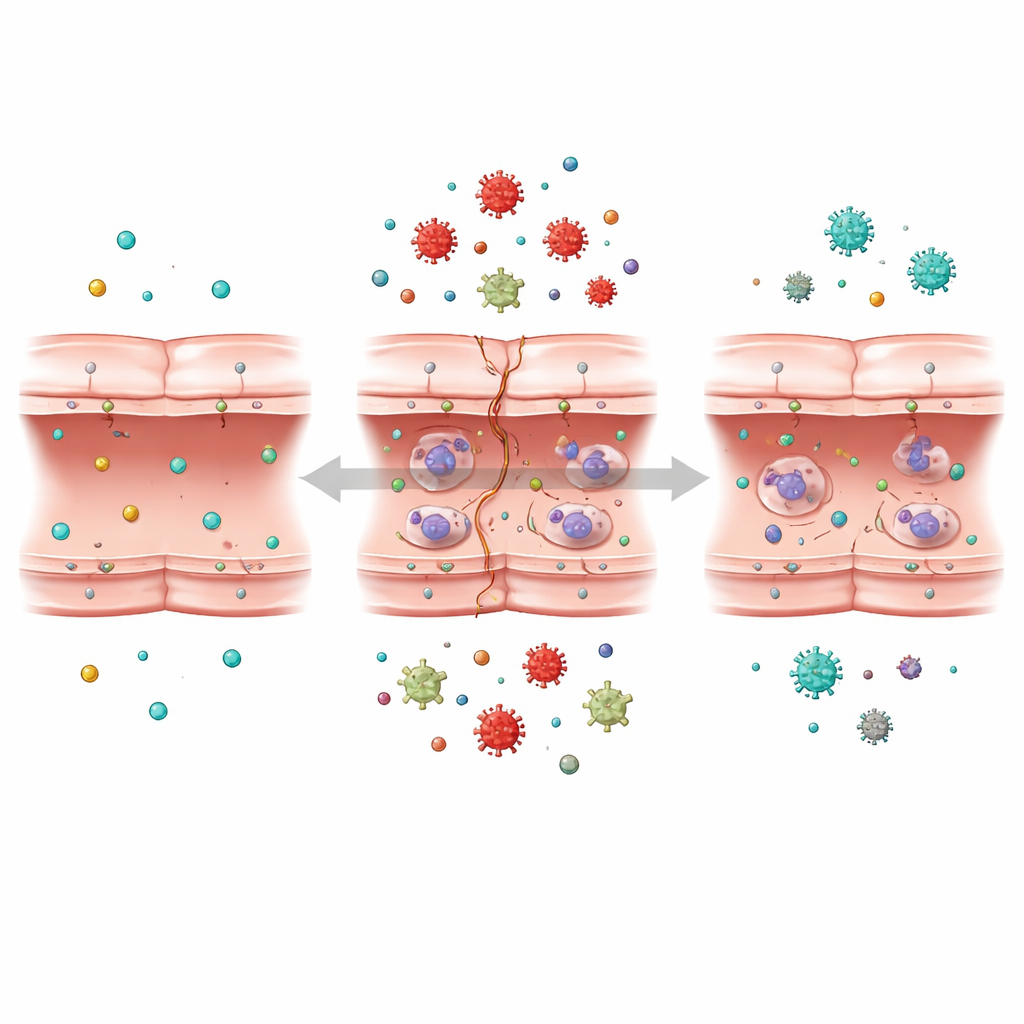
Luisteren naar het moleculaire gesprek van de cel
Het team wendde zich vervolgens tot een krachtige techniek, transcriptomica, die de activiteitsniveaus van duizenden genen tegelijk uitleest. Door normale cellen, oxygen‑glucose‑deprived cellen en cellen die mochten herstellen te vergelijken, identificeerden ze meer dan duizend genen waarvan de activiteit veranderde als reactie op stress vergelijkbaar met een beroerte. Met geavanceerde data‑tools en machine learning groepeerden ze genen die samen reageerden en zochten ze naar diegenen die het sterkst met barrière‑schade waren verbonden. Ze vonden dat veel van de meest aangetaste genen gekoppeld waren aan drie belangrijke structuren binnenin de cel: het ribosoom, dat eiwitten bouwt; het endoplasmatisch reticulum, dat helpt bij het vouwing en verwerken van eiwitten; en de mitochondriën, de kleine energiecentrales die energie leveren.
Ribosomen komen naar voren als aanwijzende signalen
Uit deze grote genenset gebruikten de onderzoekers een random forest‑algoritme — een type beslisboomgebaseerde machine learning — om een korte lijst van bijzonder informatieve genen te selecteren. Ze brachten vervolgens in kaart hoe de overeenkomstige eiwitten met elkaar interageren. Deze analyse belichtte zes kerngenen, de meeste gerelateerd aan het ribosoom, de eiwitfabriek van de cel. Onder de beroerte‑achtige omstandigheden waren deze ribosoomgerelateerde genen sterker geactiveerd, terwijl hun activiteit weer naar normaal terugkeerde toen zuurstof en glucose werden hersteld. Dit patroon suggereert dat veranderingen in de eiwitproductiemachinerie van de cel een gevoelig vroeg signaal kunnen vormen voor beschadiging en herstel van de bloed‑hersenbarrière.
Wat dit kan betekenen voor toekomstige zorg
Voor niet‑specialisten is de belangrijkste boodschap dat deze studie wijst op een nieuwe klasse moleculaire “waarschuwingslampjes” die aan gaan wanneer de beschermende barrière van de hersenen tijdens een beroerte geschaad raakt. In plaats van zich enkel te richten op bekende daders zoals enzymen die de vaatwand afbreken, laat het werk zien dat de eiwitfabrieken van de cel sterk reageren op letsel en weer tot rust komen als de omstandigheden verbeteren. Als vervolgonderzoek aantoont dat deze ribosoomgerelateerde markers in patiëntmonsters zoals bloed detecteerbaar zijn, zouden artsen ze op termijn kunnen gebruiken om de ernst van barrière‑beschadiging te beoordelen, de timing van behandelingen die ontsteking en zwelling verminderen te bepalen en nieuwe medicijnen te testen die deze cruciale poortwachter van hersengezondheid beschermen.
Bronvermelding: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Trefwoorden: ischemische beroerte, bloed-hersenbarrière, biomarkers, ribosomale genen, endotheelcellen