Clear Sky Science · nl
Bacteriële kolonisatie van tumoren stuurt immuunactivatie en de effectiviteit van checkpointremming
Waarom piepkleine bewoners in tumoren ertoe doen
De behandeling van kanker is veranderd door immunotherapieën die de eigen immuuncellen van het lichaam tegen tumoren loslaten. Toch hebben veel patiënten nog steeds weinig profijt, en voorspellende factoren voor respons zijn schaars. Deze studie onderzoekt een onverwachte speler die de balans kan doen doorslaan: bacteriën die in de tumoren zelf leven. Aan de hand van muismodellen van kanker laten de onderzoekers zien dat deze microscopische bewoners kunnen bepalen hoe het immuunsysteem zich in en rond een tumor gedraagt, en daarmee mede bepalen of een veelgebruikte immunotherapie, anti–PD-1, goed werkt of faalt.
Verborgen bacteriën in tumoren
Jarenlang lag de nadruk vooral op de triljoenen microben in de darmen en hun rol in de algemene immuniteit. Recente ontdekkingen tonen aan dat veel menselijke tumoren ook kleine maar actieve bacteriegemeenschappen herbergen. Het team achter deze studie stelde twee fundamentele vragen: bevatten veelgebruikte muistumormodellen ook bacteriën, en zo ja, beïnvloeden die bacteriën daadwerkelijk hoe tumoren groeien en reageren op behandeling? Ze vergeleken twee modellen: MCA-205, een type sarcoom, en MOC1, een model voor hoofd- en halskanker. Met DNA-tests, sequencing en kweekmethoden vonden ze dat MCA-205-tumoren consequent levende bacteriën bevatten, terwijl MOC1-tumoren dat niet deden, zelfs niet wanneer ze in de bacterierijke mond werden geplaatst. In MCA-205 steeg het aantal bacteriën vaak naarmate de tumoren groter werden, wat suggereert dat de groeiende tumor een gunstige omgeving voor microben bood.
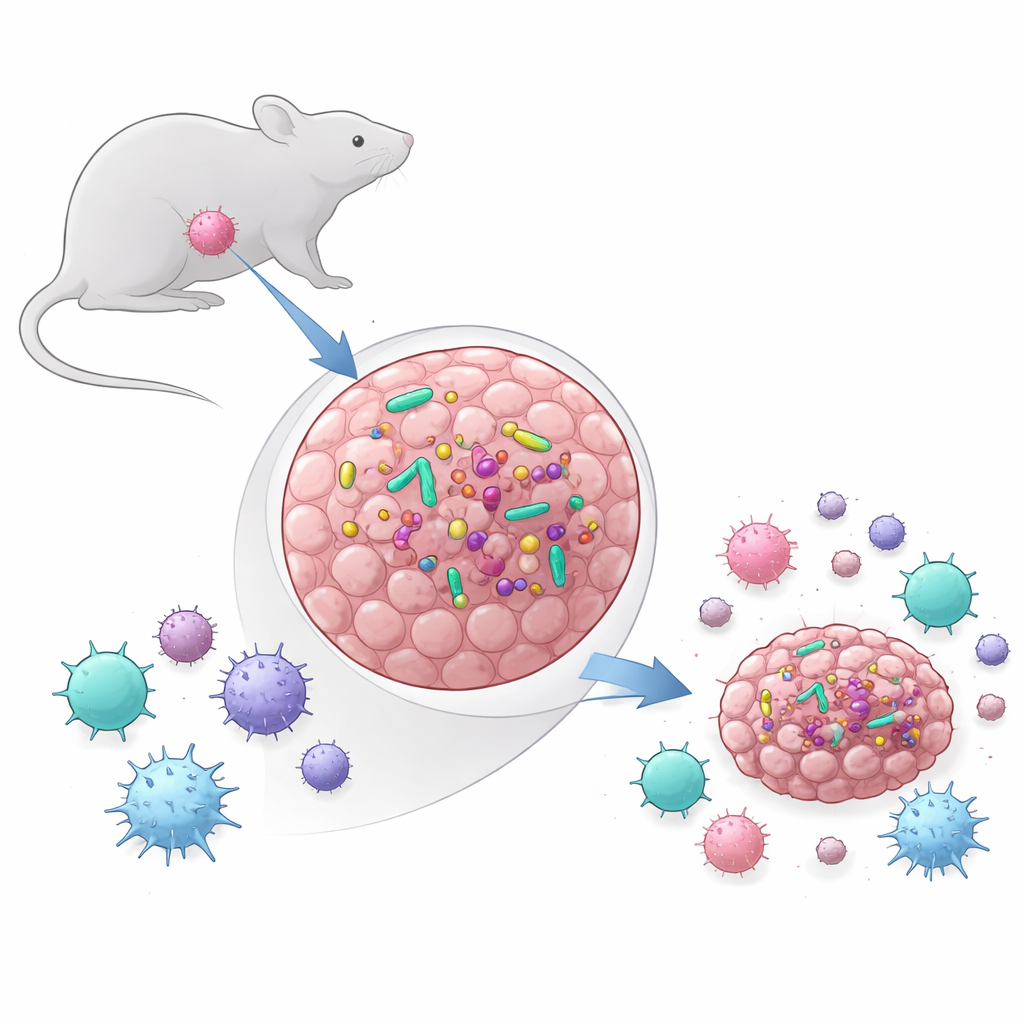
Opsporen waar de beestjes vandaan komen
Het aantreffen van bacteriën in tumoren riep een volgende vraag op: komen deze indringers van de huid, de mond of de darmen? Door het bacteriële DNA in tumoren te vergelijken met monsters uit ontlasting, huidswabs en mondswabs, vonden de onderzoekers dat de intratumorale gemeenschap eenvoudiger en minder divers was dan de rijke ecosystemen in darm en mond. De meeste bacterietypes in tumoren overlappen met die in het maag-darmkanaal, terwijl relatief weinig overeenkwam met de huid. Dit suggereert dat bacteriën via lekkage uit de darmen of mond in de bloedbaan terechtkomen en vervolgens de tumor inzaaien, waar slechts bepaalde soorten erin slagen te blijven bestaan. De samenstelling van bacteriegroepen weerspiegelde die in meerdere menselijke kankers, wat versterkt dat deze muistumoren echte tumor–microbe-interacties kunnen modelleren.
Hoe tumorbacteriën het succes van immunotherapie vormen
De kernbevinding is dat bacteriën in tumoren het succes van anti–PD-1-therapie, een checkpointremmer die uitgeputte cytotoxische T-cellen weer actief maakt, kunnen maken of breken. Wanneer het team antibiotica gebruikte die in de tumor doordrongen en lokale bacteriën uitroeiden terwijl de darmkolonisatie grotendeels gespaard bleef, werden MCA-205-tumoren veel minder responsief op anti–PD-1. De responsen nam nog sterker af wanneer de darmmicrobiota breed verstoord werden. Daarentegen hadden antibiotica bij MOC1-tumoren, die van meet af aan geen detecteerbare bacteriën bevatten, weinig effect op zowel de bacteriële belasting als de behandeluitkomst. In MCA-205-tumoren die reageerden op anti–PD-1 zaten doorgaans meer bacteriën dan in tumoren die therapieresistent waren, wat een hogere intratumorale bacteriële last koppelt aan betere groeiremming.
In het immuunstrijdperk
Om te begrijpen hoe bacteriën het immuunevenwicht beïnvloeden, onderzochten de onderzoekers immuuncellen in en rond de tumoren. Wanneer intratumorale bacteriën werden verwijderd met tumor-penetrerende antibiotica, infiltreerden minder cytotoxische CD8 T-cellen de tumor, en verschoof de verhouding tussen deze cellen en regulerende T-cellen in de richting van onderdrukking. Dendritische cellen, de verkenners die tumormateriaal oppikken en T-cellen activeren, waren eveneens in mindere aantallen aanwezig en toonden minder activeringssignalen bij afwezigheid van bacteriën. Interessant genoeg gaf het simpelweg toevoegen van een extra stam goedaardige E. coli in de tumor, of het uitschakelen van een belangrijk microbe-detectiepad (MyD88) in sleutelimmuuncellen, geen boost voor de therapie. Dit impliceert dat niet elke bacteriële aanwezigheid of simpele alarmmelding volstaat; specifieke gemeenschappen en meer genuanceerde communicatie met het immuunsysteem zijn waarschijnlijk vereist.
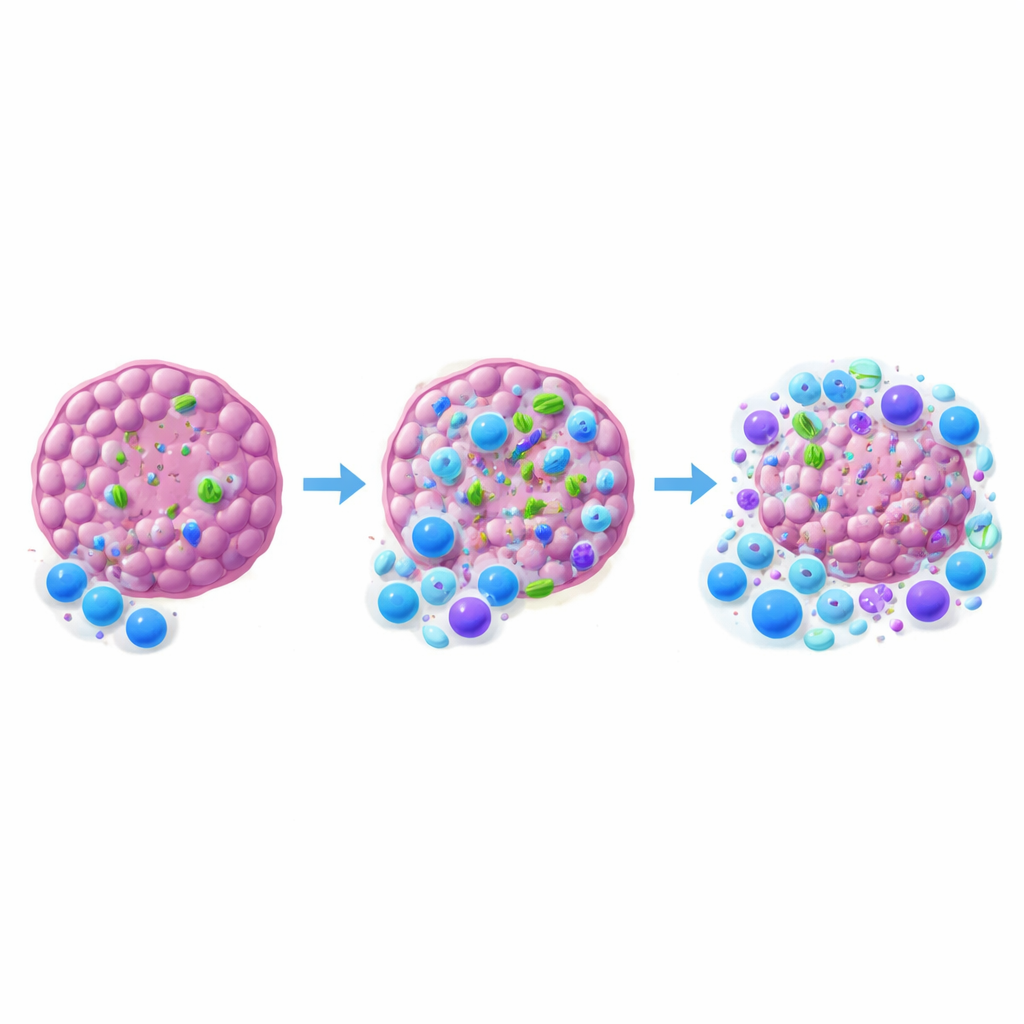
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat bacteriën in tumoren geen passanten zijn. In ten minste sommige kankers helpen ze de juiste immuuncellen naar de tumor te lokken en ondersteunen ze de werking van anti–PD-1-middelen. Andere tumoren kunnen vrijwel vrij van bacteriën blijven en zeer anders reageren. Terwijl wetenschappers nieuwe behandelingen in muismodellen ontwerpen en testen, kan het essentieel zijn om te weten of een bepaald tumor-model bacteriën draagt — en welke soorten — om resultaten correct te interpreteren en strategieën te kiezen die naar patiënten vertalen. Op de lange termijn kan het zorgvuldig afstemmen van de kleine gemeenschappen binnen tumoren zelf drugs en immuuncellen aanvullen als een nieuw hulpmiddel om kankerimmunotherapie te verbeteren.
Bronvermelding: Rolig, A.S., Ziglari, T., McGee, G.H. et al. Bacterial colonization of tumors drives immune activation and checkpoint blockade efficacy. Sci Rep 16, 8464 (2026). https://doi.org/10.1038/s41598-026-39758-z
Trefwoorden: intratumorale microbiota, kankerimmunotherapie, anti-PD-1, tumormicro-omgeving, bacteriën en tumoren