Clear Sky Science · nl
Cryptische redundantie tussen PAR1b en PAR1a, twee leden van de PAR1-kinasefamilie, in het overleven van PAR1b-knockoutmuizen
Hoe cellen noodplannen vinden voor beschadigd DNA
Onze cellen krijgen voortdurend te maken met DNA-schade, en wanneer reparatiesystemen falen, kan dat leiden tot kanker of vroegtijdig ontwikkelingsverlies. Deze studie onderzoekt een verrassend reddingsmechanisme in muizen: wanneer een sleutelproteïne die het beroemde kankergene BRCA1 helpt zijn werk te doen ontbreekt, treedt een nauw verwant eiwit stilletjes in de plaats. Het werk laat zien hoe vroege embryo’s hun genregulatie kunnen herbedraden om te overleven, en biedt nieuw inzicht in waarom sommige genetische defecten dodelijk zijn terwijl andere onverwacht worden getolereerd.
Een familie van celorganisatoren met een verborgen rol
Onderzoekers richtten zich op een familie enzymen genaamd PAR1-kinasen, die cellen helpen hun interne organisatie te behouden. Een lid van de familie, PAR1b, bleek eerder BRCA1 naar de celkern te leiden, waar BRCA1 zorgt voor nauwkeurig DNA-herstel en het beschermen van kwetsbare replicatieplaatsen. Het volledig verwijderen van BRCA1 in muizen is vroeg in de embryonale ontwikkeling fataal, wat het belang ervan onderstreept. Verwarrend genoeg overleven muizen die volledig PAR1b missen echter tot volwassenheid, ondanks dat PAR1b stroomopwaarts van BRCA1 werkt. Deze discrepantie suggereerde dat een andere PAR1-kinase onder bepaalde omstandigheden stilletjes PAR1b zou kunnen vervangen.
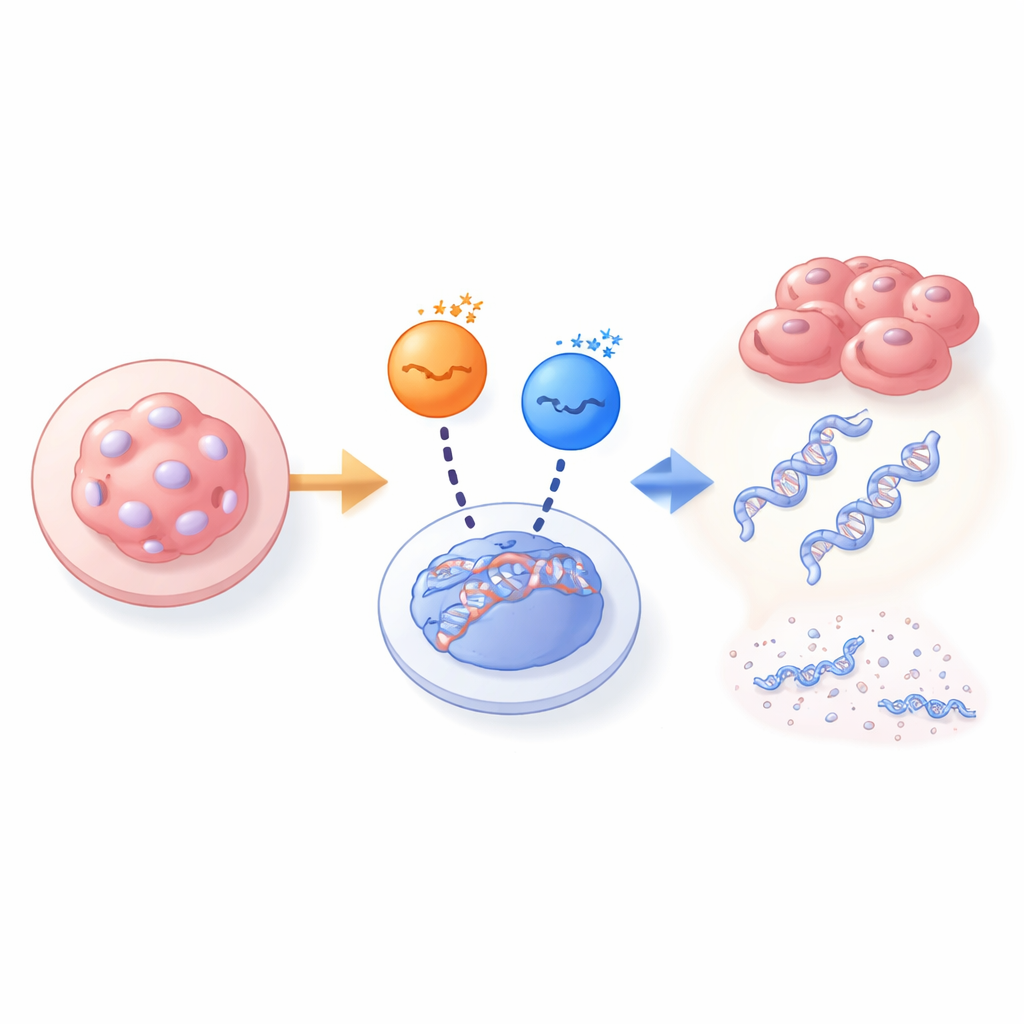
Als de ene kinase faalt, treedt een andere in
Om dit mysterie te onderzoeken vergeleek het team muisembryonale fibroblasten afkomstig van normale embryo’s met die van embryo’s die volledig PAR1b misten. In normale cellen leidde het uitschakelen van PAR1b tot een scherpe vermindering van BRCA1 in de kern en tot een uitbarsting van DNA-breekmarkers, wat op zijn beurt de celgroei blokkeerde. Het neerhalen van andere PAR1-kinasen (PAR1a, PAR1c, PAR1d) had weinig effect. In cellen afkomstig van PAR1b-knockoutembryo’s bleef BRCA1 echter in de kern aanwezig en bleef het DNA relatief intact, ondanks afwezigheid van PAR1b. In deze PAR1b-nullcellen werd het verwijderen van PAR1a nu lethaal, terwijl het verwijderen van PAR1c of PAR1d dat niet deed. Deze omschakeling in afhankelijkheid toonde aan dat PAR1a de rol van PAR1b in het begeleiden van BRCA1 had overgenomen, maar alleen in embryo’s die vanaf het allereerste begin PAR1b misten.
Vroege epigenetische herbedrading als overlevingsstrategie
De onderzoekers vermoedden dat dit verborgen back-upsysteem verband hield met epigenetica—de manier waarop DNA wordt verpakt en chemisch gemerkt om genen aan of uit te zetten zonder de genetische code te veranderen. Met een genoomwijde assay voor chromatintoegankelijkheid vonden ze duizenden gebieden waar de toegankelijkheid van DNA verschilde tussen normale en PAR1b-nullcellen. Veel veranderingen betroffen genen die regelen hoe chromosomen worden gewikkeld en gemodificeerd, wat wijst op een brede herprogrammering van het genregelnetwerk. Een opvallend effect trof het gen voor 53BP1, een eiwit dat cellen normaal gesproken naar een snelle maar onnauwkeurige reparatieweg duwt die BRCA1’s meer nauwkeurige methode tegenwerkt. In PAR1b-nullcellen was het lichaam van het 53BP1-gen strakker verpakt en waren de RNA- en eiwitniveaus veel lager.
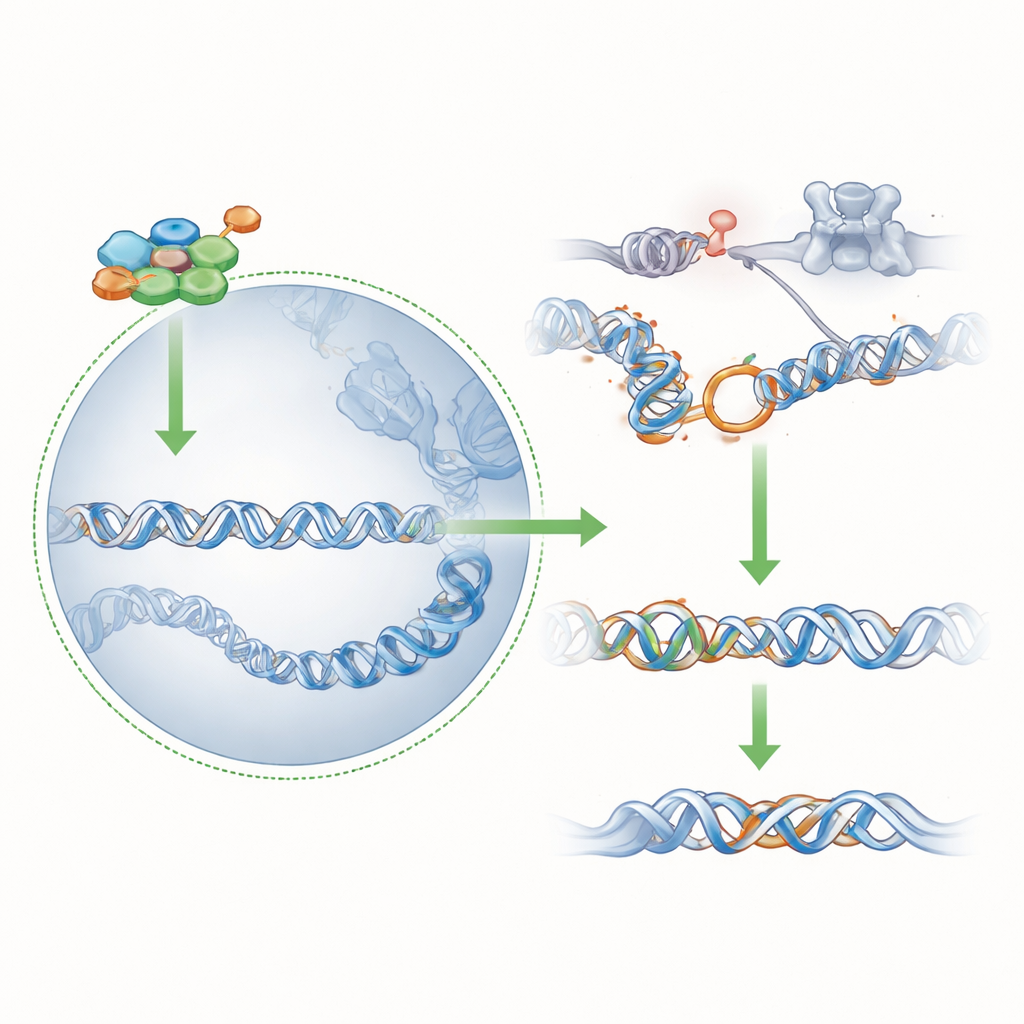
Het evenwicht tussen reparatieroutes doen kantelen
Door 53BP1 naar beneden bij te stellen vermindert het embryo effectief zijn afhankelijkheid van de volle kracht van BRCA1: zelfs een bescheiden hoeveelheid kern-BRCA1, geleverd door PAR1a in plaats van PAR1b, kan nu voldoende nauwkeurig herstel ondersteunen om cellen in leven te houden. Experimenten met een bacterieel eiwit dat alle PAR1-kinasen uitschakelt, bevestigden dat BRCA1’s aanwezigheid in de kern van PAR1b-nullcellen nog steeds afhangt van PAR1-familieactiviteit, specifiek PAR1a. Gezamenlijk schetsen de resultaten het beeld dat vroeg verlies van PAR1b een snelle herschikking van chromatine en DNA-herstelnetwerken oproept, waarbij een tegenstander van BRCA1 (53BP1) wordt gesmoord en PAR1a’s vermogen om voor PAR1b in te springen wordt onthuld.
Wat dit betekent voor ziekte en behandeling
Dit werk introduceert het idee van “cryptische redundantie”: een back-upfunctie die bestaat maar normaal gesproken inactief is en pas zichtbaar wordt wanneer een sleutelcomponent zeer vroeg in de ontwikkeling verloren gaat. Bij muizen maakt dit het embryo mogelijk het verlies van PAR1b te overleven, in tegenstelling tot het verlies van BRCA1 zelf. De bevindingen suggereren ook dat sommige mensen met schadelijke PAR1b-varianten kunnen overleven omdat soortgelijke back-upmechanismen in werking treden, hoewel dat niet zonder mogelijke gevolgen is voor hersenfunctie, stofwisseling of kankerrisico. Op de lange termijn kan inzicht in hoe vroege epigenetische aanpassingen 53BP1 stilleggen en de BRCA1-regulatie van PAR1b naar PAR1a verschuiven, strategieën inspireren om deze veranderingen opzettelijk na te bootsen—of om cellen te beschermen die PAR1b hebben verloren, of om DNA-herstelroutes in de kankertherapie fijn af te stemmen.
Bronvermelding: Murata-Kamiya, N., Del Valle Lazarte, A.A., Kikuchi, I. et al. Cryptic redundancy between PAR1b and PAR1a, two members of the PAR1 kinase family, in the survival of PAR1b-knockout mice. Sci Rep 16, 5971 (2026). https://doi.org/10.1038/s41598-026-39737-4
Trefwoorden: BRCA1, DNA-herstel, kinase-redundantie, epigenetische regulatie, embryonale ontwikkeling