Clear Sky Science · nl
Autismespectrumstoornis-geassocieerde Sema5A p.Arg676Cys activeert Arf6/FE65-signaalroute en veroorzaakt afwijkende celmorfogenese
Hoe een kleine verandering de bedrading van de hersenen kan verstoren
Autismespectrumstoornis beïnvloedt hoe mensen communiceren, omgaan met anderen en reageren op hun omgeving, maar de biologische stappen die van een DNA-verandering naar een veranderde hersenfunctie leiden, zijn vaak onduidelijk. Deze studie onderzoekt zo’n genetische verandering in een hersen‑"geleidings"-eiwit genaamd Sema5A en toont, met uitzonderlijk veel detail, hoe één verwisseld bouwsteen in dat eiwit jonge zenuwcellen ertoe kan aanzetten te veel en te lange vertakkingen te laten groeien. Inzicht in deze microscopische bedradingfout kan onderzoekers uiteindelijk helpen bij het ontwerpen van behandelingen die hersencellen weer naar een gezondere vorm sturen.
Zenuwcellen die te ver groeien
Tijdens de ontwikkeling van de hersenen sturen jonge zenuwcellen lange, dunne uitlopers uit die naar de juiste partners zoeken en zo de circuits vormen die denken en gedrag mogelijk maken. Deze groei moet strak geregeld worden: te weinig vertakking en cellen maken geen verbindingen; te veel en circuits kunnen lawaaierig of verkeerd aangesloten raken. Eerder werk toonde aan dat een aan autisme gelinkte variant van Sema5A, waarbij één aminozuur op positie 676 veranderd is van arginine naar cysteïne, zenuwcellen in kweek ongewoon lange uitlopers doet vormen. De nieuwe studie wilde uitzoeken welke interne schakelaars en hulp‑eiwitten deze mutant‑Sema5A gebruikt om zulke ongeremde groei te veroorzaken.
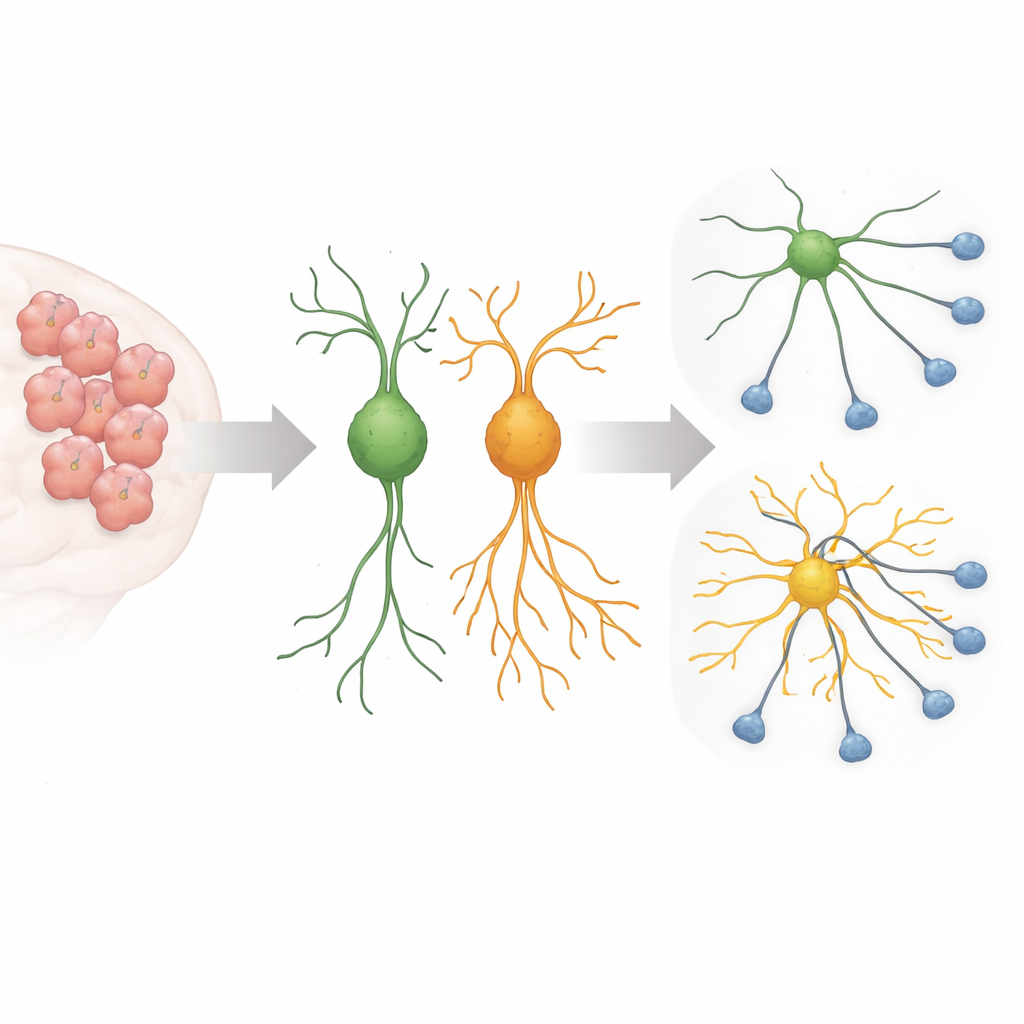
Een misleidend signaal binnenin de cel
De onderzoekers richtten zich op een kleine moleculaire schakelaar genaamd Arf6 en een scaffold‑eiwit genaamd FE65, die beide bekendstaan om hun rol bij het vormen van celmembranen en het interne skelet dat celuitlopers ondersteunt. Met behulp van een CRISPR–Cas13‑systeem om deze eiwitten selectief te verminderen in muisachtige zenuwcellen en in primaire muizenhersencellen, vonden ze dat het terugschakelen van Arf6 of FE65 de overmatige uitgroei veroorzaakt door de mutant‑Sema5A sterk verminderde. De lange, spinachtige uitlopers krimpten naar meer typische lengtes, en markers van neuronale rijping daalden, wat suggereert dat het effect van de mutatie sterk afhankelijk is van juist deze signaalroute.
Aansluiting op de vormmotor van de cel
In zenuwcellen fungeert een familie moleculen als een vorm"motor" door actine te regelen, het belangrijkste structurele filament in celvertakkingen. Een sleutellid van deze familie, Rac1, wordt gewoonlijk actief om neurieten te laten uitgroeien, maar te veel activiteit kan ongeremde groei aandrijven. Het team toonde aan dat in cellen met normale Sema5A Arf6 nodig is voor gewone Rac1‑activatie tijdens gezonde uitgroei, terwijl FE65 niet essentieel is. Met de mutant‑Sema5A werden echter zowel Arf6 als FE65 cruciaal: het verminderen van een van beiden, of het overspoelen van de cel met alleen het FE65‑domein dat bindt aan zijn partner ELMO2, bracht de abnormaal hoge Rac1‑activiteit terug richting normaal. Dit wijst erop dat de schadelijke versie van Sema5A specifiek aanboort op een Arf6–FE65–ELMO2–DOCK5 complex om Rac1 te overstimuleren en neurieten te ver laten uitgroeien.
Een druk knooppunt van signaalpartners
Om te zien hoe deze onderdelen samenhangen, onderzochten de wetenschappers ook ELMO2‑gebaseerde "signalosomen"—eiwitclusters die zich vormen om groeisignalen door te geven. Wanneer Arf6 of FE65 verminderd werd, vormden cellen die de mutant‑Sema5A tot expressie brachten minder van deze ELMO2‑complexen in hun cellichamen en groeipunten, wat consistent is met het idee dat Arf6 en FE65 helpen het apparaat op te bouwen dat de Sema5A‑mutatie omzet in een fysieke verandering van de celvorm. Het werk past in een breder beeld waarin kleine moleculaire schakelaars zoals Arf6 en Rac1, geholpen door scaffolds als FE65, fungeren als centrale knooppunten die vele autisme‑geassocieerde genen verbinden met de uiteindelijke architectuur van hersencircuits.
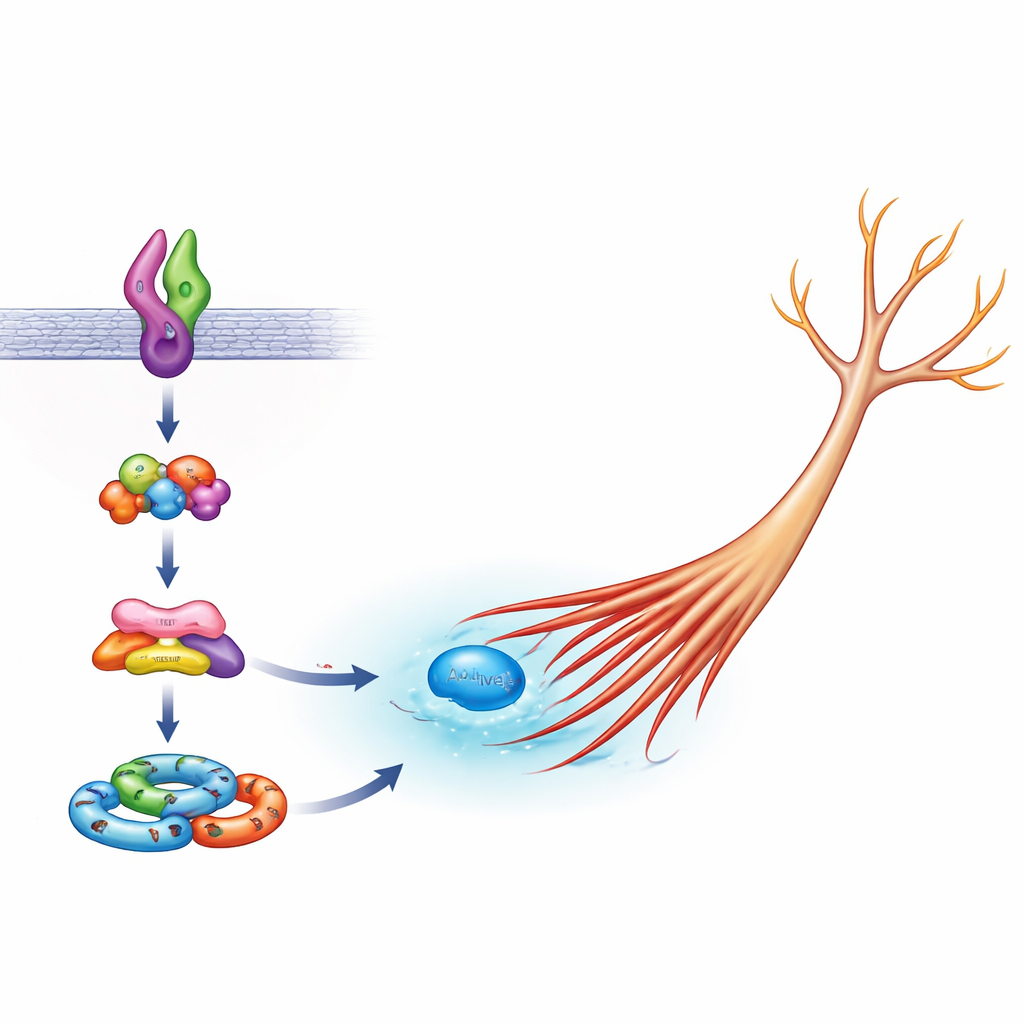
Waarom deze microscopische keten ertoe doet
Voor niet‑specialisten kan de afkortingenbrij van eiwitnamen ver afstaan van de dagelijkse ervaring van autisme. Toch biedt deze studie een concrete brug: ze traceert hoe een precieze genetische verandering in Sema5A een specifieke keten van helpermoleculen kan overactiveren, waardoor zenuwcellen hun vertakkingen te ver laten groeien en mogelijk de hersenen op atypische wijze bedraden. Door Arf6, FE65 en het ELMO2‑signaalcomplex als cruciale schakels in deze keten aan te wijzen, benadrukt het werk mogelijke toekomstige medicatiedoelen. In principe zouden medicijnen die deze overactieve route zachtjes dempen op een dag kunnen helpen de onderliggende celvormveranderingen geassocieerd met Sema5A‑gerelateerde vormen van autisme te corrigeren, en zo een belangrijk stuk toevoegen aan de bredere puzzel van neuro‑ontwikkelingsstoornissen.
Bronvermelding: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Trefwoorden: autismespectrumstoornis, Sema5A-mutatie, neurale morfogenese, Rac1-signaaltransductie, Arf6 FE65-route