Clear Sky Science · nl
Richting van specifieke neuronale typen in het niet-menselijke primatenbrein met een muisspecifiek CD25-recombinant immunotoxine
Waarom deze hersenstudie ertoe doet
Begrijpen hoe specifieke groepen hersencellen beweging, emotie en gedrag aansturen is essentieel voor de behandeling van aandoeningen zoals de ziekte van Parkinson en autisme. Maar de hersenen zijn een dicht bos van verstrengelde cellen, en de meeste instrumenten kappen veel bomen tegelijk. Deze studie beschrijft een manier om slechts één gekozen type neuron in het brein van een aap te verwijderen, met minimale nevenschade, wat de deur opent naar scherpere experimenten over hoe specifieke circuits gedrag en ziekte vormen.
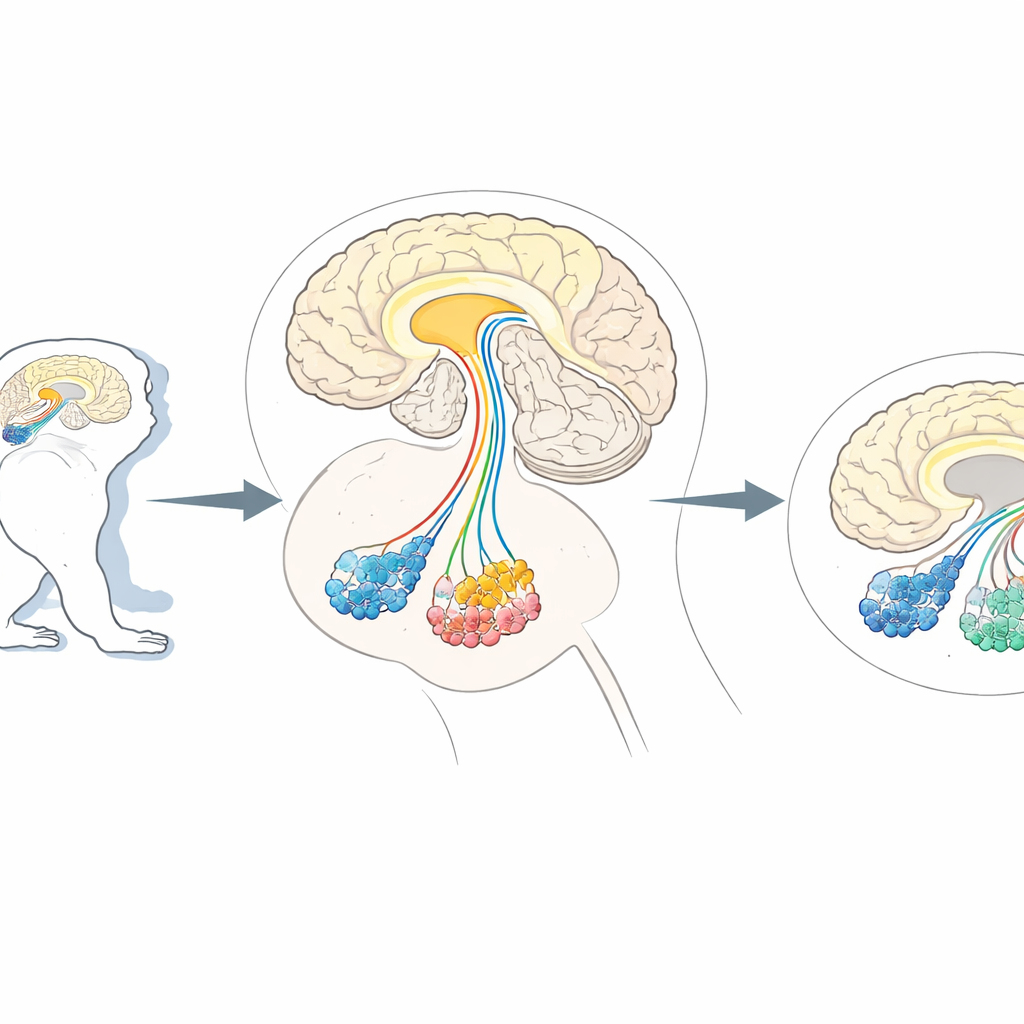
Een behoefte aan precieze "cel snoei" in de hersenen
Onderzoekers gebruiken vaak niet-menselijke primaten, zoals marmosets en makaakken, omdat hun hersenorganisatie sterk op die van ons lijkt. Deze dieren zijn onmisbare modellen voor aandoeningen die hogere hersenfuncties aantasten, van Parkinson-achtige bewegingsproblemen tot autisme-achtige veranderingen in sociaal gedrag. Huidige methoden kunnen specifieke paden dempen of stimuleren, maar daadwerkelijk één type neuron verwijderen in deze complexe hersenen zonder andere cellen te schaden blijft moeilijk. Eerder werk bij muizen gebruikte een truc: geselecteerde neuronen werden zodanig gemanipuleerd dat ze een menselijke cel-oppervlaktemarkering genaamd CD25 uitdrukten, die herkend kon worden door een ontworpen toxine dat alleen die gemarkeerde cellen doodt. Dezezelfde marker komt echter van nature voor in primatens immuniteit en mogelijk ook in sommige hersencellen, wat het risico vergroot dat het toxine in apen de verkeerde doelen aanvalt.
Ontwikkeling van een veiliger moleculair scalpel
De auteurs wilden een nieuw moleculair scalpel ontwikkelen dat geschikt is voor gebruik bij primaten. In plaats van de menselijke versie van CD25 te targeten, richtten ze zich op de muisversie, die veel minder lijkt op de natuurlijke CD25 in apen. Ze immuniseerden eerst een konijn met het muis-CD25-eiwit en gebruikten een chip-gebaseerde methode om individuele konijnencellen te selecteren die antilichamen produceerden die sterk binden aan muis-CD25 maar niet aan de menselijke vorm. Vanuit deze selectie identificeerden ze een uitblinkend antilichaam, RMAb-52, met zeer hoge bindingssterkte. Ze stelden vervolgens de sleutelonderdelen van dit antilichaam samen met een toxisch fragment van de bacterie Pseudomonas om één enkel geconstrueerd "immunotoxine"-eiwit te maken, genaamd anti-mCD25-PE38.
Het instrument op de proef stellen
In reageerbuisexperimenten greep het nieuwe immunotoxine veel sterker aan op muis-CD25 dan op menselijke CD25, wat de selectiviteit bevestigde. Toegepast op gekweekte cellen die waren gemodificeerd om muis-CD25 te dragen, verminderde het toxine hun overleving sterk bij zeer lage doses, terwijl cellen met menselijke CD25 onaangetast bleven. Vervolgens ging het team naar levende marmosets. Met een speciaal viraal vector dat achterwaarts langs zenuwvezels reist, brachten ze het muis-CD25-gen in dopaminerge neuronen die signalen sturen van een diep hersengebied, de substantia nigra, naar het striatum — een pad dat cruciaal is voor bewegingscontrole. Nadat ze het virus tijd hadden gegeven om de marker in deze neuronen aan te zetten, injecteerden ze het anti-mCD25-PE38-eiwit rechtstreeks in het doelgebied in het middenbrein.
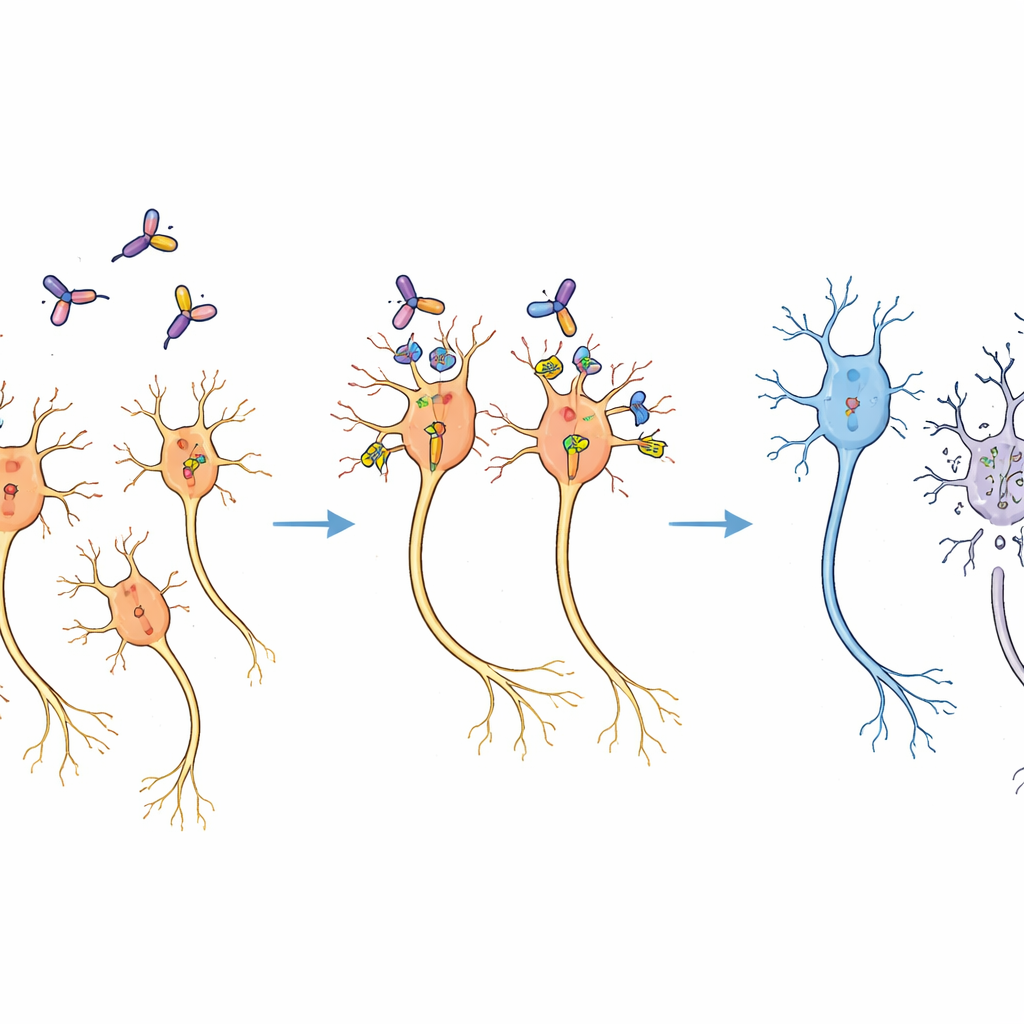
Selectief verlies zonder wijdverspreide schade
Twee weken na de behandeling vertelden hersensneden van de marmosets een duidelijk beeld. Aan de kant die het immunotoxine had ontvangen, was het aantal dopaminerge neuronen teruggebracht tot ongeveer twee derde van dat aan de niet-behandelde kant, zoals aangetoond door kleuring voor een dopamineproducerend enzym. Toch zag het omliggende hersenweefsel er normaal uit onder de microscoop, en andere hersengebieden die ook het virale vector ontvingen, toonden geen duidelijk celverlies. Pilootexperimenten hadden al een dosisbereik vastgesteld dat niet-specifieke weefselschade vermijdt, en de gekozen dosis lag ruim binnen dit veilige venster. Het patroon van verlies kwam overeen met de verwachte verspreiding van virus en toxine, wat aangeeft dat neuronen specifiek werden geëlimineerd omdat ze waren gemodificeerd om muis-CD25 uit te drukken, en niet omdat het toxine cellen ongericht beschadigde.
Wat dit betekent voor toekomstig hersenonderzoek
Voor een niet-specialistische lezer is de kernboodschap dat de onderzoekers een zeer selectieve verwijderknop hebben ontwikkeld voor gekozen neuronpopulaties in primatenhersenen. Door een retrograad viraal leveringssysteem te combineren met een muisspecifiek immunotoxine, kunnen ze gedefinieerde paden wegnemen — bijvoorbeeld dopaminerge circuits die betrokken zijn bij de ziekte van Parkinson — terwijl omliggende cellen gespaard blijven. Deze strategie voorkomt gevaarlijke kruisreacties met de eigen CD25 van het dier en zal vooral nuttig zijn wanneer die natuurlijke receptor aanwezig is of verhoogd in ziekte. Op de lange termijn zal deze aanpak wetenschappers helpen in kaart te brengen hoe individuele routes in het hersenbedradingsnetwerk bijdragen aan beweging, besluitvorming en psychiatrische symptomen, en ons dichter bij gerichte behandelingen brengen die foutieve circuits bijsturen in plaats van het hele brein breed aan te pakken.
Bronvermelding: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Trefwoorden: niet-menselijke primaten neurowetenschap, immunotoxine gericht, dopaminerge neuronen, marmoset hersencircuits, modellen van de ziekte van Parkinson