Clear Sky Science · nl
Hypoxie-induceerbare factor 1α oefent dubbele rollen uit in de progressie van blaaskanker via TIMP3-gemedieerde regulatie van angiogenese en invasie
Waarom zuurstofarme tumoren ertoe doen
Kankercellen groeien vaak zo snel dat ze hun bloedvoorziening voorbijstreven, waardoor delen van een tumor van zuurstof verstoken raken. Deze zuurstofarme, of hypoxische, omgeving dwingt cellen overlevingsprogramma’s in te schakelen die kankers moeilijker behandelbaar kunnen maken. Bij blaaskanker—een veelvoorkomende tumor van de urinewegen—vermoedden wetenschappers lange tijd dat één van die zuurstof‑sensorische programma’s, gereguleerd door een eiwit genaamd HIF-1α, voornamelijk tumorgroei en -verspreiding bevordert. Deze studie kijkt daar nauwkeuriger naar en vindt een verrassende wending: onder bepaalde omstandigheden kan het terugdringen van HIF-1α blaaskankercellen juist agressiever maken, en een tweede eiwit, TIMP3, blijkt centraal te staan in dit paradoxale effect.
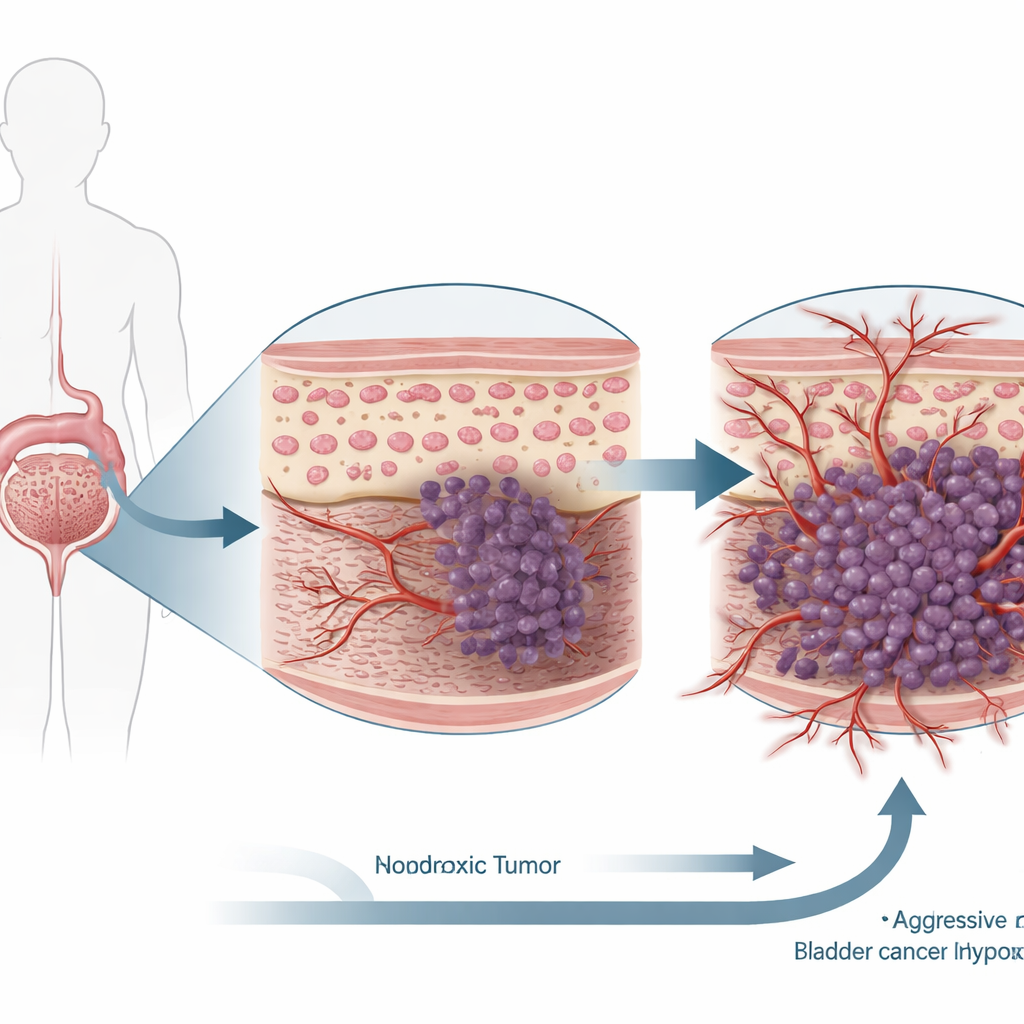
Een nadere blik op blaaskankercellen
De onderzoekers werkten met twee goed gevestigde menselijke blaaskanker-celijnen en stelden ze bloot aan normale zuurstofniveaus of aan hypoxie, waarmee de zuurstofarme plekjes in echte tumoren werden nagebootst. Vervolgens gebruikten ze genetische middelen om HIF-1α in deze cellen te verlagen en maten hoe deze wijziging de basale kankereigenschappen beïnvloedde: hoe snel de cellen zich vermenigvuldigden, hoe vatbaar ze waren voor celdood, en hoe goed ze zich konden verplaatsen, door een barrière heen konden invaseren en nieuwe bloedvaten konden stimuleren om te vormen. Parallel daaraan onderzochten ze blaastumor-monsters van patiënten om de niveaus van HIF-1α en TIMP3 in kankergezwellen te vergelijken met nabijgelegen normaal blaasweefsel.
Een verrassende rolomkering bij lage zuurstof
Patiëntmonsters bevestigden dat HIF-1α inderdaad hoger is in blaastumoren dan in normaal weefsel, in overeenstemming met zijn reputatie als tumorpromoterend factor. Toch had het in de celexperimenten onder hypoxie verminderen van HIF-1α het tegengestelde effect van wat velen zouden verwachten. Wanneer HIF-1α werd onderdrukt en zuurstof schaars was, groeiden kankercellen in de loop van de tijd sneller, waren ze minder geneigd geprogrammeerde celdood te ondergaan en werden ze beter in migratie en invasie door modelbarrières. Ze gaven ook signalen af die vaatcellen aanmoedigden om dichtere, meer uitgebreide buisachtige netwerken te vormen, een kenmerk van verhoogde tumorbloedvoorziening. Kortom: met minder HIF-1α in een zuurstofarme omgeving gedroegen blaaskankercellen zich maligner.
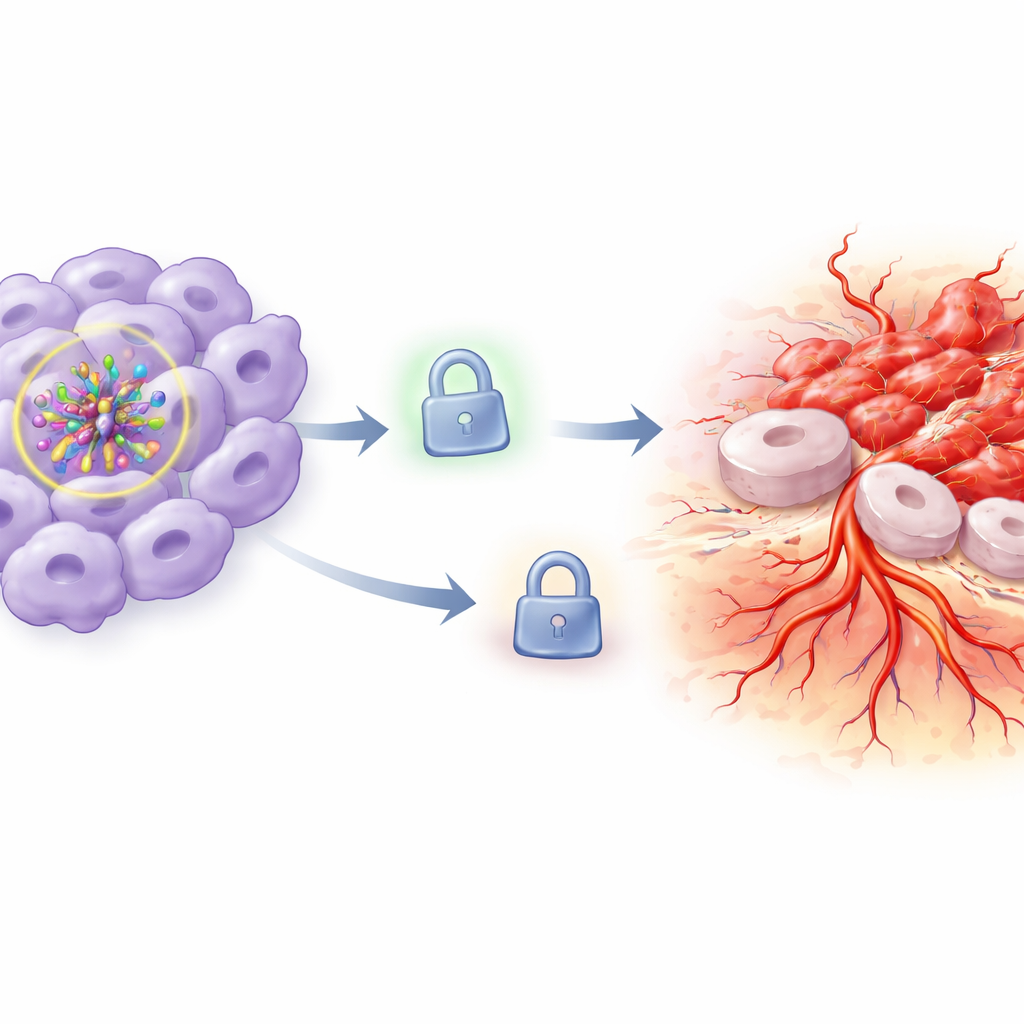
Het ontbrekende remmechanisme op tumorspread
Om te begrijpen waarom dit gebeurde, richtte het team zich op TIMP3, een eiwit dat normaal fungeert als rem op weefselafbraak en nieuwe vaangroei door enzymen te blokkeren die de omringende matrix afbreken. In cellen met verlaagd HIF-1α die onder normale zuurstof werden gehouden, bleef het TIMP3-niveau relatief hoog. Maar wanneer de zuurstofniveaus daalden, viel het TIMP3-eiwit scherp terug. Dit verlies aan TIMP3 paste goed bij de waargenomen toename in invasie en vaatvorming: met de rem verzwakt konden kankercellen hun omgeving gemakkelijker herstructureren en uitbreiden. De onderzoekers draaiden daarna de knop om door cellen extra TIMP3 te laten produceren terwijl HIF-1α nog steeds was onderdrukt onder hypoxie. Het herstellen van TIMP3 keerde het agressieve gedrag gedeeltelijk of vrijwel volledig om: cellen groeiden minder, stierven gemakkelijker, bewoog en invadeerden minder en veroorzaakten minder en kortere vaatachtige buisjes.
Wat dit betekent voor toekomstige behandelingen
Deze bevindingen suggereren dat HIF-1α een dubbele persoonlijkheid heeft in blaaskanker. Enerzijds zijn de algehele niveaus hoger in tumoren en helpt het bekende kankervriendelijke programma’s aan te sturen. Anderzijds lijkt het onder ernstige zuurstoftekort de beschermende aanwezigheid van TIMP3 te ondersteunen. Het verwijderen van HIF-1α in die context kan onbedoeld TIMP3 verlagen en meer invasief, vaatbevorderend gedrag ontketenen. Voor therapie betekent dit dat het eenvoudigweg blokkeren van HIF-1α averechts kan werken, tenzij artsen ook manieren vinden om TIMP3, of soortgelijke remmen, in stand te houden. Het werk benadrukt het belang van het begrijpen van niet alleen individuele doelwitten, maar het bredere netwerk van checks-and-balances dat bepaalt hoe een tumor reageert op zijn harde, zuurstofarme omgeving.
Bronvermelding: Wang, X., Guo, J., Zhang, R. et al. Hypoxia-inducible factor 1α exerts dual roles in bladder cancer progression through TIMP3-mediated regulation of angiogenesis and invasion. Sci Rep 16, 8425 (2026). https://doi.org/10.1038/s41598-026-39635-9
Trefwoorden: blaaskanker, tumorhypoxie, HIF-1α, TIMP3, angiogenese