Clear Sky Science · nl
Een multimodale zebravis-toolbox om de bloed-hersenbarrière te bestuderen in gezondheid en ziekte
Waarom lekkende hersenvaten ertoe doen
Als bloedvaten in de hersenen of het oog gaan lekken, sijpelen vocht en eiwitten in het omliggende zenuwweefsel en veroorzaken ze zwelling die het zicht kan vertroebelen of het denken kan belemmeren. Dit soort “verzadiging” — bekend als vasogeen oedeem — speelt een rol bij diabetische gezichtsverlies, beroerte, hersenletsel en sommige vormen van dementie. Toch ontbreekt het onderzoekers nog aan eenvoudige, betaalbare methoden om deze beschermende barrière in realtime te volgen wanneer ze faalt. Deze studie introduceert een veelzijdig zebravismodel waarmee onderzoekers kunnen zien, meten en onderzoeken hoe hoge bloedsuiker de vaatbarrière van de hersenen verzwakt, wat mogelijk het zoeken naar nieuwe behandelingen kan versnellen.
Een kleine vis met een duidelijk voordeel
Zebravislarven bieden een uniek venster op het levende brein. In tegenstelling tot zoogdieren zijn hun lichamen in de vroege levensfase transparant en kunnen hun hersenbloedvaten onder de microscoop zichtbaar worden gemaakt. De auteurs maakten hier gebruik van door zich te richten op de bloed–hersenbarrière, de strakke afdichting tussen bloed en hersenweefsel die lijkt op de binnenste bloed-retinabarrière die onze ogen beschermt. Omdat dezelfde celtypen en veel van dezelfde beschermende eiwitten worden gedeeld tussen hersenen en netvlies, gebruikte het team de hersenbarrière in zebravissen als vervanging om ziekten te bestuderen zoals diabetisch maculaoedeem en andere neurovasculaire aandoeningen, maar in een sneller, ethischer en goedkoper systeem dan traditionele knaagdiermodellen.
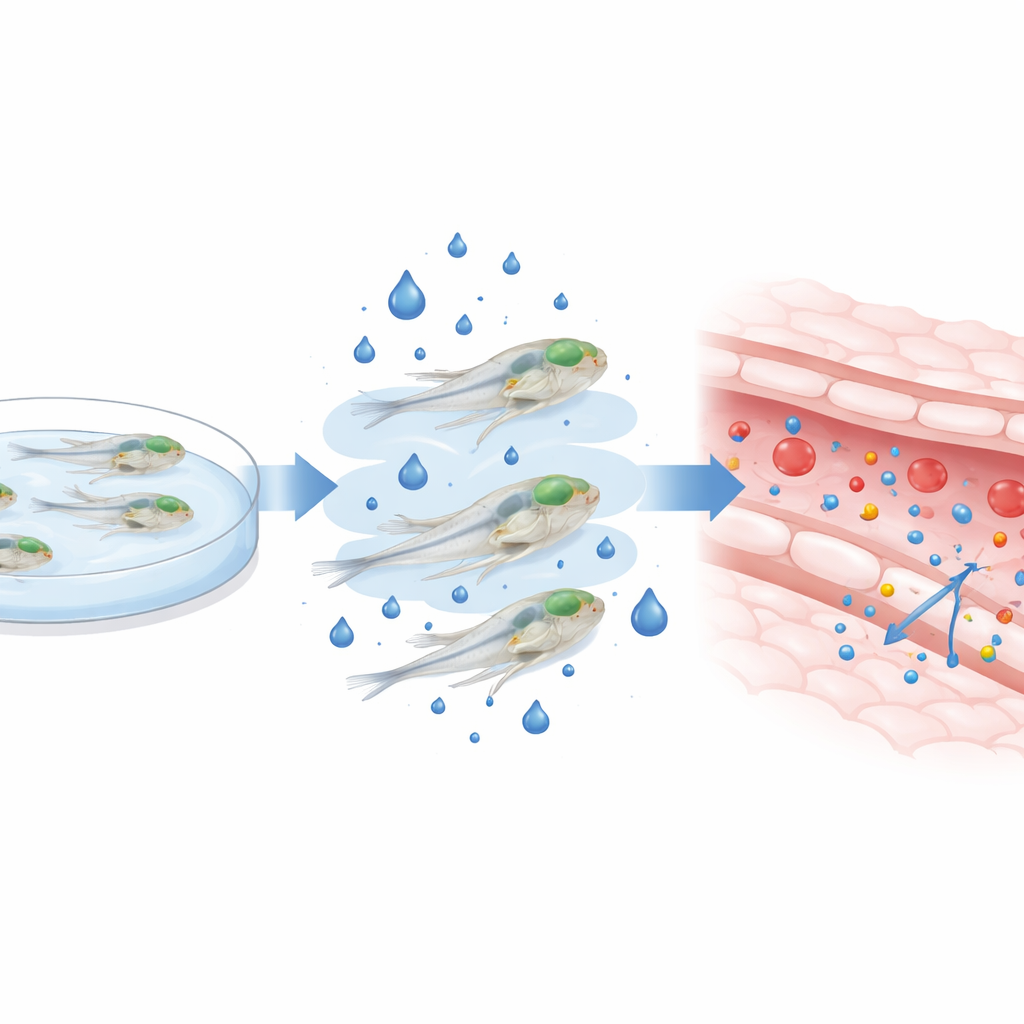
Bloedsuiker verhogen bij jonge zebravissen
Om de hoge bloedsuiker bij diabetes na te bootsen, hielden de onderzoekers zebravislarven tussen de drie en vijf dagen na bevruchting in water met extra glucose — een cruciale periode waarin de hersenbarrière nog rijpt. Ze bevestigden dat dit externe suikerritme de interne glucosewaarden meerdere malen verhoogde zonder de larven te doden of hun algemene vorm te veranderen. Met de vissen nog levend en zwemmend, injecteerden ze fluorescerende kleurstoffen van verschillende groottes in de circulatie en gebruikten ze hoogresolutieconfocale microscopen om te volgen hoeveel kleurstof uit de hersenbloedvaten lekte in het omliggende weefsel. Na twee dagen blootstelling aan hoge glucose sijpelden zowel kleine als grote kleurstofmoleculen meer in de hersenen, vooral bij de hogere suikerdosis, wat aangeeft dat de barrière doorlaatbaarder was geworden.
Wat er met de vaatwand gebeurt
Naast het eenvoudig meten van lekkage bouwde het team een multimodale “toolbox” om te onderzoeken wat er misging in de vaatwand zelf. Ze maten de breedte van een belangrijke hersenarterie en vonden dat hoge glucose de vaat deed verwijden — een vroege verandering die ook bij mensen met diabetische oogaandoeningen wordt gezien. Met zebravissen die zo waren gemonteerd dat specifieke eiwitten oplichten, toonden ze aan dat hoge glucose de niveaus van claudin-5 verminderde, een belangrijk onderdeel van de strakke sluitingen tussen aangrenzende vatenbekercellen, en de niveaus van PLVAP verhoogde, een eiwit dat geassocieerd wordt met onrijpe, lekgevoelige vaten die materiaal over de cellaag transporteren. Elektronenmicroscopie, die structuren op nanometerschaal kan onthullen, bevestigde subtiele verwijding bij juncties tussen cellen, hoewel de piepkleine transportzakjes genaamd caveolae in deze eerste analyse te schaars waren om betrouwbaar te kwantificeren.
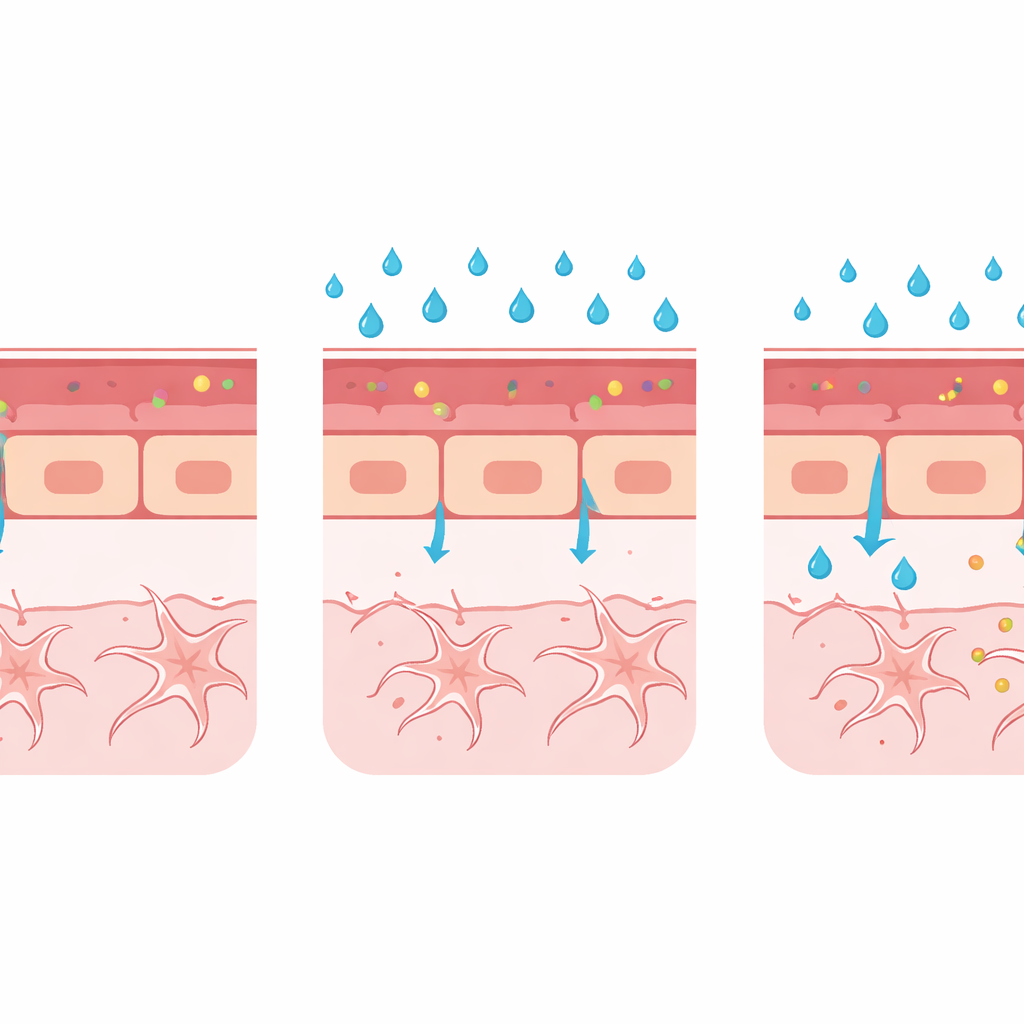
Een flexibel platform voor toekomstig ziekteonderzoek
Gezamenlijk schetsen deze veranderingen — meer kleurstoflekkage, wijde vaten, zwakkere celverbindingen en verhoogde PLVAP — een consistent beeld: hoge bloedsuiker kan de juiste barrièrevorming in de zich ontwikkelende hersenen vertragen of verstoren. Het model brengt nog niet de afbraak van een volledig rijpe barrière in kaart, zoals die voorkomt bij chronische menselijke ziekte, maar het blinkt uit in het laten zien hoe schadelijke omstandigheden tijdens de ontwikkeling kunnen voorkomen dat de barrière ooit goed afsluit. Omdat de technieken compatibel zijn met verschillende fluorescerende reporterlijnen en geavanceerde beeldvorming, kan hetzelfde platform worden uitgebreid om andere triggers van barrièrefalen te bestuderen, zoals ontstekingsmoleculen, veranderde ondersteunende cellen zoals pericyten en gliacellen, of verstoringen in sleutel-signaalroutes.
Wat dit betekent voor patiënten
Voor niet-specialisten is de kernboodschap dat dit werk een praktisch, levend testplatform levert om te zien hoe de beschermende wand van de hersenen onder stress faalt, met kleine transparante vissen in plaats van grotere zoogdieren. Door in realtime te volgen hoe hoge bloedsuiker de structuur en werking van vaten hervormt, kunnen onderzoekers sneller bepalen welke moleculen en celtypen ze moeten aanpakken om de barrière intact te houden. Uiteindelijk kunnen zulke inzichten de ontwikkeling van nieuwe geneesmiddelen of behandelstrategieën sturen om vochtlekkage in ogen en hersenen te voorkomen of te verminderen — met als doel het gezichtsvermogen te behouden en de cognitieve functie te beschermen bij mensen met diabetes en andere neurovasculaire ziekten.
Bronvermelding: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Trefwoorden: bloed-hersenbarrière, zebravismodel, diabetische complicaties, vasculaire lekkage, neurovasculaire ziekte