Clear Sky Science · nl
Integratieve profilering van het transcriptoom en H3K27ac-modificatie onthult veranderingen geassocieerd met BCG-geïnduceerde getrainde immuniteit in boviene immuuncellen
Waarom het trainen van het immuunsysteem ertoe doet
Virussen worden doorgaans ontworpen om het lichaam te trainen om één specifiek microbe te bestrijden. Maar in het afgelopen decennium hebben wetenschappers ontdekt dat sommige vaccins het immuunsysteem ook een algemenere fitheidstoename geven, waardoor het sneller en sterker kan reageren op veel verschillende dreigingen. Deze studie onderzoekt hoe het al lang gebruikte tuberculosevaccin, BCG genoemd, de frontlinie van de immuunverdediging bij jonge runderen hervormt, en biedt aanwijzingen die de diergezondheid kunnen verbeteren, de ontwikkeling van menselijke vaccins kunnen informeren en ons begrip van "aangeboren immuuns geheugen" kunnen verdiepen.
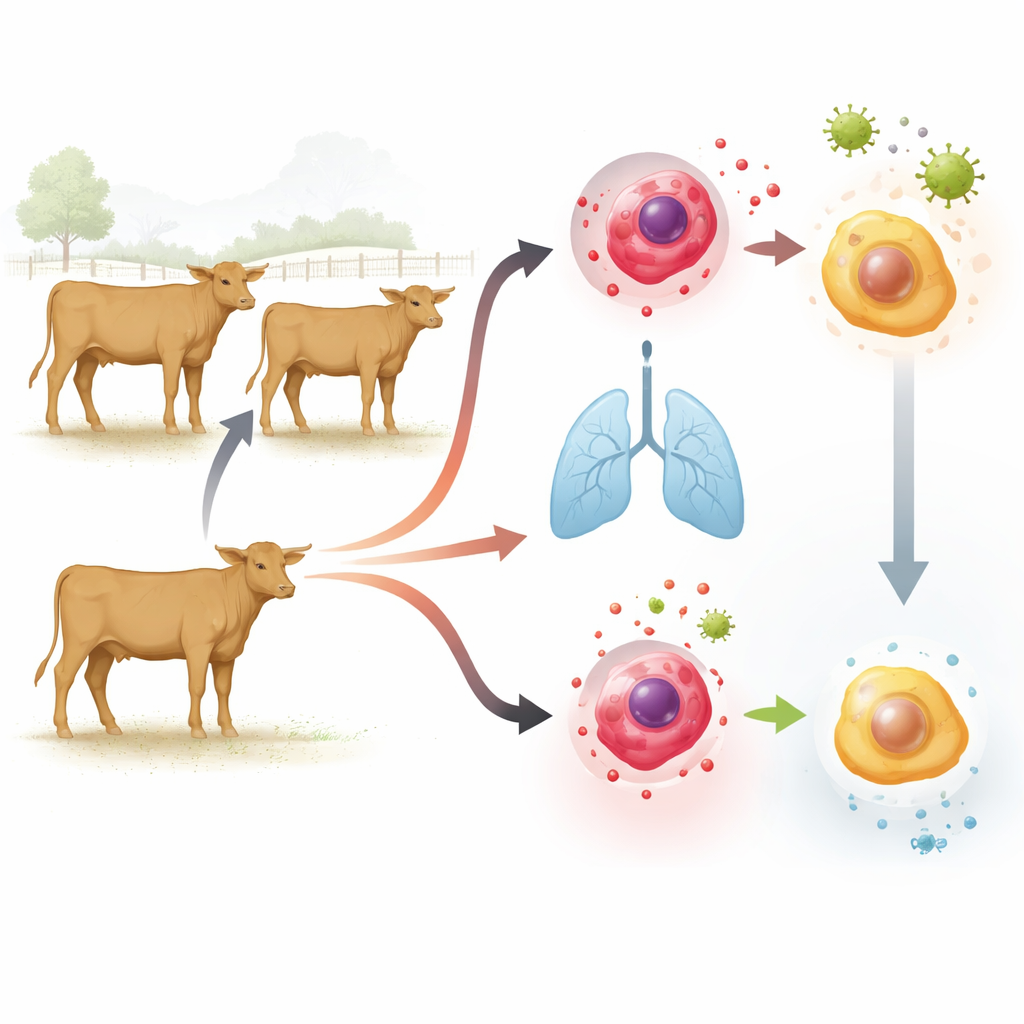
Een klassiek vaccin met een bredere wending
BCG wordt al een eeuw gebruikt om tuberculose bij mensen te voorkomen en wordt ook aan runderen gegeven om tegen boviene tuberculose te beschermen. Vreemd genoeg laten kinderen die BCG krijgen vaak lagere sterftecijfers zien door infecties die niets met tuberculose te maken hebben. Dit wekte het idee dat BCG aangeboren immuuncellen kan "trainen"—de snel reagerende cellen die binnen uren, niet dagen, reageren. In eerder werk toonden de auteurs aan dat kalveren die BCG kregen, later meer ontstekingssignaalstoffen, cytokinen genoemd, produceerden wanneer hun immuuncellen opnieuw werden uitgedaagd. In de huidige studie stelden ze een diepere vraag: wat verandert er binnen die cellen zodat ze weken na vaccinatie anders reageren?
Hoe het team immuungeheugen bij kalveren testte
De onderzoekers werkten met twintig jonge Holstein–Angus vaarsjes. De helft kreeg twee doses BCG onder de huid, met twee weken ertussen; de andere helft kreeg als controle zoutoplossing. Enkele weken later verzamelden ze twee typen immuuncellen: monocyten die in het bloed circuleren en macrofagen die in de longblaasjes wonen. In het lab stelden ze deze cellen bloot aan verschillende alarmsignalen die virale en bacteriële indringers nabootsen en maten hoeveel IL‑1β en IL‑6—twee belangrijke ontstekingscytokinen—de cellen produceerden. Ze gebruikten ook next-generation sequencing om te profileren welke genen aan- of uitgingen en brachten chemische labels in kaart op DNA-verpakkende eiwitten (histonen) die helpen genactiviteit te reguleren.
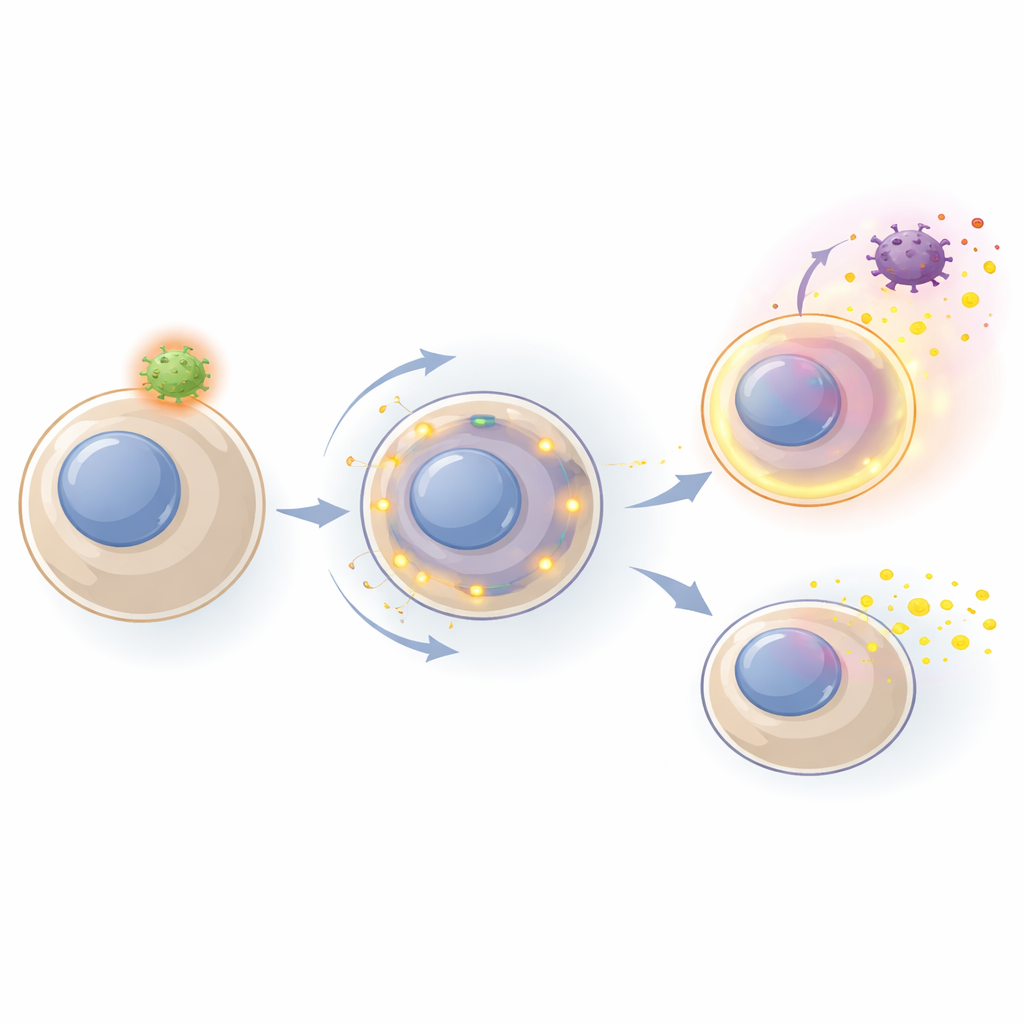
Sterkere signalen van getrainde frontlijncellen
Monocyten van BCG-gevaccineerde kalveren gedroegen zich duidelijk anders. Bij stimulatie scheidden ze meer IL‑1β en IL‑6 uit dan monocyten van niet-gevaccineerde dieren, vooral als reactie op een synthetisch virusachtig signaal. Op genniveau schakelden deze monocyten een breder scala aan genen in na herstimulatie en toonden ze sterkere activatie van routes die verband houden met aangeboren immuniteit en antimicrobiële verdediging. De versterkte respons schakelde genen niet op een volledig nieuwe manier van "uit" naar "aan"; in plaats daarvan versterkte ze bestaande patronen, waarbij veel van dezelfde genen reageerden maar in grotere mate. In de long toonden residentiële macrofagen een bescheidener trainingseffect—met name een hogere IL‑1β-productie als reactie op een bacterieel signaal—wat aangeeft dat verschillende weefsels in verschillende mate training kunnen ondergaan.
Verborgen merken die herinnering vasthouden
Om te achterhalen hoe cellen de eerdere BCG-blootstelling "onthielden", onderzochten de wetenschappers een specifiek histonmerk dat H3K27ac wordt genoemd, geassocieerd met actieve schakelaars in het genoom. Weken na vaccinatie vonden ze honderden regio's in monocyten- en longmacrofagen-DNA waar dit merk veranderd was in BCG-behandelde dieren vergeleken met controles. In monocyten lagen veel van deze veranderingen nabij genen die betrokken zijn bij immuunregulatie en cytokinecontrole, wat suggereert dat BCG blijvende chemische sporen nalaat die bepaalde genen later gemakkelijker in- of uitschakelbaar maken. Sommige van de veranderde regio's overlappen met locaties die in menselijke studies zijn geïdentificeerd, wat suggereert dat delen van dit trainingsprogramma soortenoverschrijdend zijn, terwijl veel andere regio's schijnbaar runderspecifiek waren.
Wat dit betekent voor dier- en mensgezondheid
Al met al tonen de bevindingen aan dat een standaard BCG-injectie de vroege immuunverdediging van runderen kan herstructureren: hun monocyten en longmacrofagen worden beter in staat sterke ontstekingsreacties los te laten wanneer ze nieuwe bedreigingen tegenkomen. Deze verschuiving houdt niet alleen verband met wat de cellen doen—meer cytokinen afscheiden en meer genen activeren—maar ook met hoe hun genetisch materiaal is verpakt en gemarkeerd. Voor de niet-specialist is het kernidee dat aangeboren immuuncellen niet zo "vergeetachtig" zijn als vroeger werd gedacht. In plaats daarvan kunnen ze een biochemisch geheugen van eerdere uitdagingen dragen dat hen helpt de volgende keer krachtiger te reageren. Het begrijpen en benutten van dit soort getrainde immuniteit kan leiden tot slimmere vaccinstrategieën en robuustere veestapels, en kan zelfs nieuwe benaderingen inspireren om de menselijke veerkracht tegen een breed scala aan infecties te vergroten.
Bronvermelding: Samuel, B.E.R., Yang, P., Tuggle, C.K. et al. Integrative profiling of transcriptome and H3K27ac modification reveals changes associated with BCG-induced trained immunity in bovine immune cells. Sci Rep 16, 8216 (2026). https://doi.org/10.1038/s41598-026-39580-7
Trefwoorden: getrainde immuniteit, BCG-vaccin, rundveegezondheid, innate immuuncellen, epigenetische veranderingen