Clear Sky Science · nl
Genomische en in vitro karakterisering van twee lytische bacteriofagen die de multiresistente Erwinia sp.-stam AnSW2-5 infecteren
Waarom door gewassen gedode bacteriën iedereen aangaan
Wereldwijd bestrijden landbouwers bacteriële ziekten die vruchten rotten, bladeren verschrompelen en oogsten verwoesten. Veel van deze uitbraken worden tegenwoordig veroorzaakt door stammen die niet langer reageren op gangbare antibiotica, wat zowel de voedselvoorziening als de inkomens die ervan afhangen bedreigt. Deze studie onderzoekt een opkomend alternatief: het gebruik van virussen die bacteriën aanvallen, zogenaamde bacteriofagen, om op een veilige manier een bijzonder hardnekkige plantpathogeen uit de grond — verbonden aan intensief antibioticagebruik — uit te schakelen.
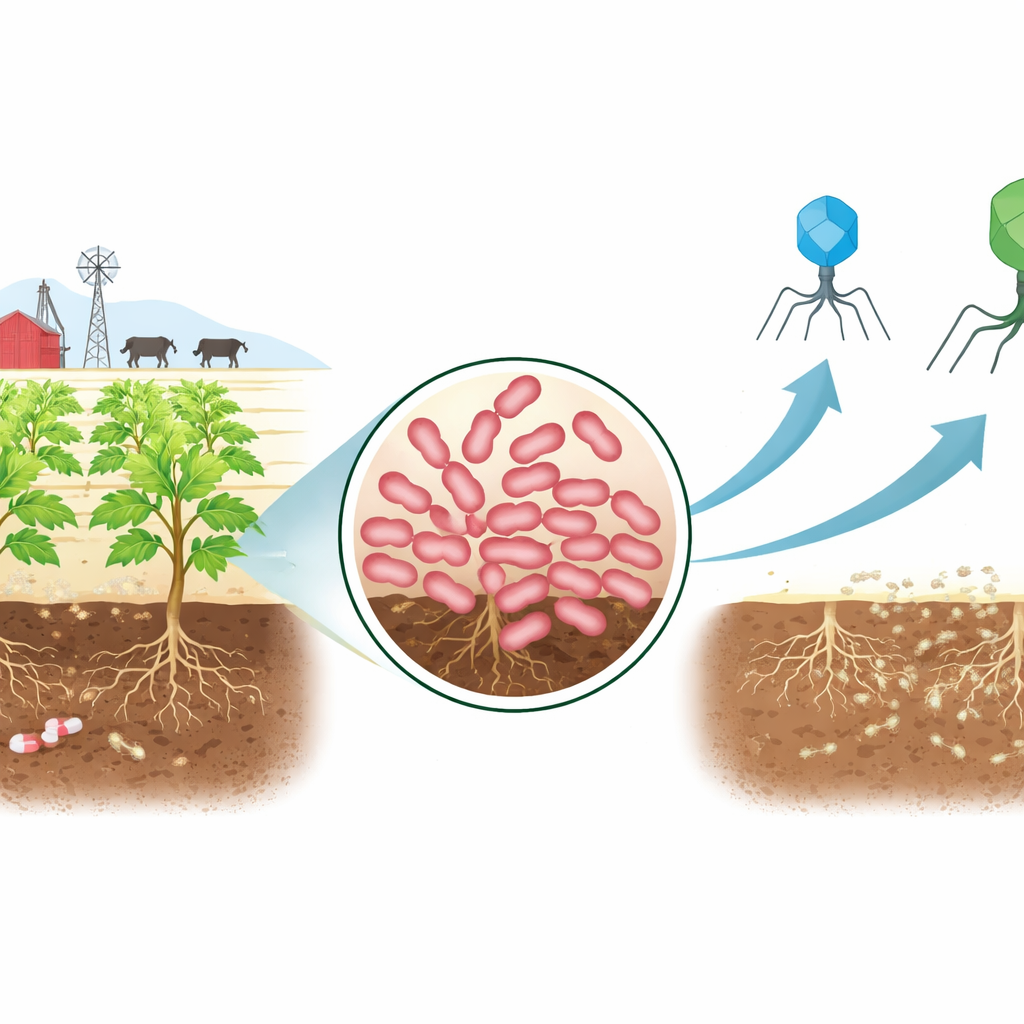
Een taaie nieuwe indringer op het erf
De onderzoekers begonnen met het bemonsteren van grond uit een veeweide waarvan bekend is dat daar dierlijke mest en antibiotica worden toegepast. Uit deze uitdagende omgeving isoleerden ze een Erwinia-stam, een bacteriegroep die beruchte ziekteverwekkers omvat, zoals de veroorzakers van vuurbrand bij appels en zachte rot bij aardappelen. Tests toonden aan dat deze stam, AnSW2-5 genoemd, bestand was tegen meerdere belangrijke antibioticaklassen, waaronder middelen die tegen een brede reeks infecties worden ingezet. Genetische analyse verklaarde waarom: het DNA droeg meerdere bekende resistentiegenen en krachtige moleculaire pompen die antibiotica uit de cel verwijderen. Tegelijkertijd lieten genoomvergelijkingen zien dat deze stam verschilt van eerder beschreven Erwinia-soorten, wat haar tot een nuttig model maakt om te bestuderen hoe nieuwe, moeilijk behandelbare plantpathogenen te beheersen zijn.
Twee piepkleine predatoren met verschillende krachten
Om natuurlijke vijanden van deze multiresistente bacterie te vinden, haalde het team water uit hetzelfde gebied en verrijkte het op bacteriofagen die AnSW2-5 konden infecteren. Ze isoleerden twee veelbelovende kandidaten, aangeduid als P-A en P-K. Onder de elektronenmicroscoop leek P-A compact met een korte staart, een ontwerp dat geassocieerd wordt met snelle, directe infectie. P-K droeg daarentegen een langere, contractiele staart met een complex basisstructuur, wat wijst op een krachtigere manier om de gastheercel binnen te dringen. Het sequentiëren van hun genomen toonde aan dat beide faagtypes strikt lytisch zijn: ze dringen binnen, repliceren en doen de cel barsten, in plaats van zich stil in het bacteriële DNA te verbergen. Toch gebruiken ze heel verschillende genetische gereedschapskisten — het gestroomlijnde genoom van P-A ondersteunt een snelle aanval, terwijl het grotere genoom van P-K meer uitgewerkte structurele en replicatiemechanismen codeert.
Hoe het virale team aanvalt
Toen de wetenschappers de levenscyclus van elke faag in het laboratorium volgden, bleek dat P-A snel toeslaat: het heeft slechts ongeveer 20 minuten nodig voordat nieuwe virale deeltjes verschijnen, en elke geïnfecteerde bacterie geeft ongeveer 70 nakomelingen vrij. P-K doet er langer over — ongeveer 35 minuten voordat het nieuwe faagdeeltjes begint te produceren — maar elke geïnfecteerde cel levert ongeveer 110 nieuwe deeltjes op. In cocultuurtests waarbij bacteriën en faag samen drie dagen groeien, remden beide faagtypes afzonderlijk de bacteriegroei maar voorkwamen die niet volledig. De bacteriën herstelden zich uiteindelijk, wat duidt op het verschijnen van resistente overlevenden. Wanneer P-A en P-K echter werden gecombineerd in één cocktail, verminderden ze de bacteriële populatie met meer dan 80% en hielden die onderdrukking gedurende het volledige 72-uur durende experiment in stand.
Weerstand geen kans geven
Een van de meest opvallende bevindingen was hoe het faagpaar de opkomst van resistente mutanten beïnvloedde. Bij blootstelling aan alleen P-A of P-K slaagde een klein deel van de bacteriën — ruwweg één op een miljoen tot één op tien miljoen — erin te ontsnappen en te groeien ondanks faagaanval. Maar wanneer beide faagtypes samen werden gebruikt, werden resistente kolonies zo zeldzaam dat ze onder de detectiegrens van het experiment vielen. Dit suggereert dat de twee virussen waarschijnlijk aan verschillende doelen op het bacteriële oppervlak binden of de cel op complementaire manieren verstoren. Voor één bacterie om te overleven, zou hij beide tegelijk moeten overwinnen — een vrijwel onwaarschijnlijke gebeurtenis. In praktische termen maakt dit het mengsel veel robuuster tegen de evolutionaire trucs die vaak antibiotica tenietdoen.
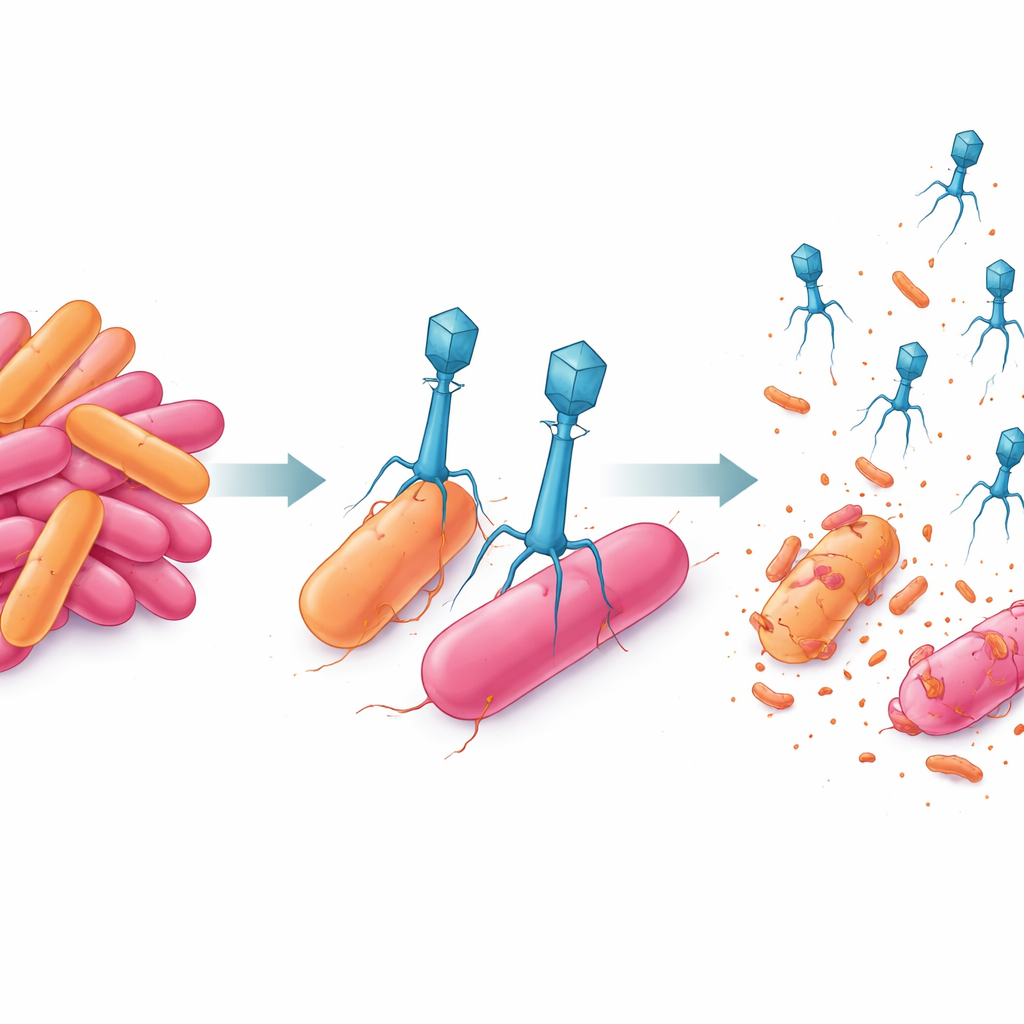
Wat dit kan betekenen voor toekomstige oogsten
Alles bij elkaar toont het werk aan dat zorgvuldig gekozen paren van bacteriofagen meer kunnen dan gevaarlijke plantbacteriën alleen onderdrukken — ze kunnen ook de mogelijkheid van de bacteriën om resistentie te ontwikkelen sterk beperken. Door een snelwerkende faag te combineren met een faag die grotere aantallen nakomelingen produceert, creëerden de onderzoekers een viraal team dat een multiresistente Erwinia-stam dagenlang onder controle hield terwijl detecteerbare ontsnappingen werden voorkomen. Hoewel deze proeven in het laboratorium en niet in boomgaarden of op proefvelden zijn uitgevoerd, wijzen ze op een toekomst waarin gerichte faagmengsels deel uitmaken van geïntegreerde plaagbestrijding, en boeren helpen gewassen te beschermen met veel minder afhankelijkheid van traditionele antibiotica.
Bronvermelding: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Trefwoorden: bacteriofaag biocontrole, plantenziekten veroorzaakt door bacteriën, antibioticaresistentie in de landbouw, Erwinia-faagtherapie, faagmengsels